30.08.2019
Tillverkningsteknik av aluminium. Den tekniska processen för aluminiumproduktion
1.1 Få aluminiumoxid från malmer
Aluminiumoxid produceras på tre sätt: alkaliskt, surt och elektrolytiskt. Den alkaliska metoden används mest (metoden enligt K. I. Bayer, utvecklad i Ryssland i slutet av seklet före sist och användes för bearbetning av högklassig bauxit med en liten mängd (upp till 5-6%) kiseldioxid). Sedan dess har dess tekniska implementering förbättrats avsevärt. Produktionen av aluminiumoxid enligt Bayer-metoden visas i fig. 1.
Kärnan i metoden är att aluminiumlösningar snabbt sönderdelas när aluminiumhydroxid införs i dem, och lösningen som återstår efter sönderdelning efter indunstning under kraftig omröring vid 169-170 ° C kan återupplösa aluminiumoxiden som finns i bauxit. Denna metod består av följande grundläggande operationer:
Beredning av bauxit, bestående av krossning och slipning i kvarnar; bauxit, kaustisk alkali och en liten mängd kalk matas till kvarnen, vilket förbättrar frisättningen av Al203; den resulterande massan matas till urlakning;
Utlakning av bauxit (nyligen använda runda autoklavblock har delvis ersatts av rörformiga autoklaver i vilka urlakning sker vid temperaturer på 230-250 ° C (500-520 K)), som består i dess kemiska sönderdelning från interaktion med en vattenhaltig alkalilösning; hydrater av aluminiumoxid i kontakt med alkali passerar in i lösningen i form av natriumaluminat:
AlOOH + NaOH → NaAlO 2 + H20
Al (OH) 3 + NaOH → NaAl02 + 2H20;
SiO2 + 2NaOH → Na2 Si03 + H20;
i en lösning bildar natriumaluminat och natriumsilikat olösligt natriumaluminosilikat; oxider av titan och järn passerar in i den olösliga återstoden, vilket gör återstoden röd; denna rest kallas röd lera. Efter avslutad upplösning utspädes det erhållna natriumaluminatet med en vattenhaltig alkalilösning under sänkning av temperaturen med 100 ° C;
Separationen av aluminatlösning från röd lera utförs vanligtvis genom tvättning i speciella förtjockningsmedel; som ett resultat sedimenterar den röda leran, och aluminatlösningen dräneras och filtreras sedan (klargörs). I begränsade mängder används slam till exempel som tillsats till cement. Beroende på kvaliteten på bauxit utgör 1–1 ton erhållen aluminiumoxid 0,6–1,0 ton röd lera (torr rest);
Nedbrytning av aluminatlösning. Det filtreras och pumpas i stora behållare med blandare (sönderdelare). Efter kylning vid 60 ° C (330 K) och konstant omrörning extraheras aluminiumhydroxid Al (OH) 3 från den övermättade lösningen. Eftersom denna process fortskrider långsamt och ojämnt, och bildningen och tillväxten av kristaller av aluminiumhydroxid är av stor betydelse under dess vidare bearbetning, tillsätts en stor mängd fast hydroxid till sönderdelarna:
Na20 OW Al203 + 4H20 → Al (OH) 3 + 2NaOH;
Tilldelning av aluminiumhydroxid och dess klassificering; detta inträffar i hydrocykloner och vakuumfilter, där en fällning som innehåller 50-60% Al (OH) -partiklar isoleras från en aluminatlösning. En betydande del av hydroxiden återförs till nedbrytningsprocessen som ett utsädesmaterial, som förblir i cirkulation i konstanta mängder. Återstoden efter tvättning med vatten går till kalcinering; filtratet återförs också till cirkulation (efter koncentration i förångare, för att läcka ut ny bauxit);
Dehydrering av aluminiumhydroxid (kalcinering); detta är den slutliga aluminiumoxidproduktionen; det utförs i rörformiga ugnar, och nyligen också i ugnar med turbulent rörelse av materialet vid en temperatur av 1150-1300 ° C; rå aluminiumhydroxid, som passerar genom en roterande ugn, torkas och dehydratiseras; vid uppvärmning sker följande strukturella transformationer sekventiellt:
| Al (OH) 3 → AlOOH → γ-Al203 → α-Al203 |
I den slutligen kalcinerade aluminiumoxiden innehåller 30-50% a-Al203 (korund), resten är y-Al203.
Denna metod extraherar 85-87% av den totala erhållna aluminiumoxiden. Den resulterande aluminiumoxiden är en stark kemisk förening med en smältpunkt 2050 ungefär C.
1.2 Få aluminium från sin oxid
Den elektrolytiska reduktionen av aluminiumoxid upplöst i en smälta baserad på kryolit utförs vid 950-970 ° C i en elektrolysator. Cellen består av ett bad fodrat med kolblock, till vars botten en elektrisk ström tillförs. Flytande aluminium som frigörs på botten som tjänar som katoden är tyngre än det smälta saltet av elektrolyten, varför det samlas upp på en kolbas, varifrån den periodiskt pumpas ut (Fig. 2). Uppifrån nedsänks kolanoder i elektrolyten, som brinner ut i atmosfären av syre frisatt från aluminiumoxid, vilket frisätter kolmonoxid (CO) eller koldioxid (CO 2). I praktiken används två typer av anoder:
a) självbakande Zederberg-anoder, bestående av briketter, de så kallade "bröden" av Zederberg-massan (kol med låg ask med 25-35% koltjärstopp) fyllda i ett aluminiumskal; under påverkan av hög temperatur förbränns (sintrad) anodmassan;
b) glödgade, eller "kontinuerliga", anoder från stora kolblock (till exempel 1900 × 600 × 500 mm som väger cirka 1,1 ton).
Strömstyrkan på elektrolysatorerna är 150 000 A. De är anslutna till nätverket i serie, det vill säga ett system (serie) erhålls - en lång serie elektrolysatorer.
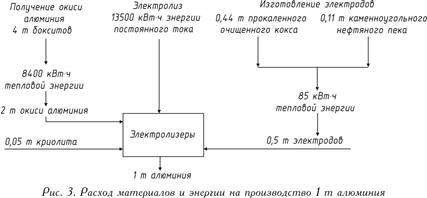
Driftspänningen på badet, som är 4-5 V, är betydligt högre än den spänning vid vilken sönderdelningen av aluminiumoxid inträffar, eftersom spänningsförluster i olika delar av systemet är oundvikliga under drift. Balansen mellan råmaterial och energi vid produktion av 1 ton aluminium presenteras i fig. 3.
Elektrolys av aluminiumklorid (Alcoa-metoden)
I reaktionskärlet omvandlas aluminiumoxid först till aluminiumklorid. Sedan, i ett tätt isolerat bad, sker elektrolys av AlCl3 upplöst i det smälta saltet av KCl, NaCl. Klor som frigörs under denna process sugs av och levereras för sekundär användning; aluminium deponeras vid katoden.
Fördelarna med denna metod jämfört med den befintliga elektrolysen av flytande kryolit-aluminiumoxidsmälta (Al203, upplöst i kryolit Na 3 AlF 6) är: spara upp till 30% energi; möjligheten att använda aluminiumoxid, som inte är lämplig för traditionell elektrolys (till exempel Al203 med högt kiselinnehåll); ersätta dyra kryolit med billigare salter; försvinnandet av faran för fluorutsläpp.
Reduktion av aluminiumklorid med mangan (Toth - metod)
När mangan reduceras från aluminiumklorid frigörs aluminium. Genom kontrollerad kondensation frigörs klorrelaterade föroreningar från mangankloridströmmen. När klor frisätts oxideras manganklorid till manganoxid, som sedan reduceras till återvinningsbar mangan. Informationen i befintliga publikationer är mycket felaktig, så i detta fall måste du överge utvärderingen av metoden.
En mycket tvivelaktig legend säger att en gång kom en man med en metall, oförstörbar skål till den romerska kejsaren Tiberius (42 f.Kr. - 37 e.Kr.). Skålmaterialet var påstås erhållet från aluminiumoxid (Al203) och måste därför vara aluminium. I fruktan för att sådan lermetall skulle kunna avskriva guld och silver beordrade Tiberius mannen att avskäras för fall. Naturligtvis är denna historia svår att tro: nativt aluminium förekommer inte i naturen, och under Romerrikets tid kunde det inte finnas några tekniska medel som skulle tillåta aluminium att utvinnas från dess föreningar.
När det gäller prevalens i naturen rankas aluminium först bland metaller; dess innehåll i jordskorpan är 7,45%. Trots dess utbredda förekomst i naturen var aluminium dock en av de sällsynta metallerna fram till slutet av 1800-talet. I sin rena form förekommer inte aluminium på grund av dess höga kemiska aktivitet. Det finns främst i form av föreningar med syre och kisel - aluminiumsilikater.
Aluminiummalmer kan endast tjäna stenar som är rika på aluminiumoxid (Al 2 O 3) och som förekommer i stora massor på jordens yta. Sådana bergarter inkluderar bauxit, nefelin - (Na, K) 2 O ּ Al 2 O 3 ּ 2 SiO 2, aluniter - (Na, K) 2 SO 4 ּ Al 2 (SO 4) 3 ּ 4 Al (OH) 3 och kaoliner (lera), fält spar (ortoklas) - K 2 O O Al 2 O 3 3 6 SiO 2.
Huvudmalmen för aluminiumproduktion är bauxit. Aluminiumet i dem finns i form av hydroxider Al (OH), AlOOH, korund Al 2 O 3 och kaolinit Al 2 0 3 ּ 2 SiO 2 ּ 2 H 2 O. Den kemiska sammansättningen av bauxit består av: 28-70% aluminiumoxid; 0,5-20% kiseldioxid; 2-50% järnoxid; 0,1-10% titanoxid. Nyligen har nefelin och alunit använts som malm.
Stora bauxitavlagringar finns i Ural, i Tikhvin-regionen i Leningrad-regionen, i Altai och Krasnoyarsk territorier.
Nepheline (K ּ Na 2 O ּ Al 2 O 3 ּ 2 SiO 2) är en del av apatitonefelinbergarter (på Kola-halvön).
För första gången i fri form isolerades aluminium 1825 av den danska fysikern Oersted genom verkan av kaliumamalgam på aluminiumklorid. 1827 Den tyska kemisten Weller förbättrade Oersteds metod genom att ersätta kaliumamalgam med metalliskt kalium:
AlCl 3 + 3K → 3KCl + Al (reaktionen fortsätter med frisläppande av värme).
1854 använde St. Clair Deville i Frankrike Weler-metoden för industriell produktion av aluminium, med billigare natrium istället för kalium, och istället för hygroskopisk aluminiumklorid, en mer stabil dubbel aluminiumklorid och natrium. År 1865 visade den ryska fysiker-kemisten NN Beketov möjligheten att förskjuta aluminium med magnesium från smält kryolit. Denna reaktion användes 1888 för att producera aluminium vid den första tyska fabriken i Gmelingen. Aluminiumproduktion med dessa så kallade "kemiska" metoder genomfördes från 1854 till 1890. Under 35 år med dessa metoder erhölls totalt cirka 20 ton aluminium.
I slutet av 80-talet före århundradet ersatte kemiska metoder den elektrolytiska metoden, vilket gjorde det möjligt att kraftigt sänka aluminiumkostnaderna och skapade förutsättningarna för en snabb utveckling av aluminiumindustrin. Grundarna av den moderna elektrolytiska metoden för framställning av aluminium, Eru i Frankrike och Hall i USA inlämnade oberoende 1886 nästan samma ansökningar om patent på en metod för framställning av aluminium genom elektrolys av aluminiumoxid upplöst i smält kryolit. Sedan Eru- och Hall-patentet har börjat har den moderna aluminiumindustrin börjat, som på mer än 115 år av sin existens har vuxit till en av de största industrierna inom metallurgi.
Processen för att producera aluminium består av tre huvudsteg:
1). Erhålla aluminiumoxid (Al203) från aluminiummalmer;
2). Erhålla aluminium från aluminiumoxid;
3). Raffinering av aluminium.
Få aluminiumoxid från malmer.
Aluminiumoxid produceras på tre sätt: alkaliskt, surt och elektrolytiskt. Den alkaliska metoden används mest (metoden enligt K. I. Bayer, utvecklad i Ryssland i slutet av seklet före sist och användes för bearbetning av högklassig bauxit med en liten mängd (upp till 5-6%) kiseldioxid). Sedan dess har dess tekniska implementering förbättrats avsevärt. Produktionen av aluminiumoxid enligt Bayer-metoden visas i fig. 1.
Kärnan i metoden är att aluminiumlösningar snabbt sönderdelas när aluminiumhydroxid införs i dem, och lösningen som återstår efter sönderdelning efter indunstning under kraftig omröring vid 169-170 ° C kan återupplösa aluminiumoxiden som finns i bauxit. Denna metod består av följande grundläggande operationer:
1). Beredning av bauxit, bestående av krossning och slipning i kvarnar; bauxit, kaustisk alkali och en liten mängd kalk matas till kvarnen, vilket förbättrar frisättningen av Al203; den resulterande massan matas till urlakning;
2). Utlakning av bauxit (nyligen använda runda autoklavblock har delvis ersatts av rörformiga autoklaver i vilka urlakning sker vid temperaturer på 230-250 ° C (500-520 K)), som består i dess kemiska sönderdelning från interaktion med en vattenhaltig alkalilösning; hydrater av aluminiumoxid i kontakt med alkali passerar in i lösningen i form av natriumaluminat:
AlOOH + NaOH → NaAlO 2 + H20
Al (OH) 3 + NaOH → NaAl02 + 2H20;
SiO2 + 2NaOH → Na2 Si03 + H20;
i en lösning bildar natriumaluminat och natriumsilikat olösligt natriumaluminosilikat; oxider av titan och järn passerar in i den olösliga återstoden, vilket gör återstoden röd; denna rest kallas röd lera. Efter avslutad upplösning utspädes det erhållna natriumaluminatet med en vattenhaltig alkalilösning under sänkning av temperaturen med 100 ° C;
3). Separationen av aluminatlösning från röd lera utförs vanligtvis genom tvättning i speciella förtjockningsmedel; som ett resultat sedimenterar den röda leran, och aluminatlösningen dräneras och filtreras sedan (klargörs). I begränsade mängder används slam till exempel som tillsats till cement. Beroende på kvaliteten på bauxit utgör 1–1 ton erhållen aluminiumoxid 0,6–1,0 ton röd lera (torr rest);
4). Nedbrytning av aluminatlösning. Det filtreras och pumpas i stora behållare med blandare (sönderdelare). Efter kylning vid 60 ° C (330 K) och konstant omrörning extraheras aluminiumhydroxid Al (OH) 3 från den övermättade lösningen. Eftersom denna process fortskrider långsamt och ojämnt, och bildningen och tillväxten av kristaller av aluminiumhydroxid är av stor betydelse under dess vidare bearbetning, tillsätts en stor mängd fast hydroxid till sönderdelarna:
Na20 OW Al203 + 4H20 → Al (OH) 3 + 2NaOH;
5). Tilldelning av aluminiumhydroxid och dess klassificering; detta inträffar i hydrocykloner och vakuumfilter, där en fällning som innehåller 50-60% Al (OH) -partiklar isoleras från en aluminatlösning. En betydande del av hydroxiden återförs till nedbrytningsprocessen som ett utsädesmaterial, som förblir i cirkulation i konstanta mängder. Återstoden efter tvättning med vatten går till kalcinering; filtratet återförs också till cirkulation (efter koncentration i förångare, för att läcka ut ny bauxit);
6). Dehydrering av aluminiumhydroxid (kalcinering); detta är den slutliga aluminiumoxidproduktionen; det utförs i rörformiga ugnar, och nyligen också i ugnar med turbulent rörelse av materialet vid en temperatur av 1150-1300 ° C; rå aluminiumhydroxid, som passerar genom en roterande ugn, torkas och dehydratiseras; vid uppvärmning sker följande strukturella transformationer sekventiellt:
| Al (OH) 3 → AlOOH → γ-Al203 → α-Al203 | |||
| 200 om C– | 950 о С– | 1200 om S. | |
I den slutligen kalcinerade aluminiumoxiden innehåller 30-50% a-Al203 (korund), resten är y-Al203.
Denna metod extraherar 85-87% av den totala erhållna aluminiumoxiden. Den resulterande aluminiumoxiden är en stark kemisk förening med en smältpunkt 2050 ungefär C.
Få aluminium från sin oxid
Elektrolys av aluminiumoxid
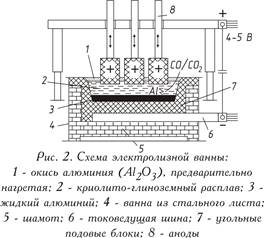 Den elektrolytiska reduktionen av aluminiumoxid upplöst i en smält baserad på kryolit utförs vid 950-970 ° C i en elektrolysator. Cellen består av ett bad fodrat med kolblock, till vars botten en elektrisk ström tillförs. Flytande aluminium som fälls ut på botten som tjänar som katoden är tyngre än elektrolyttsaltsmältan, varför det samlas upp på en kolbas, varifrån den periodiskt pumpas ut (Fig. 2). Uppifrån nedsänks kolanoder i elektrolyten, som brinner ut i atmosfären av syre frisatt från aluminiumoxid, vilket frisätter kolmonoxid (CO) eller koldioxid (CO 2). I praktiken används två typer av anoder:
Den elektrolytiska reduktionen av aluminiumoxid upplöst i en smält baserad på kryolit utförs vid 950-970 ° C i en elektrolysator. Cellen består av ett bad fodrat med kolblock, till vars botten en elektrisk ström tillförs. Flytande aluminium som fälls ut på botten som tjänar som katoden är tyngre än elektrolyttsaltsmältan, varför det samlas upp på en kolbas, varifrån den periodiskt pumpas ut (Fig. 2). Uppifrån nedsänks kolanoder i elektrolyten, som brinner ut i atmosfären av syre frisatt från aluminiumoxid, vilket frisätter kolmonoxid (CO) eller koldioxid (CO 2). I praktiken används två typer av anoder:
a) självbakande Zederberg-anoder, bestående av briketter, de så kallade "bröden" av Zederberg-massan (kol med låg ask med 25-35% koltjärstopp) fyllda i ett aluminiumskal; under påverkan av hög temperatur förbränns (sintrad) anodmassan;
b) glödgade, eller "kontinuerliga", anoder från stora kolblock (till exempel 1900 × 600 × 500 mm som väger cirka 1,1 ton).
Strömstyrkan för elektrolysatorerna är 150 000 A. De är anslutna till nätverket i serie, det vill säga ett system (serie) erhålls - en lång serie elektrolysatorer.
Driftspänningen på badet, som är 4-5 V, är betydligt högre än den spänning vid vilken sönderdelningen av aluminiumoxid inträffar, eftersom spänningsförluster i olika delar av systemet är oundvikliga under drift. Balansen mellan råmaterial och energi vid produktion av 1 ton aluminium presenteras i fig. 3.
Elektrolys av aluminiumklorid (Alcoa-metoden)
 I reaktionskärlet omvandlas aluminiumoxid först till aluminiumklorid. Därefter sker i ett tätt isolerat bad elektrolys av AlCl3 upplöst i det smälta saltet av KCl, NaCl. Klor som frigörs under denna process sugs av och levereras för sekundär användning; aluminium deponeras vid katoden.
I reaktionskärlet omvandlas aluminiumoxid först till aluminiumklorid. Därefter sker i ett tätt isolerat bad elektrolys av AlCl3 upplöst i det smälta saltet av KCl, NaCl. Klor som frigörs under denna process sugs av och levereras för sekundär användning; aluminium deponeras vid katoden.
Fördelarna med denna metod jämfört med den befintliga elektrolysen av flytande kryolit-aluminiumoxidsmälta (Al203, upplöst i kryolit Na 3 AlF 6) är: spara upp till 30% energi; möjligheten att använda aluminiumoxid, som inte är lämplig för traditionell elektrolys (till exempel Al203 med högt kiselinnehåll); ersätta dyra kryolit med billigare salter; försvinnandet av faran för fluorutsläpp.
Reduktion av aluminiumklorid med mangan (Toth - metod)
 När mangan reduceras från aluminiumklorid frigörs aluminium. Genom kontrollerad kondensation frigörs klorrelaterade föroreningar från mangankloridströmmen. När klor frisätts oxideras manganklorid till manganoxid, som sedan reduceras till återvinningsbar mangan. Informationen i befintliga publikationer är mycket felaktig, så i detta fall måste du överge utvärderingen av metoden.
När mangan reduceras från aluminiumklorid frigörs aluminium. Genom kontrollerad kondensation frigörs klorrelaterade föroreningar från mangankloridströmmen. När klor frisätts oxideras manganklorid till manganoxid, som sedan reduceras till återvinningsbar mangan. Informationen i befintliga publikationer är mycket felaktig, så i detta fall måste du överge utvärderingen av metoden.
Få raffinerad aluminium
För aluminium är det inte möjligt att raffinera elektrolys med sönderdelning av vattenhaltiga saltlösningar. Eftersom reningsgraden av industriellt aluminium (Al 99,5 - Al 99,8) för vissa ändamål erhållits genom elektrolys av en kryolit-aluminiumoxidsmälta är otillräcklig, erhålls ännu renare aluminium (Al 99, 99 R) från industriellt aluminium eller metallavfall genom raffinering. Den mest kända raffineringsmetoden är trelagselektrolys.
Trelags elektrolysraffinering
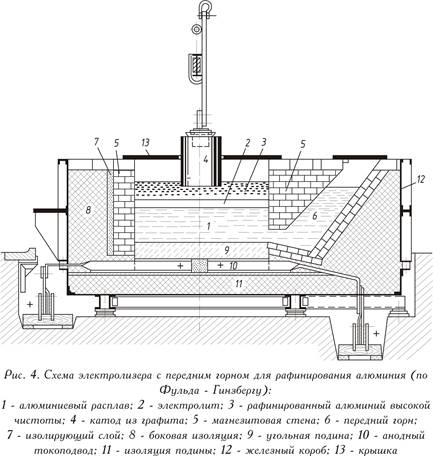
Klädd med en stålplåt, som arbetar vid likström (visas i fig. 4 - se ovan), består raffineringsbadet av en kolskärm med strömkablar och ett värmeisolerande magnesitfoder. I motsats till elektrolysen av kryolit-aluminiumoxidsmälta är den smälta raffinerade metallen (nedre anodskiktet) vanligen anoden här. Elektrolyten består av rena fluorider eller en blandning av bariumklorid och aluminium- och natriumfluorider (mellanlager). Aluminium som löses upp från anodskiktet i elektrolyten frigörs ovanför elektrolyten (övre katodskiktet). Ren metall tjänar som en katod. Strömmen tillförs katodskiktet av en grafitelektrod.
Badet arbetar vid 750-800 ° C, energiförbrukningen är 20 kW ּ h per 1 kg rent aluminium, dvs något högre än vid konventionell aluminiumelektrolys.
Anodens metall innehåller 25-35% Cu; 7-12% Zn; 6-9% Si; upp till 5% Fe och en liten mängd mangan, nickel, bly och tenn, resten (40-55%) är aluminium. Alla tungmetaller och kisel under raffinering förblir i anodskiktet. Närvaron av magnesium i elektrolyten leder till oönskade förändringar i sammansättningen av elektrolyten eller till dess starka slagg. För att avlägsna magnesium behandlas slagg som innehåller magnesium med flussmedel eller gasformigt klor.
Som ett resultat av raffinering erhålls ren aluminium (99,99%) och segregeringsprodukter (zagerprodukt), som innehåller tungmetaller och kisel och frigörs i form av en alkalisk lösning och en kristallin återstod. Den alkaliska lösningen är avfall och den fasta återstoden används för deoxidation.
Raffinerat aluminium har vanligtvis följande sammansättning,%: Fe 0,0005-0,002; Si 0,002-0,005; Cu 0,0005-0,002; Zn 0,0005-0,002; Mg-spår; Resten.
Raffinerat aluminium bearbetas till halvfabrik i den specificerade kompositionen eller legeras med magnesium (se tabell 1.2.).
TABELL 1.2. Den kemiska sammansättningen av aluminium med hög renhet och primärt aluminium enligt DIN 1712 , ark 1.
| mark | nummer | Tillåtna föroreningar *,% | |||||||
| bara | inklusive | ||||||||
| si | fe | Ti | Cu | Zn | andra | ||||
| A199,99R | 3.0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 | |
| A199,9H | 3.0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 | |
| A199,8H | 3.0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,7H | 3.0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,5H ** | 3.0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 | |
| A199H | 3.0200 | 1,0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 | |
* Så långt det är möjligt att bestämma med konventionella forskningsmetoder. ** Rent aluminium för elektroteknik (aluminiumledare) levereras i form av primärt aluminium 99,5, innehållande högst 0,03% (Ti + Cr + V + Mn); betecknas i detta fall av E-A1, materialnummer 3.0256. Annars överensstämmer den med VDE-0202. |
|||||||||
Raffinering med organoaluminiumkomplexföreningar och zonsmältning
Aluminium med en renhet högre än A1 99,99 R-kvalitet kan erhållas genom förädling av elektrolys av rent eller tekniskt rent aluminium med användning av komplexa aluminiumorganoaluminiumföreningar som en elektrolyt. Elektrolysen sker vid en temperatur av cirka 1000 ° C mellan fasta aluminiumelektroder och i princip liknar den raffineringselektrolysen av koppar. Elektrolytens natur dikterar behovet av att arbeta utan luft och med låg strömtäthet.
Denna typ av raffineringselektrolys, som ursprungligen endast används på laboratorieskala, genomförs redan i en liten produktionsskala - flera ton metall produceras per år. Den nominella reningsgraden för den resulterande metallen är 99.999-99.9999%. Potentiella tillämpningar för en metall av denna renhet är kryogen elektroteknik och elektronik.
Det är möjligt att använda den betraktade raffineringsmetoden vid elektroplätering.
Ännu högre renhet - nominellt upp till A1 99.99999 - kan erhållas genom efterföljande zonsmältning av metallen. Vid bearbetning av aluminium med hög renhet till en halvfabrik, ark eller tråd måste särskilda försiktighetsåtgärder vidtas, med hänsyn tagen till den låga omkristallisationen av metallen. En anmärkningsvärd egenskap hos raffinerad metall är dess höga elektriska konduktivitet i området för kryogena temperaturer.
Få sekundär aluminium
Bearbetning av sekundära råvaror och produktionsavfall är ekonomiskt hållbart. De resulterande sekundära legeringarna tillfredsställer cirka 25% av den totala aluminiumbehovet.
 Det viktigaste användningsområdet för sekundära legeringar är produktion av aluminiumformade gjutgods. I DIN 1725, ark 2, tillsammans med standardlegeringskvaliteter, anges många legeringskvaliteter producerade av gjuterier. Förteckningen över legeringar som produceras av dessa växter innehåller förutom standard några icke-standardlegeringar.
Det viktigaste användningsområdet för sekundära legeringar är produktion av aluminiumformade gjutgods. I DIN 1725, ark 2, tillsammans med standardlegeringskvaliteter, anges många legeringskvaliteter producerade av gjuterier. Förteckningen över legeringar som produceras av dessa växter innehåller förutom standard några icke-standardlegeringar.
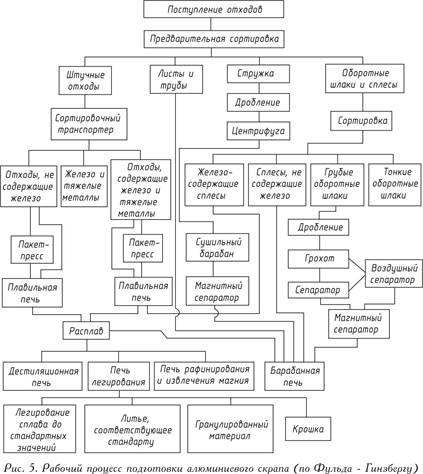
Felfri beredning av aluminiumskrot i många olika proportioner kan endast utföras i specialutrustade smältverk. Idén om ett komplext arbetsflöde vid en sådan anläggning ges i fig. 5.
Avfall omsmälts efter grov försortering. Det järn, nickel eller koppar som finns i detta avfall, vars smältpunkt är högre än smältpunkten för aluminium, kvarstår i det under smältningen i en smältgränsugn, och aluminium smälts. För att avlägsna icke-metalliska inneslutningar från avfall såsom oxider, nitrider, karbider eller gaser behandlas smält metall med salter eller (vilket är mer rationellt) gas blåses med klor eller kväve.
Olika metoder är kända för att avlägsna metalliska föroreningar från smältan, till exempel magnesiumtillsats och evakuering - Becksche-metoden; tillsatser av zink eller kvicksilver följt av evakuering - en subhalogenmetod. Avlägsnandet av magnesium är begränsat till införandet av klor i den smälta metallen. Genom att införa tillsatser exakt bestämda av smältans sammansättning erhålls en förbestämd gjuten legering.
Produktion av industriell aluminium
Den elektrolytiska metoden är den enda som används världen över för produktion av metalliskt aluminium av teknisk renhet. Alla andra metoder (zink-termisk, karbidotermisk, subklorid, nitrid, etc.), med vilka aluminium kan utvinnas från aluminiummalm, har utvecklats på laboratorie- och pilotskala, men har ännu inte hittat praktisk tillämpning.
För att erhålla aluminium-kisellegeringar används den elektrotermiska metoden, först utvecklad och implementerad i industriell skala i Sovjetunionen, med framgång. Den består av två steg: i det första steget erhålls en primär aluminium-kisellegering med ett innehåll av 60-63% Al genom direkt reduktion av aluminium-kiselmalmer i malm-termiska elektriska ugnar; i det andra steget utspädes den primära legeringen med teknisk aluminium, varvid man erhåller silumin och andra gjutna och smidda aluminium-kisellegeringar. Studier pågår för att utvinna aluminium av teknisk kvalitet från den primära legeringen.
I allmänhet inkluderar produktion av aluminium med den elektrolytiska metoden framställning av aluminiumoxid (aluminiumoxid) från aluminiummalmer, produktion av fluoridsalter (kryolit, aluminiumfluorid och natriumfluorid), produktion av kolanodmassa, kalcinerad kolanod och katodblock och andra fodermaterial, samt den faktiska elektrolytiska produktionen av aluminium, som är det sista steget i modern aluminiummetallurgi.
Karaktäristiskt för framställning av aluminiumoxid, fluoridsalter och kolprodukter är kravet för maximal materialrenhetsgrad för dessa material, eftersom kryolit-aluminiumoxidsmältor som utsätts för elektrolys inte bör innehålla föroreningar av element som är mer elektropositiva än aluminium, som, om de emitteras vid katoden först av allt, skulle förorena metall.
I aluminiumoxidkvaliteter G-00, G-0 och G-1, som huvudsakligen används vid elektrolys, är halten SiO2 0,02-0,05%, aFe203 - 0,03-0,05%. I genomsnitt innehåller kryolit 0,36-0,38% Si02 och 0,05-0,06% Fe203 och aluminiumfluorid 0,30-0,35% (SiO2 + Fe203). Anodmassan innehåller inte mer än 0,25% Si02 och 0,20% Fe203.
Den viktigaste aluminiummalmen från vilken aluminiumoxid, bauxit utvinns. I bauxit är aluminium närvarande i form av aluminiumhydroxid. I Sovjetunionen, förutom bauxit, används nefelinberg - natrium- och kaliumaluminosilikat, samt alunitberg, där aluminium är i form av sulfat, för att producera aluminiumoxid. Råvarorna för framställning av anodmassan och kalcinerade anodblock är koldioxidrena material - petroleum- eller tonkoks- och koltjärstopp som bindemedel och kalciumfluorid (fluorspar) för framställning av kryolit och andra fluoridsalter.
Vid elektrolytisk produktion av aluminium sönderdelas aluminiumoxid Al203 i smält kryolit Na 3 AlF 6 elektrokemiskt med urladdningen av aluminiumkationer vid katoden (flytande aluminium) och syreinnehållande joner (syrejoner) - vid kolanoden.
Enligt moderna begrepp dissocierar kryolit i smält tillstånd till joner och: och aluminiumoxid till komplexa joner och: ![]() som är i jämvikt med enkla joner:
som är i jämvikt med enkla joner: ![]() ,
, ![]() .
.
Den huvudsakliga processen som sker vid katoden är reduktion av trivalenta aluminiumjoner: Al 3+ + 3 e → Al (I).
Tillsammans med huvudprocessen är en ofullständig urladdning av trivalenta aluminiumjoner med bildning av monovalenta joner möjlig: Al 3+ + 2 e → Al + (II) och slutligen urladdningen av monovalenta joner med frisläppandet av metall: Al + + e → Al (III).
Under vissa förhållanden (relativt hög koncentration av Na + -joner, hög temperatur osv.) Kan ett utsläpp av natriumjoner inträffa med frisättningen av metall: Na + + e → Na (IV). Reaktionerna (II) och (IV) orsakar en minskning av den nuvarande aluminiumproduktionen.
Syrejoner släpps ut vid kolanoden: 2O 2– - 4 e → O 2. Syre frigörs emellertid inte i sin fria form, eftersom det oxiderar kolens anod för att bilda en blandning av CO 2 och CO.
Den totala reaktionen som inträffar i elektrolysatorn kan representeras av ekvationen Al203 + x C ^ 2Al + (2 x –3) CO + (3– x) CO 2.
Sammansättningen av elektrolyten i elektrolytiska celler av industriell aluminium, förutom huvudkomponenterna - kryolit, aluminiumfluorid och aluminiumoxid, innehåller små mängder (upp till 8-9%) av några andra salter - CaF 2, MgF 2, NaCl och LiF (tillsatser), som förbättrar vissa elektrolytens fysikalisk-kemiska egenskaper och därmed öka effektiviteten hos de elektrolytiska cellerna. Det maximala aluminiumoxidinnehållet i elektrolyten är vanligtvis 6-8%, vilket minskar under elektrolysen. När elektrolyten tappas ut aluminiumoxid införs en annan del aluminiumoxid i den. För normal drift av aluminiumelektrolysatorer bibehålles förhållandet NaF: AlF 3 i elektrolyten i området 2,7-2,8, vilket tillsätter delar av kryolit och aluminiumfluorid.
Vid tillverkning av aluminium används elektrolysatorer med själveldande kolanoder och sido- eller toppströmförsörjning samt elektrolysatorer med förbrända kolanoder. Den mest lovande designen av elektrolysatorer med bakade anoder, som gör det möjligt att öka enhetens effekt, minska den specifika likströmskonsumtionen för elektrolys, få renare metall, förbättra hygieniska och hygieniska arbetsförhållanden och minska utsläppen av skadliga ämnen i atmosfären.
I tabellen ges de viktigaste tekniska parametrarna och prestandaindikatorerna för aluminiumelektrolysatorer av olika typer. 1,3.
TABELL 1.3
GRUNDLÄGGANDE TEKNISKA PARAMETRAR OCH INDIKATORER FÖR ARBET FÖR ALUMINIUMELektrolyser
| Parametrar och indikatorer | Med självbakande anoder | Med brända anoder | |
lateral strömförsörjning |
högsta nuvarande ledning | ||
| Strömstyrka, kA | 60-120 | 60-155 | 160-255 |
| Elektrolysatorns dagliga produktivitet, t | 0,42-0,85 | 0,40-1,10 | 1,10-1,74 |
| Anodströmtäthet, A / cm 2 | 0,80-0,90 | 0,65-0,70 | 0,70-0,89 |
| Den genomsnittliga spänningen på cellen, V | 4,45-4,65 | 4,50-4,70 | 4,30-4,50 |
| Nuvarande produktion,% | 85-88 | 84-86 | 85-89 |
| Förbrukningsförhållanden per 1 ton aluminium: | |||
| dC-el, kW W h | 15100-16200 | 15500-17300 | 14500-15500 |
| aluminiumoxid, kg | 1920-1940 | 1920-1940 | 1920-1940 |
| anodmassa, kg | 520-560 | 560-620 | - |
| brända anoder, kg | - | - | 540-600 |
| Fluoridsalter i termer av fluor, kg | 20-30 | 25-35 | 15-25 |
Primärt aluminium extraherat från elektrolytiska celler (rått aluminium) innehåller ett antal föroreningar som kan delas in i tre grupper: icke-metalliska (fluoridsalter, α- och y-aluminiumoxid, aluminiumkarbid och nitrid, kolpartiklar som mekaniskt medförts under hällning av metall från elektrolysatorn); metall (järn, kisel) som passerar från råmaterial, kolmaterial och konstruktionselement i elektrolysatorn; gasformig - främst väte, som bildas i metallen till följd av elektrolytisk sönderdelning av vatten som kommer in i elektrolyten med råmaterial.
Förutom järn och kisel innehåller metallföroreningarna den största mängden gallium, zink, titan, mangan, natrium, vanadin, krom och koppar. Innehållet i dessa och vissa andra metalliska spårelement i elektrolytiskt aluminium anges nedan,%:
Den viktigaste källan för metalliska föroreningar i aluminium är aluminiumoxid, som beroende på typen av råmaterial kan innehålla gallium, zink, kalium, fosfor, svavel, vanadin, titan och krom. Kolmaterial (anodmassa, kalcinerade anoder, katodprodukter) tjänar som en källa till sådana mikroföroreningar som exempelvis vanadin, titan, mangan, zink.
Genom elektrolys av kryolit-aluminiumoxidsmälter, förutsatt att rena råmaterial används (främst aluminiumoxid och kolmaterial), är det möjligt att erhålla råaluminium av klass A85 och A8 (99,85 och 99,80%). Den största andelen metall av dessa kvaliteter (60-70% av den totala effekten) erhålls på elektrolysatorer med bakade anoder, liksom på elektrolysatorer med sidoströmförsörjning (upp till 70% av den totala produktionen). På elektrolysatorer med självbakande anoder och toppströmkabel är produktionen av råkvalitet A8-aluminium låg (1-3%), och kvaliteten A85-metall kan inte erhållas på grund av betydande föroreningar av järn som kommer in i aluminium från icke-råa källor (anodstift, gjutjärnssektioner av gassamlare , teknologiskt verktyg, katodmontering).
Det smälta primära aluminiumet, extraherat från de elektrolytiska cellerna med hjälp av en vakuumskopa, kommer in i gjuteriet för raffinering från icke-metalliska föroreningar och gasföroreningar och vidare bearbetning till kommersiella produkter (göt, cylindriska och plana göt, trådstav etc.). Före gjutning hålls det råa aluminiumet i ett smält tillstånd i elektriska resistensugnar (blandare) eller i gasreflekta ugnar. I dessa ugnar utförs inte bara rationell satsning av partier av flytande aluminium i olika kompositioner, utan också delvis rengöras från icke-metalliska inneslutningar, oxidfilmer och natrium.
Aluminium hälls från blandaren i göt med användning av gjutmaskiner av transporttyp; cylindriska och plana göt tillverkas med metoden för semikontinuerlig gjutning, och för att erhålla trådstav används speciella kombinerade gjut- och valsenheter.
I hushålls aluminiumsmältverk utsätts aluminiumet som kommer från blandaren till gjutmaskinens gjutform vid den gjutna götet för den enklaste formen för raffinering - filtrering av smältan genom ett glasfiber med maskstorlekar från 0,6 × 0,6 till 1,7 × 1,7 mm. Med denna metod kan du rengöra aluminium endast från mycket grova oxidinklusioner; en mer perfekt metod för att filtrera smältan genom glasfiber i uppströms. Med denna metod för filtrering fångas inte partiklar av oxidinklusioner, som kolliderar med rutnätet, av smältflödet, utan deponeras i botten av gjuttråget.
För samtidig rening av aluminium, både från icke-metalliska föroreningar och från väte, används filtreringsmetoden genom ett flödesfilter i kombination med kväverening. Som flöde kan du använda den sura elektrolyten i aluminiumelektrolysceller. Som ett resultat av sådan rengöring reduceras väteinnehållet i aluminium från 0,22 till 0,16 cm ^ per 100 g metall.
I det primära aluminium som används för produktion av Al-Mg-legeringar bör natriumhalten inte överstiga 0,001%. Detta beror på det faktum att närvaron av natrium i dessa legeringar försämrar de mekaniska och andra operationella egenskaperna hos produkter som används i ett antal sektorer i den nationella ekonomin.
Den mest effektiva metoden för att samtidigt raffinera aluminium från natrium, väte och icke-metalliska föroreningar är att rena den smälta metallen med en gasblandning av kväve med 2-10% klor, infört i smältan i form av små bubblor med hjälp av speciella anordningar. Denna raffineringsmetod gör det möjligt att reducera natriumhalten i aluminium till 0,0003-0,001% med en gasblandning flöde från 0,8 till 1,5 m 3 / t metall.
Elförbrukningen för produktion av 1 ton säljbar aluminium från råmetall vid användning av elektriska ugnar är 150-200 kWh; oåterkalleliga metallförluster vid gjuteriet är lika med 1,5-5% beroende på typen av försäljningsbara produkter.
Få aluminium med hög renhet
För att erhålla hög renhet aluminium (kvalitet A995-A95) förfinas primärt aluminium av teknisk renhet elektrolytiskt. Detta gör det möjligt att minska halten metalliska och gasformiga föroreningar i aluminium och därigenom avsevärt öka dess elektriska ledningsförmåga, duktilitet, reflektionsförmåga och korrosionsbeständighet.
Elektrolytisk raffinering av aluminium utförs genom elektrolys av smälta salter med en treskiktsmetod. Kärnan i metoden är som följer. I raffineringscellen finns tre smälta skikt. Den nedre, tyngsta, ligger på den ledande härden och fungerar som anoden; Det kallas anodlegeringen och är en legering av raffinerat aluminium med koppar, som införs för att göra skiktet tyngre. Mittskiktet är smält elektrolyt; dess densitet är mindre än anodlegeringens densitet och högre än densiteten av rent raffinerat (katod) aluminium beläget ovanför elektrolyten (övre, tredje vätskeskiktet).
Under anodisk upplösning är alla föroreningar mer elektropositiva än aluminium (Fe, Si, Ti, Cu, etc.) och förblir i den anodiska legeringen utan att passera in i elektrolyten. Endast aluminium upplöses anodiskt, vilket i form av Al 3+-joner passerar in i elektrolyten: Al– 3 e → Al 3+.
Under elektrolys överförs aluminiumjoner till katoden, på vilken de släpps ut: Al 3+ + 3 e → Al. Som ett resultat ackumuleras ett skikt av smält raffinerat aluminium vid katoden.
Om föroreningar som är mer elektronegativa än aluminium (till exempel Ba, Na, Mg, Ca) finns i anodlegeringen kan de elektrokemiskt lösa upp tillsammans med aluminium på anoden och passera in i elektrolyten i form av joner. Eftersom innehållet av elektronegativa föroreningar i det råa aluminiumet är litet, ackumuleras de inte i en märkbar mängd i elektrolyten. Utladdningen av dessa joner vid katoden sker praktiskt taget inte, eftersom deras elektrodpotential är elektronegativ än aluminium.
Som elektrolyt i elektrolytisk raffinering av aluminium i Sovjetunionen och i de flesta länder används en fluoridkloridelektrolyt, vars sammansättning är 55-60% BaCl2, 35-40% AlF 4 + NaF och 0-4% NaCl. Det molförhållandet NaF: AlF3 uppbär 1,5-2,0; smältpunkt för elektrolyt 720-730 ° C; temperaturen för elektrolysprocessen är cirka 800 ° C; elektrolytens densitet är 2,7 g / cm ^.
Anodlegeringen framställs av primärt aluminium och ren koppar (99,90-99,95% Cu), som införs i metallen i en mängd av 30-40%. Densiteten för den flytande anodlegeringen i denna komposition är 3-3,5 g / cm ^; densiteten för rent smält katodiskt aluminium är 2,3 g / cm ^. Med detta täthetsförhållande skapas de villkor som är nödvändiga för en bra separering av de tre smälta skikten.
I det kvartära Al-Cu-Fe-Si-systemet, till vilket anodlegeringen tillhör, bildas en eutektikum med en smältpunkt av 520 ° C. Kylning av anodlegeringen som innehåller föroreningar av järn och kisel i mängder högre än eutektiska koncentrationer, är det möjligt att separera järn och kisel i den fasta fasen i form av intermetalliska föreningar FeSiAl 5 och Cu 2 FeAl 7. Eftersom temperaturen på anodlegeringen i fickorna på elektrolysatorn är 30-40 ° C lägre än temperaturen på anodlegeringen i badets arbetsutrymme, frigörs fast intermetallisk utfällning i dem (eftersom järn och kisel ackumuleras i anodlegeringen). Genom att regelbundet ta bort dessa avlagringar, rengör de anodlegeringen (utan att uppdatera den) från föroreningar av järn och kisel. Eftersom gallium koncentreras i anodlegeringen kan fällningar som extraheras från elektrolysatorn (30-40 kg per 1 ton aluminium) tjäna som en källa till denna metall.
För elektrolytisk raffinering används elektrolysatorer, som i konstruktion liknar elektrolysatorer med bakade anoder för elektrolytisk produktion av primärt aluminium, men har en annan polförbindelse: härden fungerar som anoden och den övre raden av elektroder som katod. Moderna elektrolysatorer för elektrolytisk raffinering av aluminium är konstruerade för strömmar upp till 75 kA.
Nedan visas de viktigaste tekniska och ekonomiska indikatorerna för elektrolysatorer för 1979 som uppnåtts av inhemska företag (1, 2, 3).
Den elektrokemiska strömeffektiviteten beräknad av metallen hälld från elektrolysatorn är 97-98%. Den verkliga strömeffektiviteten, beräknad med mängden salbar metall, är 92-96%.
| Strömstyrka, kA | 23,5 | 62,9 | 69,8* |
| Medelspänning, V | 5,43 | 5,68 | 5,69 |
| Nuvarande produktion,% | 95,7 | 93,0 | 92,7 |
| DC-effektförbrukning, kW ּ h / t | 17 370 | 18 700 | 19 830 |
| Total växelström, kW ּ h / t | 18 670 | 19 590 | 20 780 |
| Nivåer, cm | |||
| katodaluminium | 16,6 | 12,9 | 14,6 |
| elektrolyt | 13,3 | 11,6 | 14,2 |
| anodlegering | 40,1 | 29,5 | 30,0 |
| Förbrukningsförhållanden, kg / t: | |||
| bariumklorid | 40,5 | 41,5 | 27,0 |
| kryolit | 27,7 | 21,0 | 16,5 |
| aluminiumfluorid | 6,7 | 13,1 | 3,8 |
| natriumklorid | 1,0 | 4,8 | - |
| rå aluminium | 1020 | 1028 | 1032 |
| grafit | 11,9 | 11,5 | 16,6 |
| koppar | 9,8 | 15,5 | 16,4 |
| Aluminiumproduktion med hög renhet,% kvaliteter: | |||
| A995 | 47,8** | 3,5 | 2,1 |
| A99 | 30,4 | 67,1 | 54,2 |
| A97 | 8,3 | 21,5 | 43,7 |
| A95 | 10,4 | 7,9 | - |
| under A95 | 3,1 | - | - |
* Hög renhet i aluminiumproduktionshastigheter. ** Betyg för elektrolysatorer utan expansion. |
|||
Den viktigaste faktorn som minskar strömeffektiviteten, förutom direktströmförluster till urladdningen av mer elektronegativa joner, metallförluster på grund av dess oxidation och mekaniska förluster av aluminium, är driften av elektrolysatorer med frisläppande av icke-sorterad metall, som återgår tillbaka till anodlegeringen för efterföljande raffinering. Dessa perioder av cellernas drift sker under uppstart av celler och kränkningar av den tekniska regimen.
Elektrolytisk raffinering av aluminium är en mycket energiintensiv produktion. Elektrisk energiförbrukning i växelström, inklusive energin som används för beredningen av elektrolyt- och anodlegeringen, driften av ventilationsanordningar och fordon samt förlusten av att omvandla växelström till likström, är 18,5-21,0 tusen kWh per 1 ton aluminium. Energieffektiviteten för raffinering av elektrolytiska celler överstiger inte 5-7%, dvs 93-95% av energin förbrukas i form av värmeförlust genererad huvudsakligen i elektrolytlagret (cirka 80-85% av den totala värmeinmatningen). Därför är de viktigaste sätten att ytterligare minska den specifika energiförbrukningen för elektrolytisk raffinering av aluminium att förbättra den termiska isoleringen av elektrolysatorn (särskilt den övre delen av strukturen) och minska elektrolytskiktet (minska interelektrodavståndet).
Renheten av aluminium, förfinad enligt treskiktsmetoden, 99.995%; det bestäms av skillnaden med fem huvudsakliga föroreningar - järn, kisel, koppar, zink och titan. Mängden metall som produceras av detta märke kan uppgå till 45-48% av den totala produktionen (utan utvidgning med lägre kvaliteter).
Det bör emellertid noteras att i elektrolytiskt raffinerat aluminium ingår föroreningar av andra metaller i mindre mängder, vilket minskar den absoluta renheten för sådant aluminium. Radioaktiv analys möjliggör upptäckt av upp till 30 föroreningar i elektrolytiskt raffinerat aluminium, vars totala innehåll är cirka 60 º 10–4%. Därför är renheten av raffinerat aluminium i skillnad med dessa föroreningar 99.994%.
Förutom de föroreningar som tillhandahålls av GOST (se tabell 1.1), innehåller den vanligaste kvaliteten (A99) elektrolytiskt raffinerat aluminium,%: Cr 0,00016; V 0,0001; Ga 0,0006; Pb 0,002; Sn 0,00005; Ca 0,002-0,003; Na 0,001-0,008; Mn 0,001-0,007; Mg 0,001-0,007; som<0,0001; Sb<0,00002; Bi<0,00001; Cd<0,000001; S 0,0007.
En av källorna till katodaluminiumföroreningar är grafit-nedledare som innehåller järn och kiseloxid och ständigt i kontakt med raffinerat aluminium. Om strömmen matas direkt till katodaluminium med aluminiumstänger och ett mycket rent grafitverktyg används, är det möjligt att erhålla en metall med en renhet av 99,999% efter skillnad med de bestämda föroreningarna (Fe, Si, Cu, Zn och Ti). En sådan metall innehåller ett genomsnitt,%: Si 0,0002; Fe 0,00032; Cu 0,0002; Zn 0,0002 och Ti 0,00005. På grund av tekniska svårigheter har denna metod för tillförsel av ström ännu inte hittat någon bred industriell tillämpning.
Produktion av aluminium med hög renhet
Aluminium med hög renhet (kvalitet A999) kan erhållas på tre sätt: smältning av zoner, destillation genom subhalider och elektrolys av aluminiumorganiska föreningar. Av ovanstående metoder för framställning av aluminium med hög renhet erhölls en praktisk metod för zonsmältning i USSR.
Principen för zonsmältning är den multipla passagen av den smälta zonen längs en aluminiumgöt. Med värdet på distributionskoefficienter K \u003d C TV / S w (var C tv är koncentrationen av föroreningar i fast och C g - i vätskefasen), som till stor del bestämmer effektiviteten för rening från föroreningar, kan dessa föroreningar delas in i tre grupper. Den första gruppen inkluderar föroreningar som sänker smältpunkten för aluminium, de har K<1 under zonsmältning koncentreras de i den smälta zonen och överförs genom den till den sista delen av götet. Dessa föroreningar inkluderar Ga, Sn, Be, Sb, Ca, Th, Fe, Co, Ni, Ce, Te, Ba, Pt, Au, Bi, Pb, Cd, In, Na, Mg, Cu, Si, Ge , Zn. Den andra gruppen inkluderar föroreningar som ökar smältpunkten för aluminium; de kännetecknas K\u003e 1 och under zonsmältning koncentreras de i den fasta (initiala) delen av göt. Dessa föroreningar inkluderar Nb, Ta, Cr, Ti, Mo, V. Den tredje gruppen inkluderar föroreningar med en distributionskoefficient mycket nära enhet (Mn, Sc). Dessa föroreningar avlägsnas praktiskt taget inte under zonsmältning av aluminium.
Aluminiumet som är avsett för zonsmältning utsätts för viss beredning, vilket består i filtrering, avgasning och etsning. Filtrering är nödvändig för att ta bort från aluminium en eldfast och stark oxidfilm dispergerad i metallen. Den aluminiumoxid som finns i smält aluminium kan bilda kristallisationscentra när den stelnar, vilket leder till bildandet av en polykristallin göt och en kränkning av omfördelningen av föroreningar mellan den fasta metallen och den smälta zonen. Aluminium filtreras i vakuum (återstående tryck 0,1-0,4 Pa) genom en öppning i botten av en grafitdigel med en diameter av 1,5-2 mm. Preliminär avgasning av aluminium före zonsmältning (även uppvärmning i vakuum) utförs för att förhindra metallstänk under zonsmältning i händelse av en process i högvakuum. Det sista steget i beredningen av aluminium för zonsmältning är etsning av dess yta med en blandning av koncentrerad saltsyra och salpetersyra.
Eftersom aluminium har betydande kemisk aktivitet och särskilt ren grafit används som huvudmaterial för behållare (båtar) utförs zonsmältning av aluminium i vakuum eller i en inert gasatmosfär (argon, helium).
Zonsmältning i vakuum säkerställer hög renhet av aluminium på grund av förångningen av vissa föroreningar under vakuum (magnesium, zink, kadmium, alkali och jordalkalimetaller), och även kontaminering av den rena metallen med föroreningar som ett resultat av användningen av skyddande inerta gaser elimineras. Zonsmältning av aluminium i vakuum kan utföras under kontinuerlig pumpning av ett kvartsrör, där en grafitbåt med en aluminiumgjut placeras, såväl som i förseglade kvartsampuller, från vilken luft preliminärt pumpas till ett resttryck på cirka 1 10-3 Pa.
För att skapa en smält zon på en aluminiumgöt under sin zonsmältning kan värme appliceras med hjälp av små resistensugnar eller högfrekvensströmmar. För kraftförsörjning av elektriska motståndsugnar krävs inte komplex utrustning, ugnarna är enkla att använda. Den enda nackdelen med denna uppvärmningsmetod är det lilla tvärsnittet av göt av renat aluminium.
Induktionsvärme med högfrekventa strömmar är ett idealiskt sätt att skapa en smält zon på en göt under zonsmältning. Metoden för högfrekvensuppvärmning (förutom att tillåta zonsmältning av göt av stora tvärsnitt) möjliggör den viktiga fördelen att den smälta metallen kontinuerligt blandas i zonen; detta underlättar diffusionen av föroreningsatomer från kristallisationsfronten djupt in i smältan.
För första gången behärskades industriell produktion av aluminium med hög renhet genom smältning av zoner vid Volkhovs aluminiumverk 1965 med UZPI-3-installationen utvecklad av DU. Denna installation var utrustad med fyra kvartsretorter med induktionsuppvärmning, medan induktorerna var rörliga och behållarna med metall var stationära. Produktiviteten var 20 kg metall per rengöringscykel. Därefter skapades en mer högpresterande allmetallinstallation UZPI-4 och sattes i kommersiell drift 1972 på Volkhov aluminiumverk.
Effektiviteten av aluminiumrening under zonsmältning kan kännetecknas av följande data. Om den totala halten av föroreningar i elektrolytiskt raffinerat aluminium är (30–60) ּ 10–4%, minskar den efter zonsmältning till (2,8–3,2) ּ 10–4%, dvs 15–20 gånger. Detta motsvarar den kvarvarande elektriska resistiviteten hos aluminium ρ ○ (vid en flytande heliumtemperatur på 4,2 K) respektive (20 ÷ 40) 10 10–10 och (1,8 ÷ 2,1) - 10 –10 eller en renhet av 99,997-99,994 och 99,9997%. I tabellen. 1.4 (se nedan) visar data från radioaktiv analys av innehållet i vissa föroreningar i zonrenat aluminium och raffinerat elektrolytiskt. Dessa data indikerar en stark minskning av innehållet i de flesta föroreningar, även om föroreningar såsom mangan och skandium praktiskt taget inte avlägsnas under zonsmältning.
Under de senaste åren har VAMI utvecklat och testat under industriella förhållanden en teknik för att producera aluminium med en renhet på 99.9999% genom smältning av kaskadzoner. Kärnan i metoden för smältning av kaskadzoner är att rening av källaluminium med en renhet av A999 utförs genom sekventiell upprepning av zonremsans cykler (kaskader). I detta fall är utgångsmaterialet för varje efterföljande kaskad den mittersta, renaste delen av göt som erhållits som ett resultat av den tidigare rengöringscykeln.
TABELL 1.4
| förorening | Källaluminium (elektrolytiskt raffinerat 99.993-99.994%) | Zonsmältande aluminium | |
| grafit, vakuum | alund air | ||
| koppar | 1,9 | 0,02 | 0,08 |
| arsenik | 0,15 | 0,0015 | 0,001 |
| antimon | 1,2 | 0,03 | 0,02 |
| Uranus | 0,002 | - | - |
| järn | 3 | ≤0,2 | ≤0,3 |
| gallium | 0,3 | 0,02 | 0,05 |
| mangan | 0,2-0,3 | 0,1-0,2 | 0,15 |
| skandium | 0,4-0,5 | 0,4-0,5 | 0,4-0,5 |
| yttrium | 0,02-0,04 | <<0,001 | <<0,001 |
| lutetium | 0,002-0,004 | <<0,0001 | <<0,0001 |
| holmium | 0,005-0,01 | <<0,0001 | <<0,0001 |
| gadolinium | 0,02-0,04 | <<0,01 | <<0,01 |
| terbium | 0,003-0,006 | <<0,001 | <<0,001 |
| samarium | 0,05-0,01 | <<0,0001 | <<0,0001 |
| neodym | 0,1-0,2 | <<0,01 | <<0,01 |
| praseodym | 0,05-0,1 | <<0,001 | <<0,001 |
| cerium | 0,3-0,6 | <<0,01 | <<0,01 |
| lantan | 0,01 | <<0,001 | <<0,001 |
| nickel | 2,3 | - | <1 |
| kadmium | 3,5 | <<0,01 | 0,02-0,07 |
| zink | 20 | <<0,05 | 1 |
| kobolt | 0,01 | <<0,01 | <<0,01 |
| natrium | 1-2 | <0,2 | <0,2 |
| kalium | 0,05 | 0,01 | 0,01 |
| barium | 6 | - | - |
| klor | 0,01 | <0,01 | <0,01 |
| fosfor | 3 | 0,04 | - |
| svavel | 15 | 0,5-1,5 | - |
| kol | 1-2 | - | 1-2 |
| Anm. Mängderna tellur, vismut, silver, molybden, krom, zirkonium, kalcium, strontium, rubidium, cerium, indium, selen och kvicksilver i aluminium efter zonsmältning är lägre än känsligheten för den radioaktiva analysen. | |||
I tabellen. 1.5 (se nedan) visar resultaten av massspektralanalys och mätning R 293 K / R 4,2 K aluminium erhållet genom smältning av kaskadzon. Från ovanstående data kan man dra slutsatsen att renheten för sådant aluminium, bestämt av skillnaden med tio basiska föroreningar (Si, Fe, Mg, Mn, Ti, Cu, Cr, Zn, Na och V), är\u003e 99,9999%. Denna slutsats bekräftas indirekt av värdet R 293 K / R 4,2 K, som i alla prover var\u003e 30 10 3.
För att få en metall med en renhet av 99.9999% räcker det att utföra två kaskader av zonsmältning (se tabell 1.5). En ytterligare ökning av antalet kaskader ökar inte renheten för aluminium, även om det ökar det totala metallutbytet med en renhet på 99.9999%.
En annan möjlig process för att erhålla aluminium med hög renhet är dess destillation genom subhalider, särskilt genom aluminiumsubfluorid.
Det mättade ångtrycket av aluminiummetall är inte tillräckligt högt för att direkt destilleras med praktiskt acceptabla hastigheter. Emellertid, när aluminium värms upp i vakuum (vid 1000-1050 ° C) med AlF 3, bildar aluminium en flyktig AlF-subfluorid, som destilleras till en kall zon (800 ° C), där den åter sönderdelas (disproportionerliga) med frisättningen av rent aluminium:
Möjligheten för djup rening av aluminium från föroreningar beror huvudsakligen på det faktum att sannolikheten för bildandet av aluminiumunderföreningar är mycket högre än sannolikheten för bildandet av underföreningar av föroreningen.
TABELL 1.5
RESULTAT AV MASS SPEKTRAL ANALYS OCH MÄTNINGAR R 293 K / R 4.2 K ALUMINIUM CASCADE ZONE SMELT.
| Antalet kaskader | Innehållet i föroreningar, × 10-4% | ||||||
| si | fe | mg | mn | Ti | beloppet | ||
| förälder | 18,3 | 0,210 | <0,103 | 0,89 | <0,061 | 0,069 | 1,544 |
| A999 | |||||||
| 2 | 36,5 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 38,0 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 39,5 | 0,073 | <0,103 | 0,045 | <0,061 | 0,07 | 0,563 |
| 3 | 32,0 | 0,204 | <0,103 | 0,006 | <0,061 | 0,017 | 0,502 |
| 3 | 30,0 | 0,073 | 0,100 | 0,006 | 0,020 | 0,07 | 0,480 |
| 3 | 32,0 | 0,052 | 0,100 | 0,006 | 0,061 | 0,07 | 0,500 |
| 4 | 40,0 | <0,021 | <0,103 | 0,006 | 0,061 | 0,07 | 0,472 |
| 4 | 30,5 | 0,031 | 0,100 | 0,006 | 0,061 | 0,07 | 0,479 |
| 5 | 34,0 | 0,104 | <0,060 | 0,006 | 0,061 | 0,017 | 0,459 |
| Anmärkningar: 1. Mängden föroreningar anges med beaktande av andra föroreningar, vars innehåll i alla prover var × 10-4%:<0,071 Cu; <0,038 Cr; 0,048 Zn; 0,017 Na; 0,037 V. 2. При подсчете суммы примесей принимали их максимальное значение, равное пределу чувствительности анализа, например <0,061 считали как 0,061. | |||||||
Innehållet av föroreningar i aluminium destillerat genom subfluorid är omvänt relaterat till massan på de erhållna götarna. I göt som väger 1,5-1,7 kg är den totala halten av föroreningar (Si, Fe, Cu, Mg) 11 4 10–4%, och gashalten är 0,007 cm 3/100 g. Den specifika restmotståndet (ρ ○) vid flytande heliumtemperatur för en sådan metall är (1,7 ÷ 2,0) 10 - 10 Ohm cm. Destillationen av aluminium genom subfluorid har flera nackdelar (relativt liten produktivitet, otillräcklig djup rening från magnesium, etc.), därför har metoden inte fått industriell utveckling.
Metoder har också utvecklats för framställning av aluminium med hög renhet genom elektrolys av komplexa organoaluminiumföreningar, som skiljer sig i elektrolytkompositionen. Till exempel används i Tyskland ett förfarande för elektrolys av en 50% -ig lösning av NaF ^ Al (C2H5) 3 i toluen. Förädling utförs vid 100 ° C, spänningen på cellen 1,0-1,5 V och strömtätheten 0,3-0,5 A / DM 2 med hjälp av aluminiumelektroder. Katodströmutgång 99%. Elektrokemisk raffinering i organoaluminiumelektrolyter reducerar avsevärt innehållet av mangan och skandium, som praktiskt taget inte avlägsnas under zonrengöring. Nackdelarna med denna metod är dess låga produktivitet och höga brandrisk.
För en djupare rening av aluminium och erhållande av en metall med en renhet av 99.99999% eller mer, kan en kombination av ovanstående metoder användas: elektrolys av organoaluminiumföreningar eller sublimering med subfluorid följt av zonsmältning av det erhållna aluminiumet. Exempelvis genom multipelzonsrening av aluminium erhållet genom elektrolys av organoaluminiumföreningar är det möjligt att erhålla en metall med hög renhet med ett föroreningsinnehåll på 10–9%: Fe 50; si<500; Cu 10; Mg 30; Mn5; Ti <500; Cr 20; Zn <50; Co <1; Ag <5; Sb <1 и Se 3.
ansökan
Kombinationen av fysikaliska, mekaniska och kemiska egenskaper hos aluminium avgör dess utbredda användning inom nästan alla tekniska områden, särskilt i form av legeringar med andra metaller. Inom elektroteknik ersätter aluminium framgångsrikt koppar, speciellt vid produktion av fasta ledare, till exempel i luftledningar, högspänningskablar, kopplingsbussar, transformatorer (den elektriska ledningsförmågan hos aluminium når 65,5% av den elektriska ledningsförmågan hos koppar, och den är mer än tre gånger lättare än koppar; med ett tvärsnitt som ger samma konduktivitet är massan av aluminiumtrådar hälften av koppar). Ultrapure-aluminium används vid tillverkning av elektriska kondensatorer och likriktare, vars effekt baseras på förmågan hos en aluminiumoxidfilm att överföra elektrisk ström i endast en riktning. Ultren rent aluminium, renat genom zonsmältning, används för syntes av halvledarföreningar av typ A III B V som används vid tillverkning av halvledaranordningar. Ren aluminium används för tillverkning av olika slags reflektionsspeglar. Aluminium med hög renhet används för att skydda metallytor mot atmosfärisk korrosion (beklädnad, aluminiumfärg). Med ett relativt lågt neutronabsorptionstvärsnitt används aluminium som strukturellt material i kärnreaktorer.
I aluminiumkapslar med stor kapacitet lagras och transporteras flytande gaser (metan, syre, väte, etc.), salpetersyra och ättiksyra, rent vatten, väteperoxid och ätliga oljor. Aluminium används allmänt i utrustning och apparater inom livsmedelsindustrin, för förpackning av livsmedelsprodukter (i form av folie), för produktion av olika typer av hushållsprodukter. Aluminiumförbrukningen har ökat kraftigt för inredning av byggnader, arkitektur, transport och idrottsanläggningar.
I metallurgi är aluminium (utöver legeringar baserat på det) en av de vanligaste legeringsadditiverna i legeringar baserade på Cu, Mg, Ti, Ni, Zn och Fe. Aluminium används också för avoxidering av stål innan det hälls i formen, liksom i processerna för framställning av vissa metaller med aluminiuminotermetoden. Baserat på aluminium skapades SAP (sintrad aluminiumpulver) genom pulvermetallurgi, som har hög värmebeständighet vid temperaturer över 300 ° C.
Aluminium används vid tillverkning av sprängämnen (ammonal, aluminiumoxid). Olika aluminiumföreningar används ofta.
Produktion och konsumtion av aluminium växer ständigt, vilket väsentligt överträffar produktionen av stål, koppar, bly, zink.
DIN (DeutschIndustrienorm) - Tysklands industriella standard.
Den tekniska processen för aluminiumproduktion omfattar tre huvudstadier:
1. Skapandet av aluminiumoxid från aluminiummalm;
2. Tillverkning av aluminium från aluminiumoxid;
3. Förädling av aluminium.
Och samtidigt är användningen av sådan utrustning nödvändig:
utrustning för ett centralt aluminiumoxidfördelningssystem;
elektrolysör;
katod samlingsstång;
torrgasreningsverk;
montering, tekniska kranar och gjuterier;
sug enheter;
gjuteriutrustning;
utrustning för anodmonteringsbutiken;
metallstrukturer i produktionsbyggnader.
Skapandet av aluminiumoxid från malm - stadiet i aluminiumproduktionen
Aluminiumoxid kan erhållas med tre metoder: syra, alkaliskt och elektrolytiskt. Den mest populära är den alkaliska metoden. Kärnan i metoden är att aluminiumlösningar börjar sönderdelas mycket snabbt med införandet av aluminiumhydroxid, och lösningen som återstår från sönderdelning efter indunstning med kraftig omröring vid en temperatur av 170 ° C kan åter lösa aluminiumoxiden som finns i bauxit. Denna metod har följande huvudstadier:
1. Beredning av bauxit, som involverar krossning och slipning i specialbruk. Kaustisk alkali, bauxit och lite kalk skickas till bruken. Massan, som visade sig, skickas för lakning.
2. Utlakning av bauxit innebär dess kemiska sönderdelning från en förening med en vattenhaltig lösning av alkali. I detta fall passerar aluminiumoxidhydrater, när de kombineras med alkali, till lösningen i form av natriumaluminat, och kiseldioxiden innehållande i bauxit, ansluten med alkalin, passerar in i lösningen i form av natriumsilikat. I en lösning bildar dessa föreningar: natriumaluminat och natriumsilikat olösligt natriumaluminosilikat. Oxider av järn och titan passerar in i denna rest, vilket ger återstoden en röd nyans. En sådan rest är röd lera. När upplösningen av det erhållna natriumaluminatet är avslutat utspädes det med en vattenlösning av alkali medan temperaturen sänks till 100 ° C.
3. Separation av röd lera och aluminatlösning från varandra beror på tvättning i förtjockningsmedel. Sedan sedimenterar den röda leran, och den återstående aluminatlösningen filtreras.
4. Nedbrytning av aluminatlösning. Det filtreras och skickas till stora behållare med blandare. Från denna lösning frisätter kylning till 60 ° C och omrörning konstant aluminiumhydroxid. På grund av det faktum att processen är ojämn och mycket långsam, och tillväxten av kristaller av aluminiumhydroxid är mycket viktig vid vidare bearbetning, lägger sönderdelare fortfarande mycket fast hydroxid till dessa behållare med blandare.
5. Produktionen av aluminiumhydroxid utförs i vakuumfilter och hydrocykloner. Mest hydroxid som utsädesmaterial återgår till nedbrytningsproceduren. Efter vattentvätt skickas återstoden för kalcinering; och filtratet återgår också till processen.
6. Uttorkning av aluminiumhydroxid - det sista stadiet av aluminiumoxidproduktionen. Det sker i rörformiga, ständigt roterande ugnar. Rå aluminiumhydroxid, när den passeras genom ugnen, torkas och torkas fullständigt.
Tillverkningen av aluminium från aluminiumoxid i produktionen sker också i flera steg.
1. Elektrolysen av aluminiumoxid sker vid en temperatur i cellen - 970 ° C. Cellen har ett bad fodrat med kolblock, till vilka en elektrisk ström är ansluten. Det flytande aluminium som släpps upp samlas på en kolbas och därifrån pumpas det regelbundet ut. Kolanoder nedsänks i elektrolyten ovanifrån och brinner i en atmosfär av syre, som frigörs från aluminiumoxid, och kolmonoxid eller dioxid frigörs.
2. Elektrolysen av aluminiumklorid utförs genom omvandling av aluminiumoxid i reaktionskärlet till aluminiumklorid. Sedan i ett isolerat bad är elektrolys av aluminiumklorid. Klor, som släpps i detta fall, sugs bort och skickas för återvinning. Och aluminium fälls ut vid katoden.
3. Minskning av manganaluminiumklorid medan aluminium frigörs. På grund av kontrollerad kondensation frigörs föroreningar associerade med klor från flödet av manganklorid. När klor frisätts omvandlas manganklorid till manganoxid, som sedan reduceras till ett tillstånd av mangan som är återvinningsbart.
Aluminiumraffinering i aluminiumproduktion
Förädling av elektrolys med sönderdelning av vattenhaltiga saltlösningar för aluminium är inte möjligt. Eftersom reningsgraden av industriellt aluminium, som erhålls genom elektrolys av en kryolit-aluminiumoxidsmälta, kommer att vara otillräcklig för vissa ändamål, är aluminium ännu renare från metall och industriellt aluminiumavfall på grund av raffinering. Den vanligaste raffineringsmetoden är treskiktselektrolys.
Aluminium används för tillverkning av explosiva ämnen (alumotol, ammonal). En mängd olika aluminiumföreningar används. Produktion och konsumtion av aluminium växer ständigt, mycket snabbare än produktion av koppar, stål, zink och bly.
För att få koppar används kopparmalm, såväl som kopparavfall och dess legeringar. Malmen innehåller 1 - 6% koppar. Malm som innehåller mindre än 0,5% koppar bearbetas inte eftersom det vid den nuvarande teknologinivån är att olja att utvinna koppar ur det är olönsamt.
I malmer är koppar i form av svavelföreningar (CuFeS 2 - kalkopyrit, Cu 2 S - kalkosin, CuS - kovelin), oxider (CuO, CuO) och bikarbonater
Gangmalm består av pyrit (FeS 2), kvarts (Si02), olika föreningar som innehåller Al203, MgO, CaO och järnoxider.
Malmer innehåller ibland betydande mängder av andra metaller (zink, guld, silver och andra).
Det finns två metoder för att producera koppar från malmer:
- hydro;
- pyrometallurgisk.
Den hydrometallurgiska hittade inte sin breda tillämpning på grund av oförmågan att utvinna ädelmetaller tillsammans med koppar.
Den pyrometallurgiska metoden är lämplig för bearbetning av alla malmer och inkluderar följande operationer:
- beredning av malmer för smältning;
- matt smältning;
- matt omvandling;
- kopparraffinering.
Förberedelse av malm för smältning
Beredningen av malmer består i berikning och rostning. Anrikningen av kopparmalm utförs genom flotation. Resultatet är ett kopparkoncentrat som innehåller upp till 35% koppar och upp till 50% svavel. Koncentrat avfyras vanligen i ugnar med fluidiserad bädd för att reducera svavelhalten till optimala värden. Under bränningen oxideras svavel vid en temperatur av 750 - 800 ° C, en del av svavlet avlägsnas med gaser. Resultatet är en produkt som kallas cinder.
Smältning till matte
Matt smälts i reflekterande eller elektriska ugnar vid en temperatur av 1250 - 1300 ° C. Smältkoncentrat av kopparmalm kommer in i smältprocessen, under vilken uppvärmningen av reduktionsreaktionerna av kopparoxid och högre järnoxider fortsätter
6CuO + FeS \u003d 3Cu2O + FeO + SO 2
FeS + 3Fe3O4 + 5SiO2 \u003d 5 (2FeO · SiO2) + SO2
Som ett resultat av interaktion mellan Cu20 med FeS, bildas Cu2S genom reaktionen:
Cu2O + FeS \u003d Cu2S + FeO
Sulfider av koppar och järn, smälta samman, bildar matta och smälta silikater av järn, löser andra oxider, bildar slagg. Matt innehåller 15 - 55% Cu; 15 till 50% Fe; 20-30% S. Slag består huvudsakligen av SiO2, FeO, CaO, Al203.
Matt och slagg släpps när de ackumuleras genom speciella öppningar.
Matt konvertering
Matten omvandlas i kopparsmältverk (figur 44) genom att blåsa den med luft för att oxidera svavelhaltigt järn, överföra järn till slagg och isolera blisterkoppar.
Omvandlarna har en längd av 6 - 10 m och en ytterdiameter på 3 - 4 m. Den smälta matten hälls, smältprodukterna dräneras och gaserna avlägsnas genom en hals belägen mitt i omvandlarhöljet. För att rena matten tillförs tryckluft genom lanser belägna längs konverterarens generatrix. Ett hål är beläget i en av omvandlarens ändväggar genom vilka pneumatisk belastning av kvartsflöde utförs, vilket är nödvändigt för att ta bort järn i slaggen.
Spolningsprocessen genomförs under två perioder. Under den första perioden hälls matten in i omvandlaren och kvartsflöde tillförs. Under denna period inträffar sulfidoxidationsreaktioner.
Den resulterande järnoxiden interagerar med kvartsflöde och avlägsnas till slagg.
När slaggen ackumuleras dräneras den delvis och en ny del av den initiala mattan hälls in i omvandlaren, vilket bibehåller en viss nivå av matt i omvandlaren. Under den andra perioden interagerar kopparoxid med kopparsulfid och bildar metallisk koppar
Som ett resultat av rensningen erhålls således blisterkoppar innehållande 98,4 - 99,4% Cu. Den resulterande blisterkopparen hälls i platta formar på en bandgjutningsmaskin.
Magnesiumproduktionsteknik
Den huvudsakliga metoden för magnesiumproduktion är elektrolytisk. Elektrolytisk produktion av magnesium från vattenhaltiga lösningar är omöjlig, eftersom den elektrokemiska potentialen hos magnesium är mycket mer negativ än potentialen för utsläpp av vätejoner vid katoden. Därför utförs elektrolys av magnesium från dess smälta salter.
Huvudkomponenten i elektrolyten är magnesiumklorid MgCl2, och NaCl, CaCl2, KCl och små mängder NaF och CaF2 införs i den för att sänka smälttemperaturen för elektrolyten och öka dess elektriska konduktivitet.
De viktigaste råvarorna för magnesiumproduktion är karnallit (MgCl2 KCl 6H2O), magnesit (MgCO3), dolomit (CaCO3 MgCO3), bischofit (MgCl2 6H2O). Den största mängden magnesium erhålls från karnallit.
De viktigaste stadierna i magnesiumproduktionen:
1. Carnallite;
2. Berikning av karnallit;
3. Uttorkning av karnallit;
4. Elektrolytisk produktion av magnesium;
5. Raffinering av magnesium;
6. Magnesium.
Berikningen av karnallit är det första steget i dess bearbetning. Kärnan i anrikningsprocessen är att separera KCl och olösliga föroreningar genom att överföra MgCl2 och KCl till en vattenlösning. När den resulterande lösningen kyls i vakuumkristallisatorer fälls kristaller av konstgjord karnallit MgCl2 KCl 6H20, som separeras genom filtrering.
Carnallite är uttorkad i två steg. Det första steget utförs i rörformiga ugnar eller ugnar med fluidiserad bädd vid 550-600 ° C. Under verkan av värmen från uppvärmda gaser dehydratiseras karnallit och innehåller efter denna behandling 3-4% fukt.
Det andra dehydratiseringssteget utförs antingen genom att smälta karnalliten erhållen efter det första steget i elektriska ugnar, följt av sedimentering av magnesiumoxid eller genom klorering av karnallit i smält tillstånd.
Elektrolytisk produktion av magnesium. För detta ändamål används en elektrolysator, som är invändig fodrad med eldstenar. Anoderna är grafitplattor och katoderna är stålplattor belägna på båda sidorna av anoden.
För elektrolytisk sönderdelning av magnesiumklorid passeras en ström på 2,7-2,8 V genom elektrolyten.
Som ett resultat av elektrolytisk sönderdelning av magnesiumklorid bildas klorjoner, som rör sig till anoden och efter utmatning skapar klorbubblor som kommer ut från elektrolyten. Magnesiumjoner flyttas till katoden och släpps efter utmatning på ytan och bildar droppar flytande magnesium. Magnesium har en lägre densitet än elektrolyten, så den flyter till ytan i katodutrymmet, varifrån den periodvis avlägsnas med en vakuumskopa.
Under elektrolysen ökar koncentrationen av andra klorider i elektrolyten på grund av konsumtionen av MgCl2. Därför avlägsnas periodvis en del av den förbrukade elektrolyten från badet och i stället för den hälls MgCl2 eller karnallitsmälta. Som ett resultat av den partiella nedbrytningen av föroreningar bildas slam vid badets botten, som regelbundet avlägsnas från badet.
Raffinering av magnesium. I elektrolysbaden erhålls grovt magnesium, som innehåller 5% föroreningar: metalliska föroreningar (Fe, Na, K, Al, Ca) och icke-metallföroreningar (MgCl2, KCl, NaCl, CaCl2, MgO). Magnesium raffineras (förfinas) genom omsmältning med flöden.


