07.06.2019
Опис продукції алюміній. Технологічний процес виробництва алюмінію
Технологічний процесВиробництво алюмінію включає три основні етапи:
1. Створення глинозему з алюмінієвих руд;
2. Створення із глинозему алюмінію;
3. Процес рафінування алюмінію.
І при цьому потрібне використання такого обладнання:
обладнання для системи центральної роздачі глинозему;
електролізер;
катодна ошиновка;
установки сухого газоочищення;
монтажні, технологічні та ливарні крани;
аспіраційні установки;
обладнання ливарного цеху;
обладнання анодно-монтажного цеху;
металоконструкції виробничих корпусів
Створення глинозему з руд – етап виробництва алюмінію.
Глинозем можна отримати трьома методами: кислотним, лужним та електролітичним. Найпопулярнішим є лужний метод. Суть методу полягає в тому, що алюмінієві розчини дуже швидко починають розкладатися при введенні гідроксиду алюмінію, а розчин, що залишився від розкладання після випарювання при інтенсивному перемішуванні при температурі 170 °С, може знову розчинити глинозем, який міститься у бокситах. Цей метод має такі основні стадії:
1. Підготовка бокситу, яка має на увазі його дроблення та подрібнення у спеціальних млинах. До млина відправляють їдкий луг, боксит і трохи винищити. Пульпу, яка вийшла, направляють на вилуговування.
2. Вилужування бокситу має на увазі його хімічне розкладання від з'єднання з водним розчиномлуги. При цьому гідрати окису алюмінію при з'єднанні з лугом розчин переходять у формі алюмінію натрію, а кремнезем, який міститься в боксіті, з'єднуючись з лугом, в розчин переходить у формі силікату натрію. У розчині ці сполуки: алюмінат натрію та силікат натрію формують нерозчинний натрієвий алюмосилікат. У цей залишок переходять окисли заліза та титану, які надають залишку червоного відтінку. Такий залишок – це червоний шлам. Коли розчинення отриманого алюмінату натрію завершується, розводять його водним розчином лугу при зниженні температури до 100°С.
3. Відділення червоного шламу та алюмінатного розчину один від одного відбувається завдяки промиванню у згущувачах. Після чого червоний шлам осідає, а алюмінатний розчин, що залишився, фільтрують.
4. Розкладання алюмінатного розчину. Його фільтрують та відправляють у великі ємності з мішалками. З даного розчинупри охолодженні до 60°С і постійному перемішуванні виділяється гідроксид алюмінію. Через те, що процес протікає нерівномірно і дуже повільно, а зростання кристалів гідроксиду алюмінію дуже важливий при подальшій обробці, то в ці ємності з мішалками - декомпозери ще додають багато твердого гідроксиду.
5. Отримання гідроксиду алюмінію здійснюється у вакуум-фільтрах та гідроциклонах. Більшу частину гідроксиду як затравальний матеріал повертають до процедури декомпозиції. Після водного промивання залишок відправляється на кальцинацію; і фільтрат теж повертається у процес.
6. Зневоднення гідроксиду алюмінію - завершальна стадія виробництва глинозему. Вона проходить в трубчастих печах, що постійно обертаються. Сирий гідроксид алюмінію, коли проходить через піч, повністю висушується та зневоднюється.
Створення із глинозему алюмінію при виробництві також проходить у кілька етапів.
1. Електроліз окису алюмінію відбувається при температурі електролізері - 970°С. Електролізер має футеровану вуглецевими блоками ванну, до якої підключається електричний струм. Рідкий алюміній, що виділився, збирається на вугільній підставі, і звідти його регулярно відкачують. В електроліт зверху занурені вугільні аноди, що згоряють в атмосфері кисню, який виділяється з окису алюмінію, і при цьому виділяється окис або двоокис вуглецю.
2. Електроліз хлориду алюмінію здійснюється шляхом перетворення окису алюмінію в реакційній посудині на хлорид алюмінію. Після чого в ізольованій ванні здійснюється електроліз хлориду алюмінію. Хлор, який при цьому виділився, відсмоктується та спрямовується для вторинного використання. А алюміній випадає в осад на катоді.
3. Відновлення марганцем хлориду алюмінію, при цьому звільняється алюміній. За рахунок керованої конденсації виділяються забруднення, пов'язані з хлором, потоку хлориду марганцю. Коли відбувається звільнення хлору, хлорид марганцю перетворюється на окис марганцю, який потім відновлюється до стану марганцю, який придатний до вторинного використання.
Процес рафінування алюмінію під час виробництва алюмінію
Рафінуючий електроліз з розкладанням водяних сольових розчинів для алюмінію неможливий. Так як ступінь очищення промислового алюмінію, отриманий шляхом електролізу кріолітоглиноземного розплаву, для деяких цілей буде недостатня, то з відходів металу та промислового алюмінію завдяки рафінуванню отримують алюміній ще чистіший. Найпоширенішим методом рафінування є тришаровий електроліз.
Алюміній застосовується у виготовленні вибухових речовин (алюмотол, аммонал). Широко використовуються різноманітні сполуки алюмінію. Виробництво та споживання алюмінію постійно зростає, сильно випереджаючи за темпами зростання виробництво міді, сталі, цинку, свинцю.
Для отримання міді застосовують мідні руди, а також відходи міді та її сплави. У рудах міститься 1-6% міді. Руду, що містить менше 0,5% міді, не переробляють, тому що при сучасному рівні техніки вилучення з неї міді нерентабельне.
У рудах мідь знаходиться у вигляді сірчистих сполук (CuFeS 2 – халько-пірит, Cu 2 S – халькозин, CuS – ковелін), оксидів (CuO, CuO) та гідрокарбонатів
Порожня порода руд складається з піриту (FeS 2), кварцу (SiO 2), різних сполук, що містять Al 2 O 3 , MgO, CaO, і оксидів заліза.
У рудах іноді міститься значна кількість інших металів (цинк, золото, срібло та інші).
Відомі два способи отримання міді із руд:
- гідрометалургійний;
- пірометалургійний.
Гідрометалургійний не знайшов свого широкого застосування через неможливість витягувати попутно з міддю дорогоцінні метали.
Пірометалургійний спосіб придатний для переробки всіх руд і включає наступні операції:
- підготовка руд до плавки;
- плавлення на штейн;
- конвертування штейна;
- рафінування міді.
Підготовка руд до плавки
Підготовка руд полягає у проведенні збагачення та випалу. Збагачення мідних руд проводять шляхом флотації. В результаті одержують мідний концентрат, що містить до 35% міді та до 50% сірки. Концентрати обпалюють зазвичай у печах киплячого шару з метою зниження вмісту сірки до оптимальних значень. При випалюванні відбувається окислення сірки при температурі 750 – 800 °С, частина сірки видаляється з газами. В результаті одержують продукт, званий недогарком.
Плавку на штейн
Плавку на штейн ведуть у відбивних чи електричних печах за нормальної температури 1250 – 1300 °З. У плавку надходять обпалені концентрати мідних руд, в ході нагрівання яких протікають реакції відновлення оксиду міді та вищих оксидівзаліза
6CuO + FeS = 3Cu 2 O + FeO + SO 2
FeS + 3Fe 3 O 4 + 5SiO 2 = 5(2FeO·SiO 2) + SO 2
В результаті взаємодії Cu 2 O з FeS утворюється Cu 2 S реакції:
Cu 2 O + FeS = Cu 2 S + FeO
Сульфіди міді та заліза, сплавляючись між собою, утворюють штейн, а розплавлені силікати заліза, розчиняючи інші оксиди, утворюють шлак. Штейн містить 15-55% Cu; 15 - 50% Fe; 20 - 30% S. Шлак складається в основному з SiO 2 FeO, CaO, Al 2 O 3 .
Штейн і шлак випускають у міру їхнього накопичення через спеціальні отвори.
Конвертування штейна
Конвертування штейна здійснюється в мідеплавильних конвертерах (малюнок 44) шляхом продування його повітрям для окислення сірчистого заліза, переведення заліза в шлак і виділення чорнової міді.
Конвертери мають довжину 6 – 10 м та зовнішній діаметр 3 – 4 м. Заливку розплавленого штейна, злив продуктів плавки та видалення газів здійснюють через горловину, розташовану в середній частині корпусу конвертера. Для продування штейна подається стиснене повітря через фурми, розташовані за утворюючим конвертером. В одній із торцевих стінок конвертера розташований отвір, через який проводиться пневматичне завантаження кварцового флюсу, необхідного для видалення заліза в шлак.
Процес продування ведуть у два періоди. У перший період конвертер заливають штейн і подають кварцовий флюс. У цьому періоді протікають реакції окиснення сульфідів
Закис заліза, що утворюється, взаємодіє з кварцовим флюсом і видаляється в шлак
У міру накопичення шлаку його частково зливають та заливають у конвертер нову порцію вихідного штейна, підтримуючи певний рівень штейна у конвертері. У другому періоді закис міді взаємодіє з сульфідом міді, утворюючи металеву мідь.
Таким чином, в результаті продування одержують чорнову мідь, що містить 98,4 - 99,4% Cu. Отриману чорнову мідь розливають у плоскі виливниці на стрічковій машині.
Технологія виробництва магнію
Основний спосіб виробництва магнію – електролітичний. Електролітичне отримання магнію з водних розчинів неможливе, оскільки електрохімічний потенціал магнію значно негативніший, ніж потенціал розряду іонів водню на катоді. Тому електроліз магнію ведуть із його розплавлених солей.
Основна складова електроліту - хлористий магній МgCl2, а зниження температури плавлення електроліту і підвищення його електропровідності до нього вводять NаСl, СаСl2, КСl і невеликі кількості NaF і СаF2.
Основною сировиною для отримання магнію є карналіт (МgСl2 КСl 6Н2О), магнезит (МgСО3), доломіт (СаСО3 МgСО3), бішофіт (МgСl2 6Н2О). Найбільше магнію отримують з карналіту.
Основні етапи виробництва магнію:
1. Карналіт;
2. Збагачення карналіту;
3. Зневоднення карналіту;
4. Електролітичне отримання магнію;
5. Рафінування магнію;
6. Магній.
Збагачення карналіту є першою стадією його переробки. Сутність процесу збагачення зводиться до відділення КСl та нерозчинних домішок шляхом переведення у водний розчин МgСl2 та КСl. При охолодженні отриманого розчину у вакуум-кристалізаторах випадають кристали штучного карналіту МgСl2 КСl 6Н2О, які відокремлюють фільтруванням.
Карналіт зневоднюють у дві стадії. Першу стадію проводять у трубчастих печах або печах киплячого шару при 550-600 ° С. Під дією теплоти нагрітих газів карналіт зневоднюється і після такої обробки містить 3-4% вологи.
Другу стадію зневоднення здійснюють або плавкою отриманого після першої стадії карналіту в електропечах з подальшим відстоюванням окису магнію, або хлоруванням карналіту в розплавленому стані.
Електролітичне одержання магнію. Для цієї мети застосовують електролізер, який зсередини футерований шамотною цеглою. Анодами є графітові пластини, а катодами - сталеві пластини, розташовані по обидва боки анода.
Для електролітичного розкладання хлористого магнію через електроліт пропускають струм під напругою 2,7-2,8.
Внаслідок електролітичного розкладання хлористого магнію утворюються іони хлору, які рухаються до анода і після розряду створюють бульбашки хлору, що виходять з електроліту. Іони магнію рухаються до катода і після розряду виділяються на поверхні, утворюючи крапельки рідкого магнію. Магній має меншу щільність, ніж електроліт, тому він виринає на його поверхню в катодному просторі, звідки періодично видаляється за допомогою вакуумного ковша.
У процесі електролізу в електроліті підвищується концентрація інших хлоридів за рахунок витрачання МgСl2. Тому періодично частину відпрацьованого електроліту видаляють із ванни і замість нього заливають розплав МgСl2 або карналіту. Внаслідок часткового розкладання домішок на дні ванни утворюється шлам, який регулярно видаляють із ванни.
Рафінування магнію. В електролізних ваннах отримують чорновий магній, який містить 5% домішок: металеві домішки (Fе, Na, К, Аl, Са) і не метал домішки (МgСl2, КСl, NaCl, СаСl2, МgО). Магній очищають (рафінують) переплавленням з флюсами.
Одна вельми сумнівна легенда розповідає, що одного разу до римського імператора Тиберія (42 р. до н. е. - 37 р. н. е.) прийшла людина з металевою чашею, що не б'ється. Матеріал чаші нібито був отриманий з глинозему (Al 2 O 3) і, отже, повинен був являти собою алюміній. Побоюючись, що такий метал із глини може знецінити золото та срібло, Тіберій про всяк випадок наказав відрубати людині голову. Зрозуміло, цій розповіді важко повірити: самородний алюміній у природі не зустрічається, а за часів Римської імперії не могло бути технічних засобів, які б витягти алюміній з його сполук.
За поширеністю у природі алюміній посідає перше місце серед металів; його вміст у земній корі становить 7,45%. Однак, незважаючи на широку поширеність у природі, алюміній до кінця XIX століття належав до рідкісних металів. У чистому вигляді алюміній не зустрічається через свою високу хімічну активність. Він переважно зустрічається у вигляді сполук із киснем та кремнієм – алюмосилікатів.
Рудами алюмінію можуть служити лише породи, багаті на глинозем (Al 2 O 3) і залягають великими масами на поверхні землі. До таких пород відносяться боксити, нефеліни - (Na, K) 2 O ? шпат (ортоклаз) - K 2 OּAl 2 O 3 6SiO 2 .
Основною рудою для отримання алюмінію є боксити. Алюміній в них міститься у вигляді гідроксиду Al(OH), AlOOH, корунду Al 2 O 3 і каолініту Al 2 O 3 2SiO 2 2H 2 O. Хімічний складбокситів складений: 28-70% глинозему; 0,5-20% кремнезему; 2-50% окису заліза; 0,1-10% окису титану. У Останнім часомяк руди стали застосовувати нефеліни та алуніти.
Великі родовища бокситів перебувають на Уралі, в Тихвінському районі Ленінградської області, Алтайському і Красноярському краях.
Нефелін входить до складу апатитонефелінових порід (на Кольському півострові).
Вперше у вільному вигляді алюміній був виділений 1825 р. датським фізиком Ерстедом шляхом впливу амальгами калію на хлорид алюмінію. У 1827р. німецький хімік Велер удосконалив спосіб Ерстеда, замінивши амальгаму калію металевим калієм.
AlCl 3 + 3K→3KCl + Al (Реакція протікає із виділенням тепла).
У 1854 р. Сент-Клер Девіль у Франції вперше застосував спосіб Велера для промислового виробництваалюмінію, використовуючи замість калію більш дешевий натрій, а замість гігроскопічного хлориду алюмінію - стійкіший подвійний хлорид алюмінію та натрію. У 1865 р. російський фізико-хімік Н. Н. Бекетов показав можливість витіснення алюмінію магнієм із розплавленого кріоліту. Ця реакція у 1888 р. була використана для виробництва алюмінію на першому німецькому заводі у Гмелінгені. Виробництво алюмінію цими так званими «хімічними» способами здійснювалося з 1854 по 1890 р. Протягом 35 років за допомогою цих способів, було отримано загалом близько 20 т алюмінію.
Наприкінці 80-х років позаминулого сторіччя хімічні способивитіснив електролітичний спосіб, який дозволив різко знизити вартість алюмінію та створив передумови швидкого розвитку алюмінієвої промисловості. Основоположники сучасного електролітичного способу виробництва алюмінію Еру у Франції та Холл у США незалежно один від одного подали в 1886 майже аналогічні заявки на патентування способу отримання алюмінію електролізом глинозему, розчиненого в розплавленому кріоліті. З моменту появи патентів Еру і Холла і починається сучасна алюмінієва промисловість, яка за 115 років свого існування виросла в одну з найбільших галузей металургії.
Технологічний процес отримання алюмінію складається із трьох основних стадій:
1). Одержання глинозему (Al2O3) з алюмінієвих руд;
2). Одержання алюмінію із глинозему;
3). Рафінування алюмінію.
Отримання глинозему із руд.
Глинозем одержують трьома способами: лужним, кислотним та електролітичним. Найбільше поширення має лужний спосіб (метод К. І. Байєра, розроблений в Росії наприкінці позаминулого століття і застосовується для переробки високосортних бокситів з невеликою кількістю (до 5-6%) кремнезему). З того часу технічне виконання його було суттєво покращено. Схема виробництва глинозему за способом Байєра представлена на рис. 1.
Сутність способу полягає в тому, що алюмінієві розчини швидко розкладаються при введенні в них гідроксиду алюмінію, а розчин, що залишився, після його випарювання в умовах інтенсивного перемішування при 169-170 про С може знову розчиняти глинозем, що міститься в бокситах. Цей спосіб складається з наступних основних операцій:
1). Підготовка бокситу, що полягає в його дробленні та подрібненні в млинах; до млина подають боксит, їдкий луг і не велика кількістьвапна, яке покращує виділення Al 2 O 3 ; отриману пульпу подають на вилуговування;
2). Вилужування бокситу (останнім часом застосовувані досі блоки автоклав круглої форми частково замінені трубчастими автоклавами, в яких при температурах 230-250°С (500-520 К) відбувається вилуговування), що полягає в його хімічному розкладанні від взаємодії з водним розчином лугу; гідрати окису алюмінію при взаємодії зі лугом переходять у розчин у вигляді алюмінію натрію:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH) 3 +NaOH→NaAlO 2 +2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H 2 O;
у розчині алюмінат натрію та силікат натрію утворюють нерозчинний натрієвий алюмосилікат; у нерозчинний залишок переходять окисли титану і заліза, що надають залишку червоного кольору; цей залишок називають червоним шламом. Після закінчення розчинення отриманий алюмінат натрію розбавляють водним розчином лугу при одночасному зниженні температури на 100°З;
3). Відділення алюмінатного розчину від червоного шламу зазвичай здійснюється шляхом промивання у спеціальних згущувачах; внаслідок цього червоний шлам осідає, а алюмінійний розчин зливають і потім фільтрують (освітлюють). В обмежених кількостях шлам знаходить застосування, наприклад як добавка до цементу. Залежно від сорту бокситів на 1 т одержаного окису алюмінію припадає 0,6-1,0 т червоного шламу (сухого залишку);
4). Розкладання алюмінатного розчину. Його фільтрують та перекачують у великі ємності з мішалками (декомпозери). З пересиченого розчину при охолодженні на 60°С (330 До) і постійному перемішуванні витягується гідроксид алюмінію Al(OH) 3 . Так як цей процес протікає повільно і нерівномірно, а формування і зростання кристалів гідроксиду алюмінію мають велике значення при її подальшій обробці, декомпозери додають велику кількість твердого гідроксиду - затравки:
Na 2 OּAl 2 O 3 +4H 2 O→Al(OH) 3 +2NaOH;
5). Виділення гідроксиду алюмінію та його класифікації; це відбувається у гідроциклонах та вакуум-фільтрах, де від алюмінатного розчину виділяють осад, що містить 50-60% частинок Al(OH). Значну частину гідроокису повертають у процес декомпозиції як затравний матеріал, яка залишається в обороті в незмінних кількостях. Залишок після промивання водою йде кальцинацію; фільтрат також повертається в оборот (після концентрації у випарних апаратах - для вилуговування нових бокситів);
6). Зневоднення гідроксиду алюмінію (кальцинації); це завершальна операція виробництва глинозему; її здійснюють у трубчастих обертових печах, а останнім часом також у печах з турбулентним рухом матеріалу при температурі 1150-1300 про З; сирий гідроксид алюмінію, проходячи через піч, що обертається, висушується і зневоднюється; при нагріванні відбуваються послідовно такі структурні перетворення:
| Al(OH) 3 →AlOOH→ γ-Al 2 O 3 → α-Al 2 O 3 | |||
| 200 про С- | 950 про С- | 1200 про З. | |
В остаточно прожареному глиноземі міститься 30-50% -Al 2 O 3 (корунд), решта -Al 2 O 3 .
Цим способом витягується 85-87% від всього одержуваного глинозему. Отриманий окис алюмінію є міцним хімічне з'єднанняз температурою плавлення 2050 о.
Одержання алюмінію з його окису
Електроліз окису алюмінію
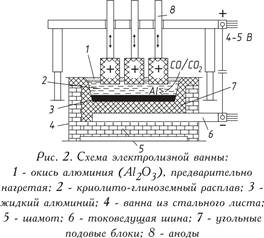
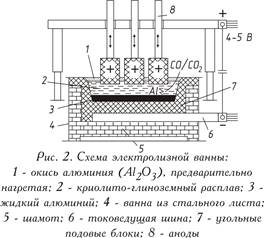 Електролітичне відновлення окису алюмінію, розчиненого в розплаві на основі кріоліту, здійснюється за 950-970°С в електролізері. Електролізер складається з футерованої вуглецевими блоками ванни, до подіни якої підводиться електричний струм. Рідкий алюміній, що виділився на подині, що служить катодом, важчий за розплав солі електроліту, тому збирається на вугільній підставі, звідки його періодично відкачують (рис. 2). Зверху в електроліт занурені вугільні аноди, які згоряють в атмосфері кисню, що виділяється з окису алюмінію, виділяючи окис вуглецю (CO) або двоокис вуглецю (CO 2). На практиці знаходять застосування два типи анодів:
Електролітичне відновлення окису алюмінію, розчиненого в розплаві на основі кріоліту, здійснюється за 950-970°С в електролізері. Електролізер складається з футерованої вуглецевими блоками ванни, до подіни якої підводиться електричний струм. Рідкий алюміній, що виділився на подині, що служить катодом, важчий за розплав солі електроліту, тому збирається на вугільній підставі, звідки його періодично відкачують (рис. 2). Зверху в електроліт занурені вугільні аноди, які згоряють в атмосфері кисню, що виділяється з окису алюмінію, виділяючи окис вуглецю (CO) або двоокис вуглецю (CO 2). На практиці знаходять застосування два типи анодів:
а) самопалюючі аноди Зедерберга, що складаються з брикетів, так званих «хлібів» маси Зедерберга (малозолильне вугілля з 25-35% кам'яновугільного пеку), набитих в алюмінієву оболонку; під дією високої температури анодна маса випалюється (спікається);
б) обпалені, або «безперервні», аноди з великих вугільних блоків (наприклад, 1900 600 500 мм масою близько 1,1 т).
Сила струму на електролізерах становить 150 000 А. Вони входять у мережу послідовно, т. е. виходить система (серія) - довгий ряд електролізерів.
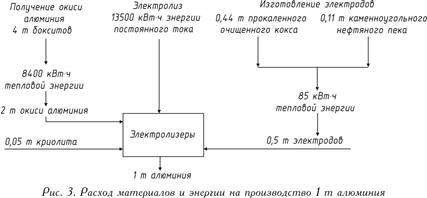
Робоча напруга на ванні, що становить 4-5 В, значно вище напруги, при якому відбувається розкладання окису алюмінію, оскільки в процесі роботи неминучі втрати напруги різних частинахсистеми. Баланс сировини та енергії при отриманні 1 т алюмінію представлений на рис. 3.
Електроліз хлориду алюмінію (метод фірми Алкоа)
 У реакційній посудині окис алюмінію перетворюється спочатку на хлорид алюмінію. Потім у щільно ізольованій ванні відбувається електроліз AlCl 3 розчиненого в розплаві солей KCl, NaCl. Хлор, що виділяється при цьому, відсмоктується і подається для вторинного використання; алюміній осідає на катоді.
У реакційній посудині окис алюмінію перетворюється спочатку на хлорид алюмінію. Потім у щільно ізольованій ванні відбувається електроліз AlCl 3 розчиненого в розплаві солей KCl, NaCl. Хлор, що виділяється при цьому, відсмоктується і подається для вторинного використання; алюміній осідає на катоді.
Перевагами даного методуперед існуючим електролізом рідкого кріолітоглиноземного розплаву (Al 2 O 3 розчинена в кріоліті Na 3 AlF 6) вважають: економію до 30% енергії; можливість застосування окису алюмінію, який не підходить для традиційного електролізу (наприклад, Al 2 O 3 с високим змістомкремнію); заміну дорогого кріоліту дешевшими солями; зникнення небезпеки виділення фтору.
Відновлення хлориду алюмінію марганцем (Toth – метод)
 При відновленні марганцем із хлориду алюмінію звільняється алюміній. Через керовану конденсацію з потоку хлориду марганцю виділяються пов'язані з хлором забруднення. При звільненні хлору хлорид марганцю окислюється в окис марганцю, який відновлюється до марганцю, придатного до вторинного застосування. Відомості в наявних публікаціях дуже неточні, тому в даному випадкудоведеться відмовитися від оцінки методу.
При відновленні марганцем із хлориду алюмінію звільняється алюміній. Через керовану конденсацію з потоку хлориду марганцю виділяються пов'язані з хлором забруднення. При звільненні хлору хлорид марганцю окислюється в окис марганцю, який відновлюється до марганцю, придатного до вторинного застосування. Відомості в наявних публікаціях дуже неточні, тому в даному випадкудоведеться відмовитися від оцінки методу.
Отримання рафінованого алюмінію
Для алюмінію рафінуючий електроліз з розкладанням сольових водних розчинів неможливий. Оскільки для деяких цілей ступінь очищення промислового алюмінію (Al 99,5 - Al 99,8), отриманого електролізом криолитоглиноземного розплаву, недостатня, з промислового алюмінію або відходів металу шляхом рафінування отримують ще чистіший алюміній (Al 99, 99 R). Найбільш відомий метод рафінування – тришаровий електроліз.
Рафінування методом тришарового електролізу
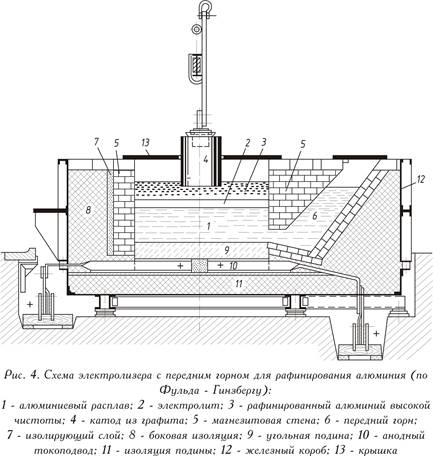
Одягнена сталевим листом, що працює на постійному струмі (представлена на рис. 4 - див. вище) ванна для рафінування складається з вугільної подини з струмопідведення і теплоізолюючої магнезитової футеровки. На противагу електролізу кріолітоглиноземного розплаву анодом тут служить, як правило, розплавлений рафінований метал (нижній анодний шар). Електроліт складається з чистих фторидів або суміші хлориду барію та фторидів алюмінію та натрію (середній шар). Алюміній, що розчиняється з анодного шару електроліті, виділяється над електролітом (верхній катодний шар). Чистий метал є катодом. Підведення струму до катодного шару здійснюється графітовим електродом.
Ванна працює при 750-800°С, витрата електроенергії становить 20 кВт на 1 кг чистого алюмінію, тобто дещо вище, ніж при звичайному електролізі алюмінію.
Метал анода містить 25-35% Cu; 7-12% Zn; 6-9% Si; до 5% Fe та незначна кількість марганцю, нікелю, свинцю та олова, решта (40-55%) – алюміній. Усі важкі метали та кремній при рафінуванні залишаються в анодному шарі. Наявність магнію в електроліті призводить до небажаних змін складу електроліту або сильного його ошлакування. Для очищення магнію шлаки, що містять магній, обробляють флюсами або газоподібним хлором.
В результаті рафінування отримують чистий алюміній (99,99%) та продукти сегрегації (зайгер-продукт), які містять важкі метали та кремній та виділяються у вигляді лужного розчину та кристалічного залишку. Лужний розчин є відходом, а твердий залишок застосовується для розкислення.
Рафінований алюміній зазвичай має наступний склад, %: Fe 0,0005-0,002; Si 0,002-0,005; Cu 0,0005-0,002; Zn 0,0005-0,002; Mg сліди; Al інше.
Рафінований алюміній переробляють на напівфабрикат у зазначеному складі або легують магнієм (див. табл. 1.2).
ТАБЛИЦЯ 1.2.Хімічний склад алюмінію підвищеної чистоти та первинного алюмінію DIN 1712, Лист 1.
| Марка | Номер | Допустимі домішки* , % | |||||||
| всього | в тому числі | ||||||||
| Si | Fe | Ti | Cu | Zn | інші | ||||
| A199,99R | 3.0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 | |
| A199,9H | 3.0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 | |
| A199,8H | 3.0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,7H | 3.0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,5H** | 3.0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 | |
| A199H | 3.0200 | 1,0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 | |
* Наскільки можливо визначити звичайними методами дослідження. ** Чистий алюміній для електротехніки (алюмінієві провідники) постачають у вигляді первинного алюмінію 99,5, що містить не більше 0,03% (Ti+Cr+V+Mn); позначається у разі E-A1, номер матеріалу 3.0256. В іншому відповідає нормам VDE-0202. |
|||||||||
Рафінування шляхом алюмоорганічних комплексних сполук та зонною плавкою
Алюміній ступеня чистоти вище марки A1 99,99 R може бути отриманий рафінуючим електролізом чистого або технічно чистого алюмінію із застосуванням електроліту комплексних алюмоорганічних сполук алюмінію. Електроліз проходить при температурі близько 1000°С між твердими алюмінієвими електродами і в принципі схожий на рафінуючий електроліз міді. Природа електроліту диктує необхідність працювати без доступу повітря та за низької щільності струму.
Цей вид рафінуючого електролізу, що застосовується спочатку лише в лабораторному масштабі, вже здійснюється у невеликому виробничому масштабі – виготовляється кілька тонн металу на рік. Номінальний ступінь очищення одержуваного металу 99,999-99,9999%. Потенційними областями застосування металу такої чистоти є кріогенна електротехніка та електроніка.
Можливе застосування розглянутого методу рафінування та в гальванотехніці.
Ще більш високу чистоту – номінально до A1 99,99999 – можна отримати наступною зонною плавкою металу. При переробці алюмінію підвищеної чистоти на напівфабрикат, лист або дріт необхідно, враховуючи низьку температурурекристалізації металу, вживати особливих запобіжних заходів. Примітною властивістю рафінованого металу є його висока електропровідність у сфері кріогенних температур.
Отримання вторинного алюмінію
Переробка вторинної сировини та відходів виробництва є економічно вигідною. При цьому вторинними сплавами задовольняється близько 25% загальної потреби в алюмінії.
 Найважливішою сферою застосування вторинних сплавів є виробництво фасонного алюмінієвого лиття. У DIN 1725 лист 2 поряд зі стандартними марками сплавів наведені численні марки сплавів, що виробляються ливарними заводами. Перелік сплавів, які випускаються цими заводами, містить, крім стандартних, деякі нестандартні сплави.
Найважливішою сферою застосування вторинних сплавів є виробництво фасонного алюмінієвого лиття. У DIN 1725 лист 2 поряд зі стандартними марками сплавів наведені численні марки сплавів, що виробляються ливарними заводами. Перелік сплавів, які випускаються цими заводами, містить, крім стандартних, деякі нестандартні сплави.
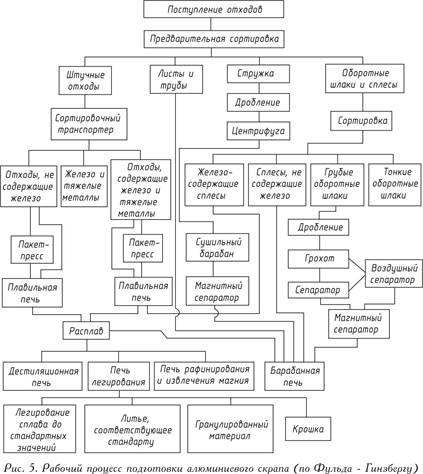
Бездоганне приготування алюмінієвого скрапу у найрізноманітніших пропорціях можна здійснювати лише спеціально обладнаних плавильних заводах. Уявлення про складний робочий процес на такому заводі дає рис. 5.
Відходи переплавляють після грубого попереднього сортування. Залізо, нікель або мідь, що містяться в цих відходах, точка плавлення яких вище точки плавлення алюмінію, при плавці в плавильній пороговій печі залишаються в ній, а алюміній виплавляється. Для видалення з відходів неметалевих включень типу оксидів, нітридів, карбідів або газів застосовують обробку розплавленого металу солями або (що раціональніше) продування газом - хлором або азотом.
Для видалення металевих домішок з розплаву відомі різні методи, наприклад, присадка магнію і вакуумування - метод Бекша (Becksche); присадка цинку або ртуті з наступним вакуумуванням - субгалогенний метод. Видалення магнію обмежується введенням у розплавлений метал хлору. Шляхом введення добавок, що точно визначаються складом розплаву, отримують заданий ливарний сплав.
Виробництво алюмінію технічної чистоти
Електролітичний спосіб - єдиний застосовується у всьому світі для виробництва металевого алюмінію технічної чистоти. Всі інші способи (цинкотермічний, карбідотермічний, субхлоридний, нітридний та ін), за допомогою яких алюміній може бути вилучений з алюмінієвих руд, розроблялися в лабораторному та дослідно-промислових масштабах, проте поки не знайшли практичного застосування.
Для отримання алюмінієво-кремнієвих сплавів успішно застосовується електротермічний спосіб, вперше розроблений та здійснений у промисловому масштабі у СРСР. Він складається з двох стадій: на першій стадії одержують первинний алюмінієво-кремнієвий сплав із вмістом 60-63 % Al шляхом прямого відновлення алюмо-кремнистих руд у рудно-термічних електричних печах; на другій стадії первинний сплав розбавляють технічним алюмінієм, отримуючи силумін та інші ливарні та деформовані алюмінієво-кремнієві сплави. Ведуться дослідження щодо вилучення з первинного сплаву алюмінію технічної чистоти.
В цілому одержання алюмінію електролітичним способом включає виробництво глинозему (окису алюмінію) з алюмінієвих руд, виробництво фтористих солей (кріоліту, фтористого алюмінію і фтористого натрію), виробництво вуглецевої анодної маси, обпалених вугільних анодних і катодних блоків. власне електролітичне виробництво алюмінію, яке є завершальним етапом сучасної металургії алюмінію.
Характерним для виробництва глинозему, фтористих солей та вуглецевих виробів є вимога максимального ступеня чистоти цих матеріалів, оскільки в кріолітоглиноземних розплавах, що піддаються електролізу, не повинні утримуватися домішки елементів, більш електропозитивних, ніж алюміній, які, виділяючись на катоді в першу чергу, забруднювали б метал.
У глиноземі марок Г-00, Г-0 та Г-1, які переважно використовуються при електролізі, вміст SiO 2 становить 0,02-0,05%, aFe 2 O 3 - 0,03-0,05%. У кріоліті в середньому міститься 0,36-0,38% SiO 2 і 0,05-0,06% Fe 2 O 3 у фтористому алюмінію 0,30-0,35% (SiO 2 + Fe 2 O 3). В анодній масі міститься не більше 0,25% SiO2 і 0,20% Fe2O3.
Найважливіша алюмінієва руда, з якої витягають глинозем, боксит. У бокситі алюміній присутній у формі гідроксиду алюмінію. У Радянському Союзі, крім бокситу, для одержання глинозему застосовують нефелінову породу - алюмосилікат натрію та калію, а також алунітову породу, в якій алюміній знаходиться у вигляді його сульфату. Сировиною для виготовлення анодної маси та обпалених анодних блоків служать вуглецеві чисті матеріали - нафтовий або печовий кокс і кам'яновугільний печ як сполучний, а для виробництва кріоліту та інших фтористих солей - фтористий кальцій (плавиковий шпат).
При електролітичному отриманні алюмінію глинозему Al 2 O 3 розчинений в розплавленому кріоліті Na 3 AlF 6 електрохімічно розкладається з розрядом катіонів алюмінію на катоді (рідкому алюмінії), а кисневмісних іонів (іонів кисню) - на вуглецю.
за сучасним уявленням, кріоліт у розплавленому стані дисоціює на іони та : , а глинозем - на комплексні іони та : ![]() , які перебувають у рівновазі з простими іонами:
, які перебувають у рівновазі з простими іонами: ![]() ,
, ![]() .
.
Основним процесом, що відбувається на катоді, є відновлення іонів тривалентного алюмінію: Al 3+ + 3 e→ Al (I).
Поряд із основним процесом можливий неповний розряд тривалентних іонів алюмінію з утворенням одновалентних іонів: Al 3+ + 2 e→ Al + (II) і, нарешті, розряд одновалентних іонів із виділенням металу: Al + + e→ Al (III).
За певних умов (відносно велика концентрація іонів Na + , висока температурата ін) може відбуватися розряд іонів натрію з виділенням металу: Na + + e→ Na (IV). Реакції (II) та (IV) обумовлюють зниження виходу алюмінію струмом.
На вугільному аноді відбувається розряд іонів кисню: 2O 2-4 e→ O 2 . Однак кисень не виділяється у вільному вигляді, оскільки він окислює вуглець аноду з утворенням суміші CO2 та CO.
Сумарна реакція, що відбувається в електролізері, може бути представлена рівнянням Al2O3+ x C ↔ 2Al + (2 x-3)CO + (3- x) CO 2 .
До складу електроліту промислових алюмінієвих електролізерів, крім основних компонентів - кріоліту, фтористого алюмінію та глинозему, входять невеликі кількості (у сумі до 8-9%) деяких інших солей - CaF 2 , MgF 2 , NaCl і LiF (добавки), які покращують деякі фізико-хімічні властивості електроліту і цим підвищують ефективність роботи електролізерів. Максимальний вміст глинозему в електроліті зазвичай становить 6-8%, знижуючись в процесі електролізу. У міру збіднення електроліту глиноземом до нього вводять чергову порцію глинозему. Для нормальної роботи алюмінієвих електролізерів відношення NaF: AlF 3 в електроліті підтримують у межах 2,7-2,8, додаючи порції кріоліту та фтористого алюмінію.
У виробництві алюмінію застосовують електролізери з вугільними анодами, що самообпалюються, і бічним або верхнім підведенням струму, а також електролізери з попередньо обпаленими вугільними анодами. Найбільш перспективною є конструкція електролізерів з обпаленими анодами, що дозволяє збільшити одиничну потужність агрегату, знизити питому витрату електроенергії постійного струму на електроліз, отримати більш чистий метал, покращити санітарно-гігієнічні умови праці та зменшити викиди шкідливих речовин в атмосферу.
Основні технічні параметри та показники роботи алюмінієвих електролізерів різного типу наведені у табл. 1.3.
ТАБЛИЦЯ 1.3
ОСНОВНІ ТЕХНІЧНІ ПАРАМЕТРИ І ПОКАЗНИКИ РОБОТИ АЛЮМІНІЄВИХ ЕЛЕКТРОЛІЗЕРІВ
| Параметри та показники | З анодами, що самопалюються. | З обпаленими анодами | |
бічний струмопідведення |
верхній струмопідвід | ||
| Сила струму, як | 60-120 | 60-155 | 160-255 |
| Добова продуктивність електролізера, т | 0,42-0,85 | 0,40-1,10 | 1,10-1,74 |
| Анодна щільність струму, А/см 2 | 0,80-0,90 | 0,65-0,70 | 0,70-0,89 |
| Середня напруга на електролізері, | 4,45-4,65 | 4,50-4,70 | 4,30-4,50 |
| Вихід за струмом, % | 85-88 | 84-86 | 85-89 |
| Витратні коефіцієнти на 1 т алюмінію: | |||
| електроенергії постійного струму, кВт | 15100-16200 | 15500-17300 | 14500-15500 |
| глинозему, кг | 1920-1940 | 1920-1940 | 1920-1940 |
| анодної маси, кг | 520-560 | 560-620 | - |
| обпалених анодів, кг | - | - | 540-600 |
| Фтористих солей у перерахунку на фтор, кг | 20-30 | 25-35 | 15-25 |
Первинний алюміній, що витягується з електролізерів (алюміній-сирець), містить ряд домішок, які можна поділити на три групи: неметалеві (фтористі солі, α- і γ-глинозем, карбід і нітрид алюмінію, вугільні частинки, що механічно захоплюються при виливці металу з електролізера); металеві (залізо, кремній), що переходять із сировини, вугільних матеріалів та конструктивних елементів електролізера; газоподібні - переважно водень, що утворюється в металі внаслідок електролітичного розкладання води, що потрапляє в електроліт із сировиною.
З металевих домішок, окрім заліза та кремнію, міститься найбільша кількість галію, цинку, титану, марганцю, натрію, ванадію, хрому, міді. Зміст цих та деяких інших металевих мікродомішок електролітичному алюмініїнаведено нижче, %:
Основним джерелом надходження металевих мікродомішок до алюмінію є глинозем, який залежно від виду вихідної сировини може містити галій, цинк, калій, фосфор, сірку, ванадій, титан і хром. Вуглецеві матеріали (анодна маса, обпалені аноди, катодні вироби) є джерелом таких мікродомішок, як, наприклад, ванадій, титан, марганець, цинк.
Електролізом кріоліто-глиноземних розплавів за умови застосування чистих вихідних матеріалів (насамперед глинозему та вуглецевих матеріалів) вдається отримати алюміній-сирець марок А85 та А8 (99,85 та 99,80%). Найбільша частка металу цих марок (60-70% від загального випуску) виходить на електролізер з обпаленими анодами, а також на електролізер з бічним підведенням струму (до 70% від загального виробництва). На електролізерах з самопальними анодами і верхнім струмопідведенням випуск алюмінію-сирцю марки А8 невисокий (становить 1-3%), а метал марки А85 отримати не вдається через значні домішки заліза, що надходить в алюміній з несировинних джерел (анодні , Технологічний інструмент, катодний вузол).
Розплавлений первинний алюміній, витягнутий з електролізерів за допомогою вакуумного ковша, надходить у ливарне відділення для рафінування від неметалевих та газових домішок та подальшої переробки в товарну продукцію (чушки, циліндричні та плоскі зливки, катанку тощо). Перед розливанням алюміній-сирець витримують у розплавленому стані в електричних печах опору (міксерах) або газових відбивних печах. У цих печах не тільки проводять раціональну шихтовку різних за складом порцій рідкого алюмінію, а й частково очищають від неметалевих включень, плівок окисних і натрію.
Розлив алюмінію з міксера в чушки проводиться за допомогою ливарних машин конвеєрного типу; циліндричні та плоскі зливки виготовляють методом напівбезперервного лиття, а для отримання катанки застосовують спеціальні агрегати поєднаного лиття та прокатки.
На вітчизняних алюмінієвих заводах при литті злитків алюміній, що надходить з міксера в кристалізатор ливарної машини, піддають найпростішому виду рафінування - фільтрації розплаву через склосітку з осередками розміром від 0,6×0,6 до 1,7×1,7 мм. Цей метод дозволяє очищати алюміній лише від дуже грубих окисних включень; Найбільш досконалий спосіб фільтрації розплаву через склосітку у висхідному потоці. При такому способі фільтрування частинки окисних включень, зіштовхуючись із сіткою, не захоплюються потоком розплаву, а осідають на дні ливарного жолоба.
Для одночасного очищення алюмінію як від неметалевих домішок, так і від водню успішно застосовується метод фільтрації через флюсовий фільтр у поєднанні з продувкою азотом. Як флюс можна використовувати кислий електроліт алюмінієвих електролізерів. В результаті такої очистки вміст водню в алюмінії знижується з 0,22 до 0,16 см 3 на 100 г металу.
У первинному алюмінії, який використовується для виробництва сплавів системи Al-Mg, вміст натрію не повинен перевищувати 0,001%. Це з тим, присутність натрію у цих сплавах погіршує механічні та інші експлуатаційні властивості виробів, застосовуваних у низці галузей народного господарства.
Найбільш ефективним методомодночасного рафінування алюмінію від натрію, водню та неметалічних домішок є продування розплавленого металу газовою сумішшю азоту з 2-10% хлору, що вводиться в розплав у вигляді дрібних бульбашок за допомогою спеціальних пристроїв. Цей спосіб рафінування дозволяє знизити вміст натрію алюмінію до 0,0003-0,001% при витраті газової суміші від 0,8 до 1,5 м 3 /т металу.
Витрата електроенергії на виробництво 1 т товарного алюмінію з металу-сирцю при використанні електропечей становить 150-200 кВт/год; безповоротні втрати металу на ливарному переділі дорівнюють 1,5-5 % залежно від виду товарної продукції.
Одержання алюмінію високої чистоти
Для одержання алюмінію високої чистоти (марок А995-А95) первинний алюміній технічної чистоти електролітично рафінують. Це дозволяє знизити в алюмінії вміст металевих та газоподібних домішок і тим самим значно підвищити його електропровідність, пластичність, відбивну здатність та корозійну стійкість.
Електролітичне рафінування алюмінію здійснюють електролізом розплавлених солей за тришаровим способом. Сутність способу полягає в наступному. У рафінувальному електролізері є три розплавлені шари. Нижній, найважчий, лежить на струмопровідній подіні і служить анодом; він називається анодним сплавом і являє собою сплав алюмінію, що рафінується, з міддю, яку вводять для обтяження шару. Середній шар – розплавлений електроліт; його щільність менша за щільність анодного сплаву і вище за щільність чистого рафінованого (катодного) алюмінію, що знаходиться над електролітом (верхній, третій рідкий шар).
При анодному розчиненні всі домішки електропозитивніші, ніж алюміній (Fe, Si, Ti, Cu та ін), залишаються в анодному сплаві, не переходячи в електроліт. Анодно розчинятися буде лише алюміній, який у формі іонів Al 3+ переходить до електроліту: Al– 3 e→ Al 3+.
При електролізі іони алюмінію переносяться до катода, на якому розряджаються: Al 3+ + 3 e→ Al. В результаті на катоді накопичується шар розплавленого рафінованого алюмінію.
Якщо в анодному сплаві присутні домішки електронегативніші, ніж алюміній (наприклад, Ba, Na, Mg, Ca), то вони можуть електрохімічно розчинятися на аноді разом з алюмінієм і у вигляді іонів переходити в електроліт. Оскільки вміст електронегативних домішок в алюмінію-сирці невеликий, у помітній кількості в електроліті вони не накопичуються. Розряду цих іонів на катоді практично не відбувається, так як їхній електродний потенціал електронегативніший за алюміній.
Як електроліт при електролітичному рафінуванні алюмінію в Радянському Союзі та в більшості країн застосовують фторидно-хлоридний електроліт, склад якого 55-60% BaCl 2 , 35-40% AlF 4 +NaF і 0-4% NaCl. Молярне відношення NaF: AlF 3 підтримують 1,5-2,0; температура плавлення електроліту 720-730 ° C; температура процесу електролізу близько 800°C; густина електроліту 2,7 г/см 3 .
Анодний сплав готують із первинного алюмінію та чистої міді (99,90-99,95% Cu), яку вводять у метал у кількості 30-40%. Щільність рідкого анодного сплаву такого складу 3-3,5 г/см 3 ; щільність чистого розплавленого катодного алюмінію дорівнює 2,3 г/см 3 . При такому співвідношенні щільностей створюються умови, необхідні хорошого поділу трьох розплавлених шарів.
У четверній системі Al-Cu-Fe-Si, до якої належить анодний сплав, утворюється евтектика з температурою плавлення 520°C. Охолоджуючи анодний сплав, що містить домішки заліза та кремнію в кількостях вище евтектичних концентрацій, можна виділити залізо та кремній у тверду фазу у вигляді інтерметалевих сполук FeSiAl 5 та Cu 2 FeAl 7 . Так як температура анодного сплаву в кишенях електролізера на 30-40°C нижче за температуру анодного сплаву в робочому просторі ванни, в них (у міру накопичення в анодному сплаві заліза і кремнію) виділятимуться тверді інтерметалічні опади. Періодично видаляючи ці опади, очищають анодний сплав (без оновлення) від домішок заліза і кремнію. Так як в анодному сплаві концентрується галій, то опади, що витягуються з електролізера (30-40 кг на 1 т алюмінію) можуть служити джерелом отримання цього металу.
Для електролітичного рафінування служать електролізери, які за конструкцією нагадують електролізери з обпаленими анодами для електролітичного отримання первинного алюмінію, але мають інше підключення полюсів: подина служить анодом, а верхній ряд електродів - катодом. Сучасні електролізери для електролітичного рафінування алюмінію розраховані на силу струму до 75 кА.
Нижче наведено основні техніко-економічні показники електролізерів за 1979 р., досягнуті вітчизняними (1, 2, 3) підприємствами.
Електрохімічний вихід струму, розрахований по вилитому з електролізера металу, становить 97-98%. Фактичний вихід по струму, розрахований за кількістю товарного металу, становить 92-96%.
| Сила струму, як | 23,5 | 62,9 | 69,8* |
| Середня напруга, | 5,43 | 5,68 | 5,69 |
| Вихід за струмом, % | 95,7 | 93,0 | 92,7 |
| Витрата електроенергії постійного струму, кВт ּ ч/т | 17 370 | 18 700 | 19 830 |
| Сумарний електроенергії змінного струму, кВт ּ ч/т | 18 670 | 19 590 | 20 780 |
| Рівні, см | |||
| катодного алюмінію | 16,6 | 12,9 | 14,6 |
| електроліту | 13,3 | 11,6 | 14,2 |
| анодного сплаву | 40,1 | 29,5 | 30,0 |
| Витратні коефіцієнти, кг/т: | |||
| хлористий барій | 40,5 | 41,5 | 27,0 |
| кріоліт | 27,7 | 21,0 | 16,5 |
| фтористий алюміній | 6,7 | 13,1 | 3,8 |
| хлористий натрій | 1,0 | 4,8 | - |
| алюміній-сирець | 1020 | 1028 | 1032 |
| графіт | 11,9 | 11,5 | 16,6 |
| мідь | 9,8 | 15,5 | 16,4 |
| Випуск алюмінію високої чистоти, % марок: | |||
| А995 | 47,8** | 3,5 | 2,1 |
| А99 | 30,4 | 67,1 | 54,2 |
| А97 | 8,3 | 21,5 | 43,7 |
| А95 | 10,4 | 7,9 | - |
| нижче А95 | 3,1 | - | - |
* Показники виробництва алюмінію високої чистоти. ** Сортність по електролізерах без розшиття. |
|||
Основним фактором, що знижує вихід по струму, крім прямих втрат струму на розряд електронегативних іонів, втрат металу за рахунок його окислення і механічних втрат алюмінію, є робота електролізерів з випуском несортового металу, який знову повертається в анодний сплав для подальшого рафінування. Ці періоди роботи електролізерів мають місце при пуску електролізерів та порушення технологічного режиму.
Електролітичне рафінування алюмінію є дуже енергоємним виробництвом. Витрата електроенергії в змінному струмі, включаючи енергію, витрачену на підготовку електроліту та анодного сплаву, роботу вентиляційних пристроїв та транспортних засобів, а також втрати на перетворення змінного струму на постійний, становить 18,5-21,0 тис. кВт/год на 1 т алюмінію. Енергетичний к. п. д. рафінувальних електролізерів не перевищує 5-7%, тобто 93-95% енергії витрачається у вигляді втрат тепла, що виділяється в основному в шарі електроліту (приблизно 80-85% від загального приходу тепла). Отже, основними шляхами подальшого зниження питомої витрати електроенергії на електролітичне рафінування алюмінію є вдосконалення теплоізоляції електролізера (особливо верхньої частини конструкції) та зниження шару електроліту (зменшення міжелектродної відстані).
Чистота алюмінію, рафінованого за тришаровим методом, 99,995%; вона визначається по різниці з п'ятьма основними домішками - залізом, кремнієм, міддю, цинком та титаном. Кількість одержуваного металу такої марки може становити 45-48% від загального випуску (без його розшивки з нижчими, сортами).
Слід, однак, відзначити, що електролітично рафінованому алюмінію містяться в менших кількостях домішки інших металів, що знижує абсолютну чистоту такого алюмінію. Радіоактиваційний аналіз дозволяє виявити в електролітично рафінованому алюмінію до 30 домішок, сумарний вміст яких приблизно 60-10 -4%. Отже, чистота рафінованого алюмінію за різницею з цими домішками становить 99,994%.
Крім домішок, передбачених ГОСТом (див. табл. 1.1), найбільш поширеній марці (А99) електролітично рафінованого алюмінію міститься, %: Cr 0,00016; V 0,0001; Ga 0,0006; Pb 0,002; Sn 0,00005; Ca 0,002-0,003; Na 0,001-0,008; Mn 0,001-0,007; Mg 0,001-0,007; As<0,0001; Sb<0,00002; Bi<0,00001; Cd<0,000001; S 0,0007.
Один із джерел забруднення катодного алюмінію - графітові струмовідводи, що містять окис заліза і кремнію і постійно стикаються з рафінованим алюмінієм. Якщо струм до катодного алюмінію підводити безпосередньо алюмінієвими шинами і застосовувати інструмент із дуже чистого графіту, можна отримувати метал чистотою 99,999% по різниці з домішками (Fe, Si, Cu, Zn і Ti). B такому металі міститься в середньому %: Si 0,0002; Fe 0,00032; Cu 0,0002; Zn 0,0002 та Ti 0,00005. Однак через технічні труднощі такий спосіб підведення струму поки що не знайшов широкого промислового застосування.
Набуття алюмінію особливої чистоти
Алюміній особливої чистоти (марки A999) може бути отриманий трьома способами: зонною плавкою, дистиляцією через субгалогеніди та електролізом алюміній-органічних сполук. З перерахованих способів отримання алюмінію особливої чистоти практичне застосування СРСР отримав спосіб зонної плавки.
Принцип зонної плавки полягає в багаторазовому проходженні розплавленої зони вздовж зливу алюмінію. За величиною коефіцієнтів розподілу К=Ств /Сж (де Зтв - концентрація домішки в твердій та Зж - в рідкій фазі), які значною мірою визначають ефективність очищення від домішок, ці домішки можуть бути розбиті на три групи. До першої групи відносяться домішки, що знижують температуру плавлення алюмінію; вони мають До<1 при зонній плавці концентруються в розплавленій зоні і переносяться нею до кінцевої частини зливка. До цих домішок належать Ga, Sn, Be, Sb, Ca, Th, Fe, Co, Ni, Ce, Te, Ba, Pt, Au, Bi, Pb, Cd, In, Na, Mg, Cu, Si, Ge , Zn. До другої групи належать домішки, що підвищують температуру плавлення алюмінію; вони характеризуються До>1і при зонній плавці концентруються у твердій (початковій) частині злитка. До цих домішок відносяться Nb, Ta, Cr, Ti, Mo, V. До третьої групи належать домішки з коефіцієнтом розподілу, дуже близьким до одиниці (Mn, Sc). Ці домішки практично не видаляються при зонній плавці алюмінію.
Алюміній, призначений для зонної плавки, піддають деякій підготовці, яка полягає у фільтрації, дегазації та травленні. Фільтрація необхідна для видалення з алюмінію тугоплавкою та міцної окисної плівки диспергованої в металі. Окис алюмінію, присутня в розплавленому алюмінії, може при його твердінні створювати центри кристалізації, що веде до отримання полікристалічного зливка та порушення ефекту перерозподілу домішок між твердим металом та розплавленою зоною. Фільтрацію алюмінію ведуть у вакуумі (залишковий тиск 0,1-0,4 Па) через отвір у дні графітового тигля діаметром 1,5-2 мм. Попередню дегазацію алюмінію перед зонною плавкою (також нагріванням у вакуумі) проводять для попередження розбризкування металу при розплавленні зони у разі проведення процесу у глибокому вакуумі. Остання стадія підготовки алюмінію до зонної плавки - травлення його поверхні сумішшю концентрованих соляної та азотної кислот.
Так як алюміній має значну хімічну активність і як основний матеріал для контейнерів (човників) застосовують особливо чистий графіт, то зонну плавку алюмінію проводять у вакуумі або в атмосфері інертного газу (аргон, гелій).
Зонною плавкою у вакуумі забезпечується велика чистота алюмінію внаслідок випаровування частини домішок при вакуумуванні (магнію, цинку, кадмію, лужних та лужноземельних металів), а також виключається забруднення очищеного металу домішками внаслідок застосування захисних інертних газів. Зонну плавку алюмінію у вакуумі можна проводити при безперервному відкачуванні кварцової труби, куди поміщають графітовий човник зі злитком алюмінію, а також у запаяних кварцових ампулах, з яких попередньо відкачують повітря до залишкового тиску приблизно 1?10 -3 Па.
Для створення розплавленої зони на зливці алюмінію при його зонній плавці може бути застосований нагрівання за допомогою невеликих печей опору або струмів високої частоти. Для електроживлення печей електроопору не потрібна складна апаратура, печі прості в експлуатації. Єдиний недолік цього методу нагріву - невеликий переріз зливка алюмінію, що очищається.
Індукційне нагрівання струмами високої частоти - ідеальний спосіб створення розплавленої зони на злитку при зонній плавці. Метод високочастотного нагріву (крім того, що він дозволяє здійснити зонне плавлення злитків великих перерізів) має важливу перевагу, що полягає в тому, що розплавлений метал безперервно перемішується в зоні; це полегшує дифузію атомів домішки від фронту кристалізації в глиб розплаву.
Вперше промислове виробництво алюмінію високої чистоти зонною плавкою було освоєно на Волхівському алюмінієвому заводі 1965 р. на установці УЗПІ-3, розробленої ВАМІ. Ця установка була оснащена чотирма кварцовими ретортами з індукційним нагріванням, причому індуктори були рухливими, а контейнери з металом нерухомими. Продуктивність її становила 20 кг металу за цикл очищення. Згодом була створена та введена в промислову експлуатацію у 1972 р. на Волховському алюмінієвому заводі більш високопродуктивна цільнометалева установка УЗПІ-4.
Ефективність очищення алюмінію при зонному плавленні може бути охарактеризована такими даними. Якщо сумарний вміст домішок в електролітично рафінованому алюмінії становить (30÷60) 10 –4 %, то після зонної плавки воно знижується до (2,8 ÷ 3,2) 10 –4 %, тобто в 15-20 разів. Це відповідає залишковому електроопору алюмінію ρ ○ (при температурі рідкого гелію 4,2 К) відповідно (20÷40)10 -10 і (1,8÷2,1)10 -10 або чистоті 99,997-99,994 і 99,9997%. У табл. 1.4 (див. нижче) наведено дані радіоактиваційного аналізу про вміст деяких домішок у зонно-очищеному алюмінії та електролітично рафінованому. Ці дані свідчать про сильне зниження вмісту більшості домішок, хоча такі домішки, як марганець і скандій, при зонній плавці практично не видаляються.
В останні роки у ВАМІ розроблено та випробувано в промислових умовах технологію отримання алюмінію чистотою 99,9999% методом каскадної зонної плавки. Сутність способу каскадної зонної плавки полягає в тому, що очищення вихідного алюмінію чистотою ведуть А999, послідовно повторюючи цикли (каскади) зонної планки. При цьому вихідним матеріалом кожного наступного каскаду служить середня, найчистіша частина зливка, що отримується в результаті попереднього циклу очищення.
ТАБЛИЦЯ 1.4
| Домішка | Вихідний алюміній (електролітично рафінований 99,993-99,994%) | Алюміній після зонної плавки | |
| графіт, вакуум | алунд, повітря | ||
| Мідь | 1,9 | 0,02 | 0,08 |
| Миш'як | 0,15 | 0,0015 | 0,001 |
| Сурма | 1,2 | 0,03 | 0,02 |
| Уран | 0,002 | - | - |
| Залізо | 3 | ≤0,2 | ≤0,3 |
| Галій | 0,3 | 0,02 | 0,05 |
| Марганець | 0,2-0,3 | 0,1-0,2 | 0,15 |
| Скандій | 0,4-0,5 | 0,4-0,5 | 0,4-0,5 |
| Ітрій | 0,02-0,04 | <<0,001 | <<0,001 |
| Лютецій | 0,002-0,004 | <<0,0001 | <<0,0001 |
| Гольмій | 0,005-0,01 | <<0,0001 | <<0,0001 |
| Гадоліній | 0,02-0,04 | <<0,01 | <<0,01 |
| Тербій | 0,003-0,006 | <<0,001 | <<0,001 |
| Самарій | 0,05-0,01 | <<0,0001 | <<0,0001 |
| Неодим | 0,1-0,2 | <<0,01 | <<0,01 |
| Празеодим | 0,05-0,1 | <<0,001 | <<0,001 |
| Церій | 0,3-0,6 | <<0,01 | <<0,01 |
| Лантан | 0,01 | <<0,001 | <<0,001 |
| Нікель | 2,3 | - | <1 |
| Кадмій | 3,5 | <<0,01 | 0,02-0,07 |
| Цинк | 20 | <<0,05 | 1 |
| Кобальт | 0,01 | <<0,01 | <<0,01 |
| Натрій | 1-2 | <0,2 | <0,2 |
| Калій | 0,05 | 0,01 | 0,01 |
| Барій | 6 | - | - |
| Хлор | 0,01 | <0,01 | <0,01 |
| Фосфор | 3 | 0,04 | - |
| Сірка | 15 | 0,5-1,5 | - |
| Вуглець | 1-2 | - | 1-2 |
| Примітка. Кількості телуру, вісмуту, срібла, молібдену, хрому, цирконію, кальцію, стронцію, рубідії, церію, індії, селену та ртуті в алюмінії після зонної плавки нижче чутливості радіоактивного аналізу. | |||
У табл. 1.5 (див. нижче) наведено результати мас-спектрального аналізу та вимірювання R 293 К/ R 4,2 До алюмінію, отриманого каскадною зонною плавкою. З наведених даних можна зробити висновок, що чистота такого алюмінію, визначена по різниці з десятьма основними домішками (Si, Fe, Mg, Mn, Ti, Cu, Cr, Zn, Na і V), становить >99,9999%. Цей висновок побічно підтверджується величиною R 293 К/ R 4,2 До, яка у всіх зразках становила >30?10 3 .
Для отримання металу чистотою 99,9999% достатньо провести два каскади зонної плавки (див. табл. 1.5). Подальше збільшення числа каскадів не підвищує чистоту алюмінію, хоч і збільшує загальний вихід металу чистотою 99,9999%.
Іншим можливим процесом отримання алюмінію особливої чистоти є його дистиляція через субгалогениды, зокрема через субфторид алюмінію.
Тиск насиченої пари металевого алюмінію недостатньо високо, щоб здійснити його безпосередню дистиляцію з практично прийнятними швидкостями. Однак при нагріванні у вакуумі (при 1000-1050°С) з AlF 3 алюміній утворює легколетючий субфторид AlF, який переганяється в холодну зону (800°С), де знову розпадається (диспропорціонує) з виділенням чистого алюмінію:
Можливість глибокого очищення алюмінію від домішки в основному зумовлена тим, що ймовірність утворення субсполучень алюмінію значно більша за ймовірність утворення субз'єднань домішки.
ТАБЛИЦЯ 1.5
РЕЗУЛЬТАТИ МАС-СПЕКТРАЛЬНОГО АНАЛІЗУ ТА ВИМІРЮВАНЬ R 293 К/ R 4,2 ДО АЛЮМІНІЮ КАСКАДНОЇ ЗОННОЇ ПЛАВКИ.
| Число каскадів | Вміст домішок ×10 –4 % | ||||||
| Si | Fe | Mg | Mn | Ti | сума | ||
| Початковий | 18,3 | 0,210 | <0,103 | 0,89 | <0,061 | 0,069 | 1,544 |
| A999 | |||||||
| 2 | 36,5 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 38,0 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 39,5 | 0,073 | <0,103 | 0,045 | <0,061 | 0,07 | 0,563 |
| 3 | 32,0 | 0,204 | <0,103 | 0,006 | <0,061 | 0,017 | 0,502 |
| 3 | 30,0 | 0,073 | 0,100 | 0,006 | 0,020 | 0,07 | 0,480 |
| 3 | 32,0 | 0,052 | 0,100 | 0,006 | 0,061 | 0,07 | 0,500 |
| 4 | 40,0 | <0,021 | <0,103 | 0,006 | 0,061 | 0,07 | 0,472 |
| 4 | 30,5 | 0,031 | 0,100 | 0,006 | 0,061 | 0,07 | 0,479 |
| 5 | 34,0 | 0,104 | <0,060 | 0,006 | 0,061 | 0,017 | 0,459 |
| Примітки: 1. Сума домішок дана з урахуванням інших домішок, вміст яких у всіх зразках становив ×10 –4 %:<0,071 Cu; <0,038 Cr; 0,048 Zn; 0,017 Na; 0,037 V. 2. При подсчете суммы примесей принимали их максимальное значение, равное пределу чувствительности анализа, например <0,061 считали как 0,061. | |||||||
Вміст домішок в алюмінії, дистильованому через субфторид, знаходиться у зворотній залежності від маси одержуваних злитків. У зливках масою 1,5-1,7 кг сумарний вміст домішок (Si, Fe, Cu, Mg) становить 11 10 –4 %, а вміст газів 0,007 см 3 /100 г. Питомий залишковий опір (ρ ○) при температурі рідкого гелію для такого металу становить (1,7÷2,0) 10 –10 Омּсм. Дистиляція алюмінію через субфторид має ряд недоліків (порівняно невелика продуктивність, недостатньо глибока очищення від магнію та ін), тому спосіб не отримав промислового розвитку.
Розроблено також способи отримання алюмінію особливої чистоти електролізом комплексних алюмінійорганічних сполук, що відрізняються складом електроліту. Наприклад, ФРН застосовують спосіб електролізу 50%-ного розчину NaFּ2Al (C 2 H 5) 3 в толуолі. Рафінування проводять при 100°З напрузі на електролізері 1,0-1,5 і щільності струму 0,3-0,5 А/дм 2 з використанням алюмінієвих електродів. Катодний вихід струмом 99%. Електрохімічним рафінуванням в алюмінійорганічних електролітах істотно знижується вміст марганцю та скандію, які практично не видаляються при зонному очищенні. Недоліками зазначеного способу є його низька продуктивність та висока пожежна небезпека.
Для більш глибокого очищення алюмінію та отримання металу чистотою 99,99999% і більше можна використовувати комбінування зазначених вище способів: електроліз алюмінійорганічних сполук або сублімацію через субфторид з наступною зонною плавкою отриманого алюмінію. Наприклад, багаторазовим зонним очищенням алюмінію, отриманого електролізом алюмінійорганічних сполук, вдається отримати метал особливої чистоти з вмістом домішок, ×10 –9 %: Fe 50; Si<500; Cu 10; Mg 30; Mn5; Ti <500; Cr 20; Zn <50; Co <1; Ag <5; Sb <1 и Se 3.
Застосування
Поєднання фізичних, механічних та хімічних властивостей алюмінію визначає його широке застосування практично у всіх галузях техніки, особливо у вигляді його сплавів з іншими металами. У електротехніці алюміній успішно замінює мідь, особливо у виробництві масивних провідників, наприклад, у повітряних лініях, високовольтних кабелях, шинах розподільчих пристроїв, трансформаторах (електрична провідність алюмінію досягає 65,5% електричної провідності міді, і він більш ніж утричі легший за мідь; при поперечному перерізі, що забезпечує одну і ту ж провідність, маса проводів з алюмінію вдвічі менша від мідних). Надчистий алюміній використовують у виробництві електричних конденсаторів і випрямлячів, дія яких заснована на можливості окисної плівки алюмінію пропускати електричний струм лише в одному напрямку. Надчистий алюміній, очищений зонною плавкою, застосовується для синтезу напівпровідникових сполук типу A III B V, що застосовуються для виробництва напівпровідникових приладів. Чистий алюміній використовують у виробництві різноманітних дзеркал відбивачів. Алюміній високої чистоти застосовують для запобігання металевим поверхням від дії атмосферної корозії (плакування, алюмінієва фарба). Маючи відносно низький переріз поглинання нейтронів, алюміній застосовується як конструкційний матеріал у ядерних реакторах.
В алюмінієвих резервуарах великої ємності зберігають і транспортують рідкі гази (метан, кисень, водень тощо), азотну та оцтову кислоти, чисту воду, перекис водню та харчові олії. Алюміній широко застосовують і в обладнанні та апаратах харчової промисловості, для пакування харчових продуктів (у вигляді фольги), для виробництва різного роду побутових виробів. Різко зросло споживання алюмінію для оздоблення будівель, архітектурних, транспортних та спортивних споруд.
У металургії алюміній (крім сплавів на його основі) – одна з найпоширеніших легуючих добавок у сплавах на основі Cu, Mg, Ti, Ni, Zn та Fe. Застосовують алюміній також для розкислення сталі перед заливанням її у форму, а також у процесах отримання деяких металів шляхом алюмінію. На основі алюмінію методом порошкової металургії створено САП (спечений алюмінієвий порошок), що має при температурах вище 300°С великою жароміцністю.
Алюміній використовують у виробництві вибухових речовин (амонал, алюмотол). Широко застосовують різні сполуки алюмінію.
Виробництво та споживання алюмінію безперервно зростає, значно випереджаючи за темпами зростання виробництво сталі, міді, свинцю, цинку.
DIN (DeutschIndustrienorm) – промисловий стандарт ФРН.
Одна вельми сумнівна легенда розповідає, що одного разу до римського імператора Тиберія (42 р. до н. е. - 37 р. н. е.) прийшла людина з металевою чашею, що не б'ється. Матеріал чаші нібито був отриманий з глинозему (Al 2 O 3) і, отже, повинен був являти собою алюміній. Побоюючись, що такий метал із глини може знецінити золото та срібло, Тіберій про всяк випадок наказав відрубати людині голову. Зрозуміло, цій розповіді важко повірити: самородний алюміній у природі не зустрічається, а за часів Римської імперії не могло бути технічних засобів, які б витягти алюміній з його сполук.
За поширеністю у природі алюміній посідає перше місце серед металів; його вміст у земній корі становить 7,45%. Однак, незважаючи на широку поширеність у природі, алюміній до кінця XIX століття належав до рідкісних металів. У чистому вигляді алюміній не зустрічається через свою високу хімічну активність. Він переважно зустрічається у вигляді сполук із киснем та кремнієм – алюмосилікатів.
Рудами алюмінію можуть служити лише породи, багаті на глинозем (Al 2 O 3) і залягають великими масами на поверхні землі. До таких пород відносяться боксити, нефеліни - (Na, K) 2 O ? шпат (ортоклаз) - K 2 OּAl 2 O 3 6SiO 2 .
Основною рудою для отримання алюмінію є боксити. Алюміній в них міститься у вигляді гідроксиду Al(OH), AlOOH, корунду Al 2 O 3 і каолініту Al 2 O 3 2SiO 2 2H 2 O. Хімічний склад бокситів складний: 28-70% глинозему; 0,5-20% кремнезему; 2-50% окису заліза; 0,1-10% окису титану. Останнім часом як руду стали застосовувати нефеліни та алуніти.
Великі родовища бокситів перебувають на Уралі, в Тихвінському районі Ленінградської області, Алтайському і Красноярському краях.
Нефелін входить до складу апатитонефелінових порід (на Кольському півострові).
Вперше у вільному вигляді алюміній був виділений 1825 р. датським фізиком Ерстедом шляхом впливу амальгами калію на хлорид алюмінію. У 1827р. німецький хімік Велер удосконалив спосіб Ерстеда, замінивши амальгаму калію металевим калієм.
AlCl 3 + 3K→3KCl + Al (Реакція протікає із виділенням тепла).
У 1854 р. Сент-Клер Девіль у Франції вперше застосував спосіб Велера для промислового виробництва алюмінію, використавши замість калію більш дешевий натрій, а замість гігроскопічного хлориду алюмінію - стійкіший подвійний хлорид алюмінію та натрію. У 1865 р. російський фізико-хімік Н. Н. Бекетов показав можливість витіснення алюмінію магнієм із розплавленого кріоліту. Ця реакція у 1888 р. була використана для виробництва алюмінію на першому німецькому заводі у Гмелінгені. Виробництво алюмінію цими так званими «хімічними» способами здійснювалося з 1854 по 1890 р. Протягом 35 років за допомогою цих способів, було отримано загалом близько 20 т алюмінію.
Наприкінці 80-х років позаминулого століття хімічні методи витіснив електролітичний метод, який дозволив різко знизити вартість алюмінію і створив передумови швидкого розвитку алюмінієвої промисловості. Основоположники сучасного електролітичного способу виробництва алюмінію Еру у Франції та Холл у США незалежно один від одного подали в 1886 майже аналогічні заявки на патентування способу отримання алюмінію електролізом глинозему, розчиненого в розплавленому кріоліті. З моменту появи патентів Еру і Холла і починається сучасна алюмінієва промисловість, яка за 115 років свого існування виросла в одну з найбільших галузей металургії.
Технологічний процес отримання алюмінію складається із трьох основних стадій:
1). Одержання глинозему (Al2O3) з алюмінієвих руд;
2). Одержання алюмінію із глинозему;
3). Рафінування алюмінію.
Отримання глинозему із руд.
Глинозем одержують трьома способами: лужним, кислотним та електролітичним. Найбільше поширення має лужний спосіб (метод К. І. Байєра, розроблений в Росії наприкінці позаминулого століття і застосовується для переробки високосортних бокситів з невеликою кількістю (до 5-6%) кремнезему). З того часу технічне виконання його було суттєво покращено. Схема виробництва глинозему за способом Байєра представлена на рис. 1.
Сутність способу полягає в тому, що алюмінієві розчини швидко розкладаються при введенні в них гідроксиду алюмінію, а розчин, що залишився, після його випарювання в умовах інтенсивного перемішування при 169-170 про С може знову розчиняти глинозем, що міститься в бокситах. Цей спосіб складається з наступних основних операцій:
1). Підготовка бокситу, що полягає в його дробленні та подрібненні в млинах; в млина подають боксит, їдкий луг і невелику кількість вапна, яке покращує виділення Al 2 O 3 ; отриману пульпу подають на вилуговування;
2). Вилужування бокситу (останнім часом застосовувані досі блоки автоклав круглої форми частково замінені трубчастими автоклавами, в яких при температурах 230-250°С (500-520 К) відбувається вилуговування), що полягає в його хімічному розкладанні від взаємодії з водним розчином лугу; гідрати окису алюмінію при взаємодії зі лугом переходять у розчин у вигляді алюмінію натрію:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH) 3 +NaOH→NaAlO 2 +2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H 2 O;
у розчині алюмінат натрію та силікат натрію утворюють нерозчинний натрієвий алюмосилікат; у нерозчинний залишок переходять окисли титану і заліза, що надають залишку червоного кольору; цей залишок називають червоним шламом. Після закінчення розчинення отриманий алюмінат натрію розбавляють водним розчином лугу при одночасному зниженні температури на 100°З;
3). Відділення алюмінатного розчину від червоного шламу зазвичай здійснюється шляхом промивання у спеціальних згущувачах; внаслідок цього червоний шлам осідає, а алюмінійний розчин зливають і потім фільтрують (освітлюють). В обмежених кількостях шлам знаходить застосування, наприклад як добавка до цементу. Залежно від сорту бокситів на 1 т одержаного окису алюмінію припадає 0,6-1,0 т червоного шламу (сухого залишку);
4). Розкладання алюмінатного розчину. Його фільтрують та перекачують у великі ємності з мішалками (декомпозери). З пересиченого розчину при охолодженні на 60°С (330 До) і постійному перемішуванні витягується гідроксид алюмінію Al(OH) 3 . Так як цей процес протікає повільно і нерівномірно, а формування і зростання кристалів гідроксиду алюмінію мають велике значення при її подальшій обробці, декомпозери додають велику кількість твердого гідроксиду - затравки:
Na 2 OּAl 2 O 3 +4H 2 O→Al(OH) 3 +2NaOH;
5). Виділення гідроксиду алюмінію та його класифікації; це відбувається у гідроциклонах та вакуум-фільтрах, де від алюмінатного розчину виділяють осад, що містить 50-60% частинок Al(OH). Значну частину гідроокису повертають у процес декомпозиції як затравний матеріал, яка залишається в обороті в незмінних кількостях. Залишок після промивання водою йде кальцинацію; фільтрат також повертається в оборот (після концентрації у випарних апаратах - для вилуговування нових бокситів);
6). Зневоднення гідроксиду алюмінію (кальцинації); це завершальна операція виробництва глинозему; її здійснюють у трубчастих обертових печах, а останнім часом також у печах з турбулентним рухом матеріалу при температурі 1150-1300 про З; сирий гідроксид алюмінію, проходячи через піч, що обертається, висушується і зневоднюється; при нагріванні відбуваються послідовно такі структурні перетворення:
| Al(OH) 3 →AlOOH→ γ-Al 2 O 3 → α-Al 2 O 3 |
|||
В остаточно прожареному глиноземі міститься 30-50% -Al 2 O 3 (корунд), решта -Al 2 O 3 .
Цим способом витягується 85-87% від всього одержуваного глинозему. Отриманий окис алюмінію являє собою міцну хімічну сполуку з температурою плавлення 2050 про С.
Одержання алюмінію з його окису
Електроліз окису алюмінію
 Електролітичне відновлення окису алюмінію, розчиненого в розплаві на основі кріоліту, здійснюється за 950-970°С в електролізері. Електролізер складається з футерованої вуглецевими блоками ванни, до подіни якої підводиться електричний струм. Рідкий алюміній, що виділився на подині, що служить катодом, важчий за розплав солі електроліту, тому збирається на вугільній підставі, звідки його періодично відкачують (рис. 2). Зверху в електроліт занурені вугільні аноди, які згоряють в атмосфері кисню, що виділяється з окису алюмінію, виділяючи окис вуглецю (CO) або двоокис вуглецю (CO 2). На практиці знаходять застосування два типи анодів:
Електролітичне відновлення окису алюмінію, розчиненого в розплаві на основі кріоліту, здійснюється за 950-970°С в електролізері. Електролізер складається з футерованої вуглецевими блоками ванни, до подіни якої підводиться електричний струм. Рідкий алюміній, що виділився на подині, що служить катодом, важчий за розплав солі електроліту, тому збирається на вугільній підставі, звідки його періодично відкачують (рис. 2). Зверху в електроліт занурені вугільні аноди, які згоряють в атмосфері кисню, що виділяється з окису алюмінію, виділяючи окис вуглецю (CO) або двоокис вуглецю (CO 2). На практиці знаходять застосування два типи анодів:
а) самопалюючі аноди Зедерберга, що складаються з брикетів, так званих «хлібів» маси Зедерберга (малозолильне вугілля з 25-35% кам'яновугільного пеку), набитих в алюмінієву оболонку; під дією високої температури анодна маса випалюється (спікається);
б) обпалені, або «безперервні», аноди з великих вугільних блоків (наприклад, 1900 600 500 мм масою близько 1,1 т).
Сила струму на електролізерах становить 150 000 А. Вони входять у мережу послідовно, т. е. виходить система (серія) - довгий ряд електролізерів.
Робоча напруга на ванні, що становить 4-5, значно вище напруги, при якому відбувається розкладання окису алюмінію, оскільки в процесі роботи неминучі втрати напруги в різних частинах системи. Баланс сировини та енергії при отриманні 1 т алюмінію представлений на рис. 3.
Електроліз хлориду алюмінію (метод фірми Алкоа)
 У реакційній посудині окис алюмінію перетворюється спочатку на хлорид алюмінію. Потім у щільно ізольованій ванні відбувається електроліз AlCl 3 розчиненого в розплаві солей KCl, NaCl. Хлор, що виділяється при цьому, відсмоктується і подається для вторинного використання; алюміній осідає на катоді.
У реакційній посудині окис алюмінію перетворюється спочатку на хлорид алюмінію. Потім у щільно ізольованій ванні відбувається електроліз AlCl 3 розчиненого в розплаві солей KCl, NaCl. Хлор, що виділяється при цьому, відсмоктується і подається для вторинного використання; алюміній осідає на катоді.
Перевагами даного методу перед існуючим електролізом рідкого кріолітоглиноземного розплаву (Al 2 O 3 розчинена в кріоліті Na 3 AlF 6) вважають: економію до 30% енергії; можливість застосування окису алюмінію, який не підходить для традиційного електролізу (наприклад, Al 2 O 3 з високим вмістом кремнію); заміну дорогого кріоліту дешевшими солями; зникнення небезпеки виділення фтору.
Відновлення хлориду алюмінію марганцем (Toth – метод)
 При відновленні марганцем із хлориду алюмінію звільняється алюміній. Через керовану конденсацію з потоку хлориду марганцю виділяються пов'язані з хлором забруднення. При звільненні хлору хлорид марганцю окислюється в окис марганцю, який відновлюється до марганцю, придатного до вторинного застосування. Відомості в наявних публікаціях дуже неточні, тож у разі доведеться відмовитися від оцінки методу.
При відновленні марганцем із хлориду алюмінію звільняється алюміній. Через керовану конденсацію з потоку хлориду марганцю виділяються пов'язані з хлором забруднення. При звільненні хлору хлорид марганцю окислюється в окис марганцю, який відновлюється до марганцю, придатного до вторинного застосування. Відомості в наявних публікаціях дуже неточні, тож у разі доведеться відмовитися від оцінки методу.
Отримання рафінованого алюмінію
Для алюмінію рафінуючий електроліз з розкладанням сольових водних розчинів неможливий. Оскільки для деяких цілей ступінь очищення промислового алюмінію (Al 99,5 - Al 99,8), отриманого електролізом криолитоглиноземного розплаву, недостатня, з промислового алюмінію або відходів металу шляхом рафінування отримують ще чистіший алюміній (Al 99, 99 R). Найбільш відомий метод рафінування – тришаровий електроліз.
Рафінування методом тришарового електролізу
Одягнена сталевим листом, що працює на постійному струмі (представлена на рис. 4 - див. вище) ванна для рафінування складається з вугільної подини з струмопідведення і теплоізолюючої магнезитової футеровки. На противагу електролізу кріолітоглиноземного розплаву анодом тут служить, як правило, розплавлений рафінований метал (нижній анодний шар). Електроліт складається з чистих фторидів або суміші хлориду барію та фторидів алюмінію та натрію (середній шар). Алюміній, що розчиняється з анодного шару електроліті, виділяється над електролітом (верхній катодний шар). Чистий метал є катодом. Підведення струму до катодного шару здійснюється графітовим електродом.
Ванна працює при 750-800°С, витрата електроенергії становить 20 кВт на 1 кг чистого алюмінію, тобто дещо вище, ніж при звичайному електролізі алюмінію.
Метал анода містить 25-35% Cu; 7-12% Zn; 6-9% Si; до 5% Fe та незначна кількість марганцю, нікелю, свинцю та олова, решта (40-55%) – алюміній. Усі важкі метали та кремній при рафінуванні залишаються в анодному шарі. Наявність магнію в електроліті призводить до небажаних змін складу електроліту або сильного його ошлакування. Для очищення магнію шлаки, що містять магній, обробляють флюсами або газоподібним хлором.
В результаті рафінування отримують чистий алюміній (99,99%) та продукти сегрегації (зайгер-продукт), які містять важкі метали та кремній та виділяються у вигляді лужного розчину та кристалічного залишку. Лужний розчин є відходом, а твердий залишок застосовується для розкислення.
Рафінований алюміній зазвичай має наступний склад, %: Fe 0,0005-0,002; Si 0,002-0,005; Cu 0,0005-0,002; Zn 0,0005-0,002; Mg сліди; Al інше.
Рафінований алюміній переробляють на напівфабрикат у зазначеному складі або легують магнієм (див. табл. 1.2).
ТАБЛИЦЯ 1.2. Хімічний склад алюмінію підвищеної чистоти та первинного алюмінію DIN 17122, лист 1.
| Допустимі домішки* , % | |||||||||
| в тому числі |
|||||||||
| A199,99R | 3.0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 | |
| A199,9H | 3.0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 | |
| A199,8H | 3.0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,7H | 3.0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,5H** | 3.0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 | |
| A199H | 3.0200 | 1,0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 | |
| * Наскільки можливо визначити звичайними методами дослідження. ** Чистий алюміній для електротехніки (алюмінієві провідники) постачають у вигляді первинного алюмінію 99,5, що містить не більше 0,03% (Ti+Cr+V+Mn); позначається у разі E-A1, номер матеріалу 3.0256. В іншому відповідає нормам VDE-0202. |
|||||||||
Рафінування шляхом алюмоорганічних комплексних сполук та зонною плавкою
Алюміній ступеня чистоти вище марки A1 99,99 R може бути отриманий рафінуючим електролізом чистого або технічно чистого алюмінію із застосуванням електроліту комплексних алюмоорганічних сполук алюмінію. Електроліз проходить при температурі близько 1000°С між твердими алюмінієвими електродами і в принципі схожий на рафінуючий електроліз міді. Природа електроліту диктує необхідність працювати без доступу повітря та за низької щільності струму.
Цей вид рафінуючого електролізу, що застосовується спочатку лише в лабораторному масштабі, вже здійснюється у невеликому виробничому масштабі – виготовляється кілька тонн металу на рік. Номінальний ступінь очищення одержуваного металу 99,999-99,9999%. Потенційними областями застосування металу такої чистоти є кріогенна електротехніка та електроніка.
Можливе застосування розглянутого методу рафінування та в гальванотехніці.
Ще більш високу чистоту – номінально до A1 99,99999 – можна отримати наступною зонною плавкою металу. При переробці алюмінію підвищеної чистоти на напівфабрикат, лист або дріт необхідно, враховуючи низьку температуру рекристалізації металу, вживати особливих запобіжних заходів. Примітною властивістю рафінованого металу є його висока електропровідність у сфері кріогенних температур.
Отримання вторинного алюмінію
Переробка вторинної сировини та відходів виробництва є економічно вигідною. При цьому вторинними сплавами задовольняється близько 25% загальної потреби в алюмінії.
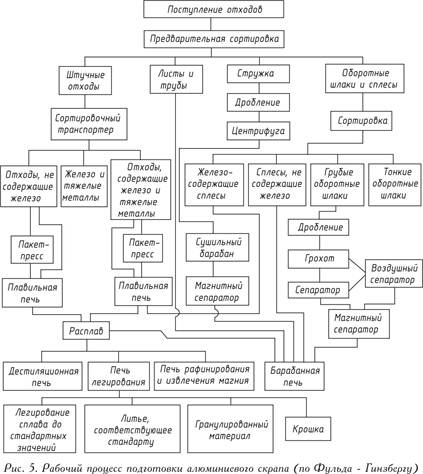 Найважливішою сферою застосування вторинних сплавів є виробництво фасонного алюмінієвого лиття. У DIN 1725 лист 2 поряд зі стандартними марками сплавів наведені численні марки сплавів, що виробляються ливарними заводами. Перелік сплавів, які випускаються цими заводами, містить, крім стандартних, деякі нестандартні сплави.
Найважливішою сферою застосування вторинних сплавів є виробництво фасонного алюмінієвого лиття. У DIN 1725 лист 2 поряд зі стандартними марками сплавів наведені численні марки сплавів, що виробляються ливарними заводами. Перелік сплавів, які випускаються цими заводами, містить, крім стандартних, деякі нестандартні сплави.
Бездоганне приготування алюмінієвого скрапу у найрізноманітніших пропорціях можна здійснювати лише спеціально обладнаних плавильних заводах. Уявлення про складний робочий процес на такому заводі дає рис. 5.
Відходи переплавляють після грубого попереднього сортування. Залізо, нікель або мідь, що містяться в цих відходах, точка плавлення яких вище точки плавлення алюмінію, при плавці в плавильній пороговій печі залишаються в ній, а алюміній виплавляється. Для видалення з відходів неметалевих включень типу оксидів, нітридів, карбідів або газів застосовують обробку розплавленого металу солями або (що раціональніше) продування газом - хлором або азотом.
Для видалення металевих домішок з розплаву відомі різні методи, наприклад, присадка магнію і вакуумування - метод Бекша (Becksche); присадка цинку або ртуті з наступним вакуумуванням - субгалогенний метод. Видалення магнію обмежується введенням у розплавлений метал хлору. Шляхом введення добавок, що точно визначаються складом розплаву, отримують заданий ливарний сплав.
Виробництво алюмінію технічної чистоти
Електролітичний спосіб - єдиний застосовується у всьому світі для виробництва металевого алюмінію технічної чистоти. Всі інші способи (цинкотермічний, карбідотермічний, субхлоридний, нітридний та ін), за допомогою яких алюміній може бути вилучений з алюмінієвих руд, розроблялися в лабораторному та дослідно-промислових масштабах, проте поки не знайшли практичного застосування.
Для отримання алюмінієво-кремнієвих сплавів успішно застосовується електротермічний спосіб, вперше розроблений та здійснений у промисловому масштабі у СРСР. Він складається з двох стадій: на першій стадії одержують первинний алюмінієво-кремнієвий сплав із вмістом 60-63 % Al шляхом прямого відновлення алюмо-кремнистих руд у рудно-термічних електричних печах; на другій стадії первинний сплав розбавляють технічним алюмінієм, отримуючи силумін та інші ливарні та деформовані алюмінієво-кремнієві сплави. Ведуться дослідження щодо вилучення з первинного сплаву алюмінію технічної чистоти.
В цілому одержання алюмінію електролітичним способом включає виробництво глинозему (окису алюмінію) з алюмінієвих руд, виробництво фтористих солей (кріоліту, фтористого алюмінію і фтористого натрію), виробництво вуглецевої анодної маси, обпалених вугільних анодних і катодних блоків. власне електролітичне виробництво алюмінію, яке є завершальним етапом сучасної металургії алюмінію.
Характерним для виробництва глинозему, фтористих солей та вуглецевих виробів є вимога максимального ступеня чистоти цих матеріалів, оскільки в кріолітоглиноземних розплавах, що піддаються електролізу, не повинні утримуватися домішки елементів, більш електропозитивних, ніж алюміній, які, виділяючись на катоді в першу чергу, забруднювали б метал.
У глиноземі марок Г-00, Г-0 та Г-1, які переважно використовуються при електролізі, вміст SiO 2 становить 0,02-0,05%, a Fe 2 O 3 - 0,03-0,05%. У кріоліті в середньому міститься 0,36-0,38% SiO 2 і 0,05-0,06% Fe 2 O 3 у фтористому алюмінію 0,30-0,35% (SiO 2 + Fe 2 O 3). В анодній масі міститься не більше 0,25% SiO2 і 0,20% Fe2O3.
Найважливіша алюмінієва руда, з якої витягають глинозем, боксит. У бокситі алюміній присутній у формі гідроксиду алюмінію. У Радянському Союзі, крім бокситу, для одержання глинозему застосовують нефелінову породу - алюмосилікат натрію та калію, а також алунітову породу, в якій алюміній знаходиться у вигляді його сульфату. Сировиною для виготовлення анодної маси та обпалених анодних блоків служать вуглецеві чисті матеріали - нафтовий або печовий кокс і кам'яновугільний печ як сполучний, а для виробництва кріоліту та інших фтористих солей - фтористий кальцій (плавиковий шпат).
При електролітичному отриманні алюмінію глинозему Al 2 O 3 розчинений в розплавленому кріоліті Na 3 AlF 6 електрохімічно розкладається з розрядом катіонів алюмінію на катоді (рідкому алюмінії), а кисневмісних іонів (іонів кисню) - на вуглецю.
За сучасними уявленнями, кріоліт у розплавленому стані дисоціює на іони та : , а глинозем - на комплексні іони та : ![]() , які перебувають у рівновазі з простими іонами:
, які перебувають у рівновазі з простими іонами: ![]() ,
, ![]() .
.
Основним процесом, що відбувається на катоді є відновлення іонів тривалентного алюмінію: Al 3+ + 3e → Al (I).
Поруч із основним процесом можливий неповний розряд тривалентних іонів алюмінію із заснуванням одновалентних іонів: Al 3+ + 2e → Al + (II) і, нарешті, розряд одновалентних іонів із виділенням металу: Al + + e → Al (III).
За певних умов (щодо великої концентрації іонів Na + , висока температура та ін.) може відбуватися розряд іонів натрію з виділенням металу: Na + + e → Na (IV). Реакції (II) та (IV) обумовлюють зниження виходу алюмінію струмом.
На вугільному аноді відбувається розряд іонів кисню: 2O 2– – 4e → O 2 . Однак кисень не виділяється у вільному вигляді, оскільки він окислює вуглець аноду з утворенням суміші CO2 та CO.
Сумарна реакція, що відбувається в електролізері, може бути представлена рівнянням Al 2 O 3 + xC ↔ 2Al + (2x-3)CO + (3-x)CO2.
До складу електроліту промислових алюмінієвих електролізерів, крім основних компонентів - кріоліту, фтористого алюмінію та глинозему, входять невеликі кількості (у сумі до 8-9%) деяких інших солей - CaF 2 , MgF 2 , NaCl і LiF (добавки), які покращують деякі фізико-хімічні властивості електроліту і цим підвищують ефективність роботи електролізерів. Максимальний вміст глинозему в електроліті зазвичай становить 6-8%, знижуючись в процесі електролізу. У міру збіднення електроліту глиноземом до нього вводять чергову порцію глинозему. Для нормальної роботи алюмінієвих електролізерів відношення NaF: AlF 3 в електроліті підтримують у межах 2,7-2,8, додаючи порції кріоліту та фтористого алюмінію.
У виробництві алюмінію застосовують електролізери з вугільними анодами, що самообпалюються, і бічним або верхнім підведенням струму, а також електролізери з попередньо обпаленими вугільними анодами. Найбільш перспективною є конструкція електролізерів з обпаленими анодами, що дозволяє збільшити одиничну потужність агрегату, знизити питому витрату електроенергії постійного струму на електроліз, отримати більш чистий метал, покращити санітарно-гігієнічні умови праці та зменшити викиди шкідливих речовин в атмосферу.
Основні технічні параметри та показники роботи алюмінієвих електролізерів різного типу наведені у табл. 1.3.
ТАБЛИЦЯ 1.3
ОСНОВНІ ТЕХНІЧНІ ПАРАМЕТРИ І ПОКАЗНИКИ РОБОТИ АЛЮМІНІЄВИХ ЕЛЕКТРОЛІЗЕРІВ
| Параметри та показники | З анодами, що самопалюються. | З обпаленими анодами |
|
| струмопідведення | верхній струмопідвід |
||
| Сила струму, як | 60-120 | 60-155 | 160-255 |
| Добова продуктивність електролізера, т | 0,42-0,85 | 0,40-1,10 | 1,10-1,74 |
| Анодна щільність струму, А/см 2 | 0,80-0,90 | 0,65-0,70 | 0,70-0,89 |
| Середня напруга на електролізері, | 4,45-4,65 | 4,50-4,70 | 4,30-4,50 |
| Вихід за струмом, % | 85-88 | 84-86 | 85-89 |
| Витратні коефіцієнти на 1 т алюмінію: | |||
| електроенергії постійного струму, кВт | 15100-16200 | 15500-17300 | 14500-15500 |
| глинозему, кг | 1920-1940 | 1920-1940 | 1920-1940 |
| анодної маси, кг | 520-560 | 560-620 | - |
| обпалених анодів, кг | - | - | 540-600 |
| Фтористих солей у перерахунку на фтор, кг | 20-30 | 25-35 | 15-25 |
Первинний алюміній, що витягується з електролізерів (алюміній-сирець), містить ряд домішок, які можна поділити на три групи: неметалеві (фтористі солі, α- і γ-глинозем, карбід і нітрид алюмінію, вугільні частинки, що механічно захоплюються при виливці металу ); металеві (залізо, кремній), що переходять із сировини, вугільних матеріалів та конструктивних елементів електролізера; газоподібні - переважно водень, що утворюється в металі внаслідок електролітичного розкладання води, що потрапляє в електроліт із сировиною.
З металевих домішок, окрім заліза та кремнію, міститься найбільша кількість галію, цинку, титану, марганцю, натрію, ванадію, хрому, міді. Вміст цих та деяких інших металевих мікродомішок в електролітичному алюмінії наведено нижче, %:
| Середній зміст | 0,0025 | 0,003 | 0,0025 | 0,004 | 0,002 | 0,007 |
| Межі зміни | 0,001-0,008 | 0,001-0,006 | 0,001-0,008 | 0,002-0,008 | 0,001-0,008 | 0,002-0,014 |
| Середній зміст | <0,002 | 0,0002 | 0,001 | 0,0005 | 0,008 | 0,004 |
| Межі зміни | <0,001-0,004 | 0,0001-0,0003 | 0,001-0,0024 | 0,0001-0,0009 | 0,004-0,012 | 0,002-0,008 |
Основним джерелом надходження металевих мікродомішок до алюмінію є глинозем, який залежно від виду вихідної сировини може містити галій, цинк, калій, фосфор, сірку, ванадій, титан і хром. Вуглецеві матеріали (анодна маса, обпалені аноди, катодні вироби) є джерелом таких мікродомішок, як, наприклад, ванадій, титан, марганець, цинк.
Електролізом кріоліто-глиноземних розплавів за умови застосування чистих вихідних матеріалів (насамперед глинозему та вуглецевих матеріалів) вдається отримати алюміній-сирець марок А85 та А8 (99,85 та 99,80%). Найбільша частка металу цих марок (60-70% від загального випуску) виходить на електролізер з обпаленими анодами, а також на електролізер з бічним підведенням струму (до 70% від загального виробництва). На електролізерах з самопальними анодами і верхнім струмопідведенням випуск алюмінію-сирцю марки А8 невисокий (становить 1-3%), а метал марки А85 отримати не вдається через значні домішки заліза, що надходить в алюміній з несировинних джерел (анодні , Технологічний інструмент, катодний вузол).
Розплавлений первинний алюміній, витягнутий з електролізерів за допомогою вакуумного ковша, надходить у ливарне відділення для рафінування від неметалевих та газових домішок та подальшої переробки в товарну продукцію (чушки, циліндричні та плоскі зливки, катанку тощо). Перед розливанням алюміній-сирець витримують у розплавленому стані в електричних печах опору (міксерах) або газових відбивних печах. У цих печах не тільки проводять раціональну шихтовку різних за складом порцій рідкого алюмінію, а й частково очищають від неметалевих включень, плівок окисних і натрію.
Розлив алюмінію з міксера в чушки проводиться за допомогою ливарних машин конвеєрного типу; циліндричні та плоскі зливки виготовляють методом напівбезперервного лиття, а для отримання катанки застосовують спеціальні агрегати поєднаного лиття та прокатки.
На вітчизняних алюмінієвих заводах при литті злитків алюміній, що надходить з міксера в кристалізатор ливарної машини, піддають найпростішому виду рафінування - фільтрації розплаву через склосітку з осередками розміром від 0,6×0,6 до 1,7×1,7 мм. Цей метод дозволяє очищати алюміній лише від дуже грубих окисних включень; Найбільш досконалий спосіб фільтрації розплаву через склосітку у висхідному потоці. При такому способі фільтрування частинки окисних включень, зіштовхуючись із сіткою, не захоплюються потоком розплаву, а осідають на дні ливарного жолоба.
Для одночасного очищення алюмінію як від неметалевих домішок, так і від водню успішно застосовується метод фільтрації через флюсовий фільтр у поєднанні з продувкою азотом. Як флюс можна використовувати кислий електроліт алюмінієвих електролізерів. В результаті такої очистки вміст водню в алюмінії знижується з 0,22 до 0,16 см 3 на 100 г металу.
У первинному алюмінії, який використовується для виробництва сплавів системи Al-Mg, вміст натрію не повинен перевищувати 0,001%. Це з тим, присутність натрію у цих сплавах погіршує механічні та інші експлуатаційні властивості виробів, застосовуваних у низці галузей народного господарства.
Найбільш ефективним методом одночасного рафінування алюмінію від натрію, водню та неметалічних домішок є продування розплавленого металу газовою сумішшю азоту з 2-10% хлору, що вводиться в розплав у вигляді дрібних бульбашок за допомогою спеціальних пристроїв. Цей спосіб рафінування дозволяє знизити вміст натрію алюмінію до 0,0003-0,001% при витраті газової суміші від 0,8 до 1,5 м 3 /т металу.
Витрата електроенергії на виробництво 1 т товарного алюмінію з металу-сирцю при використанні електропечей становить 150-200 кВт/год; безповоротні втрати металу на ливарному переділі дорівнюють 1,5-5 % залежно від виду товарної продукції.
Одержання алюмінію високої чистоти
Для одержання алюмінію високої чистоти (марок А995-А95) первинний алюміній технічної чистоти електролітично рафінують. Це дозволяє знизити в алюмінії вміст металевих та газоподібних домішок і тим самим значно підвищити його електропровідність, пластичність, відбивну здатність та корозійну стійкість.
Електролітичне рафінування алюмінію здійснюють електролізом розплавлених солей за тришаровим способом. Сутність способу полягає в наступному. У рафінувальному електролізері є три розплавлені шари. Нижній, найважчий, лежить на струмопровідній подіні і служить анодом; він називається анодним сплавом і являє собою сплав алюмінію, що рафінується, з міддю, яку вводять для обтяження шару. Середній шар – розплавлений електроліт; його щільність менша за щільність анодного сплаву і вище за щільність чистого рафінованого (катодного) алюмінію, що знаходиться над електролітом (верхній, третій рідкий шар).
При анодному розчиненні всі домішки електропозитивніші, ніж алюміній (Fe, Si, Ti, Cu та ін), залишаються в анодному сплаві, не переходячи в електроліт. Анодно розчинятися буде лише алюміній, який у формі іонів Al 3+ переходить до електроліту: Al–3e → Al 3+ .
При електролізі іони алюмінію переносяться до катода, на якому розряджаються: Al 3+ + 3e → Al. В результаті на катоді накопичується шар розплавленого рафінованого алюмінію.
Якщо в анодному сплаві присутні домішки електронегативніші, ніж алюміній (наприклад, Ba, Na, Mg, Ca), то вони можуть електрохімічно розчинятися на аноді разом з алюмінієм і у вигляді іонів переходити в електроліт. Оскільки вміст електронегативних домішок в алюмінію-сирці невеликий, у помітній кількості в електроліті вони не накопичуються. Розряду цих іонів на катоді практично не відбувається, так як їхній електродний потенціал електронегативніший за алюміній.
Як електроліт при електролітичному рафінуванні алюмінію в Радянському Союзі та в більшості країн застосовують фторидно-хлоридний електроліт, склад якого 55-60% BaCl 2 , 35-40% AlF 4 +NaF і 0-4% NaCl. Молярне відношення NaF: AlF 3 підтримують 1,5-2,0; температура плавлення електроліту 720-730 ° C; температура процесу електролізу близько 800°C; густина електроліту 2,7 г/см 3 .
Анодний сплав готують із первинного алюмінію та чистої міді (99,90-99,95% Cu), яку вводять у метал у кількості 30-40%. Щільність рідкого анодного сплаву такого складу 3-3,5 г/см 3 ; щільність чистого розплавленого катодного алюмінію дорівнює 2,3 г/см 3 . При такому співвідношенні щільностей створюються умови, необхідні хорошого поділу трьох розплавлених шарів.
У четверній системі Al-Cu-Fe-Si, до якої належить анодний сплав, утворюється евтектика з температурою плавлення 520°C. Охолоджуючи анодний сплав, що містить домішки заліза та кремнію в кількостях вище евтектичних концентрацій, можна виділити залізо та кремній у тверду фазу у вигляді інтерметалевих сполук FeSiAl 5 та Cu 2 FeAl 7 . Так як температура анодного сплаву в кишенях електролізера на 30-40°C нижче за температуру анодного сплаву в робочому просторі ванни, в них (у міру накопичення в анодному сплаві заліза і кремнію) виділятимуться тверді інтерметалічні опади. Періодично видаляючи ці опади, очищають анодний сплав (без оновлення) від домішок заліза і кремнію. Так як в анодному сплаві концентрується галій, то опади, що витягуються з електролізера (30-40 кг на 1 т алюмінію) можуть служити джерелом отримання цього металу.
Для електролітичного рафінування служать електролізери, які за конструкцією нагадують електролізери з обпаленими анодами для електролітичного отримання первинного алюмінію, але мають інше підключення полюсів: подина служить анодом, а верхній ряд електродів - катодом. Сучасні електролізери для електролітичного рафінування алюмінію розраховані на силу струму до 75 кА.
Нижче наведено основні техніко-економічні показники електролізерів за 1979 р., досягнуті вітчизняними (1, 2, 3) підприємствами.
Електрохімічний вихід струму, розрахований по вилитому з електролізера металу, становить 97-98%. Фактичний вихід по струму, розрахований за кількістю товарного металу, становить 92-96%.
| Сила струму, як | 23,5 | 62,9 | 69,8* |
| Середня напруга, | 5,43 | 5,68 | 5,69 |
| Вихід за струмом, % | 95,7 | 93,0 | 92,7 |
| Витрата електроенергії постійного струму, кВт/ч/т | 17 370 | 18 700 | 19 830 |
| Сумарний електроенергії змінного струму, кВт/ч | 18 670 | 19 590 | 20 780 |
| Рівні, см | |||
| катодного алюмінію | 16,6 | 12,9 | 14,6 |
| електроліту | 13,3 | 11,6 | 14,2 |
| анодного сплаву | 40,1 | 29,5 | 30,0 |
| Витратні коефіцієнти, кг/т: |
|||
| хлористий барій | 40,5 | 41,5 | 27,0 |
| 27,7 | 21,0 | 16,5 | |
| фтористий алюміній | 6,7 | 13,1 | 3,8 |
| хлористий натрій | 1,0 | 4,8 | - |
| алюміній-сирець | 1020 | 1028 | 1032 |
| 11,9 | 11,5 | 16,6 | |
| 9,8 | 15,5 | 16,4 | |
| Випуск алюмінію високої чистоти, % марок: |
|||
| 47,8** | 3,5 | 2,1 | |
| 30,4 | 67,1 | 54,2 | |
| 8,3 | 21,5 | 43,7 | |
| 10,4 | 7,9 | - | |
| 3,1 | - | - | |
| * Показники виробництва алюмінію високої чистоти. ** Сортність по електролізерах без розшиття. |
|||
Основним фактором, що знижує вихід по струму, крім прямих втрат струму на розряд електронегативних іонів, втрат металу за рахунок його окислення і механічних втрат алюмінію, є робота електролізерів з випуском несортового металу, який знову повертається в анодний сплав для подальшого рафінування. Ці періоди роботи електролізерів мають місце при пуску електролізерів та порушення технологічного режиму.
Електролітичне рафінування алюмінію є дуже енергоємним виробництвом. Витрата електроенергії в змінному струмі, включаючи енергію, витрачену на підготовку електроліту та анодного сплаву, роботу вентиляційних пристроїв та транспортних засобів, а також втрати на перетворення змінного струму на постійний, становить 18,5-21,0 тис. кВт/год на 1 т алюмінію. Енергетичний к. п. д. рафінувальних електролізерів не перевищує 5-7%, тобто 93-95% енергії витрачається у вигляді втрат тепла, що виділяється в основному в шарі електроліту (приблизно 80-85% від загального приходу тепла). Отже, основними шляхами подальшого зниження питомої витрати електроенергії на електролітичне рафінування алюмінію є вдосконалення теплоізоляції електролізера (особливо верхньої частини конструкції) та зниження шару електроліту (зменшення міжелектродної відстані).
Чистота алюмінію, рафінованого за тришаровим методом, 99,995%; вона визначається по різниці з п'ятьма основними домішками - залізом, кремнієм, міддю, цинком та титаном. Кількість одержуваного металу такої марки може становити 45-48% від загального випуску (без його розшивки з нижчими, сортами).
Слід, однак, відзначити, що електролітично рафінованому алюмінію містяться в менших кількостях домішки інших металів, що знижує абсолютну чистоту такого алюмінію. Радіоактиваційний аналіз дозволяє виявити в електролітично рафінованому алюмінію до 30 домішок, сумарний вміст яких приблизно 60-10 -4%. Отже, чистота рафінованого алюмінію за різницею з цими домішками становить 99,994%.
Крім домішок, передбачених ГОСТом (див. табл. 1.1), найбільш поширеній марці (А99) електролітично рафінованого алюмінію міститься, %: Cr 0,00016; V 0,0001; Ga 0,0006; Pb 0,002; Sn 0,00005; Ca 0,002-0,003; Na 0,001-0,008; Mn 0,001-0,007; Mg 0,001-0,007; As<0,0001; Sb<0,00002; Bi<0,00001; Cd<0,000001; S 0,0007.
Один із джерел забруднення катодного алюмінію - графітові струмовідводи, що містять окис заліза і кремнію і постійно стикаються з рафінованим алюмінієм. Якщо струм до катодного алюмінію підводити безпосередньо алюмінієвими шинами і застосовувати інструмент із дуже чистого графіту, можна отримувати метал чистотою 99,999% по різниці з домішками (Fe, Si, Cu, Zn і Ti). B такому металі міститься в середньому %: Si 0,0002; Fe 0,00032; Cu 0,0002; Zn 0,0002 та Ti 0,00005. Однак через технічні труднощі такий спосіб підведення струму поки що не знайшов широкого промислового застосування.
Набуття алюмінію особливої чистоти
Алюміній особливої чистоти (марки A999) може бути отриманий трьома способами: зонною плавкою, дистиляцією через субгалогеніди та електролізом алюміній-органічних сполук. З перерахованих способів отримання алюмінію особливої чистоти практичне застосування СРСР отримав спосіб зонної плавки.
Принцип зонної плавки полягає в багаторазовому проходженні розплавленої зони вздовж зливу алюмінію. За величиною коефіцієнтів розподілу К=Ств /С ж (де Ств - концентрація домішки в твердій і Сж - в рідкій фазі), які значною мірою визначають ефективність очищення від домішок, ці домішки можуть бути розбиті на три групи. До першої групи належать домішки, що знижують температуру плавлення алюмінію; вони мають До<1, при зонной плавке концентрируются в расплавленной зоне и переносятся ею к конечной части слитка. К числу этих примесей принадлежат Ga, Sn, Be, Sb, Ca, Th, Fe, Co, Ni, Ce, Te, Ba, Pt, Au, Bi, Pb, Cd, In, Na, Mg, Cu, Si, Ge, Zn. Ко второй группе принадлежат примеси, повышающие температуру плавления алюминия; они характеризуются К>1 і при зонній плавці концентруються у твердій (початковій) частині злитка. До цих домішок відносяться Nb, Ta, Cr, Ti, Mo, V. До третьої групи належать домішки з коефіцієнтом розподілу, дуже близьким до одиниці (Mn, Sc). Ці домішки практично не видаляються при зонній плавці алюмінію.
Алюміній, призначений для зонної плавки, піддають деякій підготовці, яка полягає у фільтрації, дегазації та травленні. Фільтрація необхідна для видалення з алюмінію тугоплавкою та міцної окисної плівки диспергованої в металі. Окис алюмінію, присутня в розплавленому алюмінії, може при його твердінні створювати центри кристалізації, що веде до отримання полікристалічного зливка та порушення ефекту перерозподілу домішок між твердим металом та розплавленою зоною. Фільтрацію алюмінію ведуть у вакуумі (залишковий тиск 0,1-0,4 Па) через отвір у дні графітового тигля діаметром 1,5-2 мм. Попередню дегазацію алюмінію перед зонною плавкою (також нагріванням у вакуумі) проводять для попередження розбризкування металу при розплавленні зони у разі проведення процесу у глибокому вакуумі. Остання стадія підготовки алюмінію до зонної плавки - травлення його поверхні сумішшю концентрованих соляної та азотної кислот.
Так як алюміній має значну хімічну активність і як основний матеріал для контейнерів (човників) застосовують особливо чистий графіт, то зонну плавку алюмінію проводять у вакуумі або в атмосфері інертного газу (аргон, гелій).
Зонною плавкою у вакуумі забезпечується велика чистота алюмінію внаслідок випаровування частини домішок при вакуумуванні (магнію, цинку, кадмію, лужних та лужноземельних металів), а також виключається забруднення очищеного металу домішками внаслідок застосування захисних інертних газів. Зонну плавку алюмінію у вакуумі можна проводити при безперервному відкачуванні кварцової труби, куди поміщають графітовий човник зі злитком алюмінію, а також у запаяних кварцових ампулах, з яких попередньо відкачують повітря до залишкового тиску приблизно 1?10 -3 Па.
Для створення розплавленої зони на зливці алюмінію при його зонній плавці може бути застосований нагрівання за допомогою невеликих печей опору або струмів високої частоти. Для електроживлення печей електроопору не потрібна складна апаратура, печі прості в експлуатації. Єдиний недолік цього методу нагріву - невеликий переріз зливка алюмінію, що очищається.
Індукційне нагрівання струмами високої частоти - ідеальний спосіб створення розплавленої зони на злитку при зонній плавці. Метод високочастотного нагріву (крім того, що він дозволяє здійснити зонне плавлення злитків великих перерізів) має важливу перевагу, що полягає в тому, що розплавлений метал безперервно перемішується в зоні; це полегшує дифузію атомів домішки від фронту кристалізації в глиб розплаву.
Вперше промислове виробництво алюмінію високої чистоти зонною плавкою було освоєно на Волхівському алюмінієвому заводі 1965 р. на установці УЗПІ-3, розробленої ВАМІ. Ця установка була оснащена чотирма кварцовими ретортами з індукційним нагріванням, причому індуктори були рухливими, а контейнери з металом нерухомими. Продуктивність її становила 20 кг металу за цикл очищення. Згодом була створена та введена в промислову експлуатацію у 1972 р. на Волховському алюмінієвому заводі більш високопродуктивна цільнометалева установка УЗПІ-4.
Ефективність очищення алюмінію при зонному плавленні може бути охарактеризована такими даними. Якщо сумарний вміст домішок в електролітично рафінованому алюмінії становить (30÷60) 10 –4 %, то після зонної плавки воно знижується до (2,8 ÷ 3,2) 10 –4 %, тобто в 15-20 разів. Це відповідає залишковому електроопору алюмінію ρ ○ (при температурі рідкого гелію 4,2 К) відповідно (20÷40)10 -10 і (1,8÷2,1)10 -10 або чистоті 99,997-99,994 і 99,9997%. У табл. 1.4 (див. нижче) наведено дані радіоактиваційного аналізу про вміст деяких домішок у зонно-очищеному алюмінії та електролітично рафінованому. Ці дані свідчать про сильне зниження вмісту більшості домішок, хоча такі домішки, як марганець і скандій, при зонній плавці практично не видаляються.
В останні роки у ВАМІ розроблено та випробувано в промислових умовах технологію отримання алюмінію чистотою 99,9999% методом каскадної зонної плавки. Сутність способу каскадної зонної плавки полягає в тому, що очищення вихідного алюмінію чистотою ведуть А999, послідовно повторюючи цикли (каскади) зонної планки. При цьому вихідним матеріалом кожного наступного каскаду служить середня, найчистіша частина зливка, що отримується в результаті попереднього циклу очищення.
ТАБЛИЦЯ 1.4
| Вихідний алюміній (електролітично рафінований 99,993-99,994%) | Алюміній після зонної плавки |
||
| графіт, вакуум | алунд, повітря |
||
| Мідь | 1,9 | 0,02 | 0,08 |
| Миш'як | 0,15 | 0,0015 | 0,001 |
| Сурма | 1,2 | 0,03 | 0,02 |
| Уран | 0,002 | - | - |
| Залізо | 3 | ≤0,2 | ≤0,3 |
| Галій | 0,3 | 0,02 | 0,05 |
| Марганець | 0,2-0,3 | 0,1-0,2 | 0,15 |
| Скандій | 0,4-0,5 | 0,4-0,5 | 0,4-0,5 |
| Ітрій | 0,02-0,04 | <<0,001 | <<0,001 |
| Лютецій | 0,002-0,004 | <<0,0001 | <<0,0001 |
| Гольмій | 0,005-0,01 | <<0,0001 | <<0,0001 |
| Гадоліній | 0,02-0,04 | <<0,01 | <<0,01 |
| Тербій | 0,003-0,006 | <<0,001 | <<0,001 |
| Самарій | 0,05-0,01 | <<0,0001 | <<0,0001 |
| Неодим | 0,1-0,2 | <<0,01 | <<0,01 |
| Празеодим | 0,05-0,1 | <<0,001 | <<0,001 |
| Церій | 0,3-0,6 | <<0,01 | <<0,01 |
| Лантан | 0,01 | <<0,001 | <<0,001 |
| Нікель | 2,3 | - | <1 |
| Кадмій | 3,5 | <<0,01 | 0,02-0,07 |
| Цинк | 20 | <<0,05 | 1 |
| Кобальт | 0,01 | <<0,01 | <<0,01 |
| Натрій | 1-2 | <0,2 | <0,2 |
| Калій | 0,05 | 0,01 | 0,01 |
| Барій | 6 | - | - |
| Хлор | 0,01 | <0,01 | <0,01 |
| Фосфор | 3 | 0,04 | - |
| Сірка | 15 | 0,5-1,5 | - |
| Вуглець | 1-2 | - | 1-2 |
| Примітка. Кількості телуру, вісмуту, срібла, молібдену, хрому, цирконію, кальцію, стронцію, рубідії, церію, індії, селену та ртуті в алюмінії після зонної плавки нижче чутливості радіоактивного аналізу. | |||
У табл. 1.5 (див. нижче) наведені результати мас-спектрального аналізу та вимірювання R 293 К /R 4,2 К алюмінію, отриманого каскадною зонною плавкою. З наведених даних можна зробити висновок, що чистота такого алюмінію, визначена по різниці з десятьма основними домішками (Si, Fe, Mg, Mn, Ti, Cu, Cr, Zn, Na і V), становить >99,9999%. Цей висновок побічно підтверджується величиною R 293 К /R 4,2 До, яка у всіх зразках становила >3010 3 .
Для отримання металу чистотою 99,9999% достатньо провести два каскади зонної плавки (див. табл. 1.5). Подальше збільшення числа каскадів не підвищує чистоту алюмінію, хоч і збільшує загальний вихід металу чистотою 99,9999%.
Іншим можливим процесом отримання алюмінію особливої чистоти є його дистиляція через субгалогениды, зокрема через субфторид алюмінію.
Тиск насиченої пари металевого алюмінію недостатньо високо, щоб здійснити його безпосередню дистиляцію з практично прийнятними швидкостями. Однак при нагріванні у вакуумі (при 1000-1050°С) з AlF 3 алюміній утворює легколетючий субфторид AlF, який переганяється в холодну зону (800°С), де знову розпадається (диспропорціонує) з виділенням чистого алюмінію:
Можливість глибокого очищення алюмінію від домішки в основному зумовлена тим, що ймовірність утворення субсполучень алюмінію значно більша за ймовірність утворення субз'єднань домішки.
ТАБЛИЦЯ 1.5
РЕЗУЛЬТАТИ МАС-СПЕКТРАЛЬНОГО АНАЛІЗУ ТА ВИМІРЮВАНЬ R 293 К /R 4,2 К АЛЮМІНІЮ КАСКАДНОЇ ЗОННОЇ ПЛАВКИ.
| Число каскадів | |||||||
| Початковий | 18,3 | 0,210 | <0,103 | 0,89 | <0,061 | 0,069 | 1,544 |
| A999 | |||||||
| 2 | 36,5 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 38,0 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 39,5 | 0,073 | <0,103 | 0,045 | <0,061 | 0,07 | 0,563 |
| 3 | 32,0 | 0,204 | <0,103 | 0,006 | <0,061 | 0,017 | 0,502 |
| 3 | 30,0 | 0,073 | 0,100 | 0,006 | 0,020 | 0,07 | 0,480 |
| 3 | 32,0 | 0,052 | 0,100 | 0,006 | 0,061 | 0,07 | 0,500 |
| 4 | 40,0 | <0,021 | <0,103 | 0,006 | 0,061 | 0,07 | 0,472 |
| 4 | 30,5 | 0,031 | 0,100 | 0,006 | 0,061 | 0,07 | 0,479 |
| 5 | 34,0 | 0,104 | <0,060 | 0,006 | 0,061 | 0,017 | 0,459 |
| Примітки: 1. Сума домішок дана з урахуванням інших домішок, вміст яких у всіх зразках становив ×10 –4 %:<0,071 Cu; <0,038 Cr; 0,048 Zn; 0,017 Na; 0,037 V. 2. При подсчете суммы примесей принимали их максимальное значение, равное пределу чувствительности анализа, например <0,061 считали как 0,061. |
|||||||
Вміст домішок в алюмінії, дистильованому через субфторид, знаходиться у зворотній залежності від маси одержуваних злитків. У зливках масою 1,5-1,7 кг сумарний вміст домішок (Si, Fe, Cu, Mg) становить 11 10 –4 %, а вміст газів 0,007 см 3 /100 г. Питомий залишковий опір (ρ ○) при температурі рідкого гелію для такого металу становить (1,7÷2,0) 10 –10 Омּсм. Дистиляція алюмінію через субфторид має ряд недоліків (порівняно невелика продуктивність, недостатньо глибока очищення від магнію та ін), тому спосіб не отримав промислового розвитку.
Розроблено також способи отримання алюмінію особливої чистоти електролізом комплексних алюмінійорганічних сполук, що відрізняються складом електроліту. Наприклад, ФРН застосовують спосіб електролізу 50%-ного розчину NaFּ2Al (C 2 H 5) 3 в толуолі. Рафінування проводять при 100°З напрузі на електролізері 1,0-1,5 і щільності струму 0,3-0,5 А/дм 2 з використанням алюмінієвих електродів. Катодний вихід струмом 99%. Електрохімічним рафінуванням в алюмінійорганічних електролітах істотно знижується вміст марганцю та скандію, які практично не видаляються при зонному очищенні. Недоліками зазначеного способу є його низька продуктивність та висока пожежна небезпека.
Для більш глибокого очищення алюмінію та отримання металу чистотою 99,99999% і більше можна використовувати комбінування зазначених вище способів: електроліз алюмінійорганічних сполук або сублімацію через субфторид з наступною зонною плавкою отриманого алюмінію. Наприклад, багаторазовим зонним очищенням алюмінію, отриманого електролізом алюмінійорганічних сполук, вдається отримати метал особливої чистоти з вмістом домішок, ×10 –9 %: Fe 50; Si<500; Cu 10; Mg 30; Mn 5; Ti <500; Cr 20; Zn <50; Co <1; Ag <5; Sb <1 и Se 3.
Застосування
Поєднання фізичних, механічних та хімічних властивостей алюмінію визначає його широке застосування практично у всіх галузях техніки, особливо у вигляді його сплавів з іншими металами. У електротехніці алюміній успішно замінює мідь, особливо у виробництві масивних провідників, наприклад, у повітряних лініях, високовольтних кабелях, шинах розподільчих пристроїв, трансформаторах (електрична провідність алюмінію досягає 65,5% електричної провідності міді, і він більш ніж утричі легший за мідь; при поперечному перерізі, що забезпечує одну і ту ж провідність, маса проводів з алюмінію вдвічі менша від мідних). Надчистий алюміній використовують у виробництві електричних конденсаторів і випрямлячів, дія яких заснована на можливості окисної плівки алюмінію пропускати електричний струм лише в одному напрямку. Надчистий алюміній, очищений зонною плавкою, застосовується для синтезу напівпровідникових сполук типу A III B V, що застосовуються для виробництва напівпровідникових приладів. Чистий алюміній використовують у виробництві різноманітних дзеркал відбивачів. Алюміній високої чистоти застосовують для запобігання металевим поверхням від дії атмосферної корозії (плакування, алюмінієва фарба). Маючи відносно низький переріз поглинання нейтронів, алюміній застосовується як конструкційний матеріал у ядерних реакторах.
В алюмінієвих резервуарах великої ємності зберігають і транспортують рідкі гази (метан, кисень, водень тощо), азотну та оцтову кислоти, чисту воду, перекис водню та харчові олії. Алюміній широко застосовують і в обладнанні та апаратах харчової промисловості, для пакування харчових продуктів (у вигляді фольги), для виробництва різного роду побутових виробів. Різко зросло споживання алюмінію для оздоблення будівель, архітектурних, транспортних та спортивних споруд.
У металургії алюміній (крім сплавів на його основі) – одна з найпоширеніших легуючих добавок у сплавах на основі Cu, Mg, Ti, Ni, Zn та Fe. Застосовують алюміній також для розкислення сталі перед заливанням її у форму, а також у процесах отримання деяких металів шляхом алюмінію. На основі алюмінію методом порошкової металургії створено САП (спечений алюмінієвий порошок), що має при температурах вище 300°С великою жароміцністю.
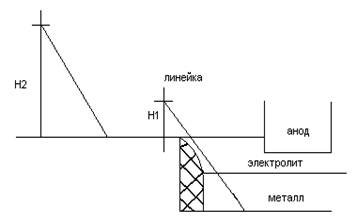
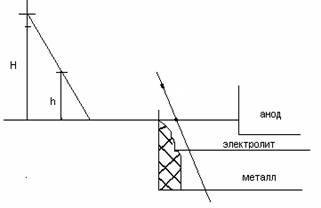
Збагачення анодних газів окисом вуглецю та появи в електроліті дуже дрібних частинок вуглецю. Інше ускладнення катодного процесу – це розряд катіонів Na+, який завжди міститься в алюмінії під час його виробництва. Кількість натрію, що виділився, залежить від кріолітового відношення (КО) електроліту. При зниженні КЗ з 3 до 2,5 вміст натрію знижується в 2,5 рази. При температурі...
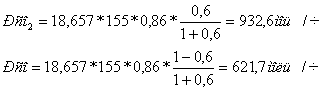
У разі застосування самопального анода частина анодної маси вибуває з процесу у вигляді летких складових її коксування. При матеріальному розрахунку визначають продуктивність електролізера та витрата сировини на виробництво алюмінію. продуктивність електролізера (Р), при силі струму J = 155А і прийнятому виході по струму = 86% становить: де 0,3354 - електрохімічний еквівалент; - ...
Інше співвідношення входять до складу домішок заліза та кремнію. Літера Е в марці АЕ означає, що алюміній цієї марки призначається для електропроводів. Додатковою вимогою до властивостей алюмінію є низький електроопір, який для дроту, виготовленого з нього, має бути не більше 0.0280 мм мм при 20 C. Алюміній застосовують для виробництва з нього виробів.
1.1 Отримання глинозему із руд
Глинозем одержують трьома способами: лужним, кислотним та електролітичним. Найбільше поширення має лужний спосіб (метод К. І. Байєра, розроблений в Росії наприкінці позаминулого століття і застосовується для переробки високосортних бокситів з невеликою кількістю (до 5-6%) кремнезему). З того часу технічне виконання його було суттєво покращено. Схема виробництва глинозему за способом Байєра представлена на рис. 1.
Сутність способу полягає в тому, що алюмінієві розчини швидко розкладаються при введенні в них гідроксиду алюмінію, а розчин, що залишився, після його випарювання в умовах інтенсивного перемішування при 169-170 про С може знову розчиняти глинозем, що міститься в бокситах. Цей спосіб складається з наступних основних операцій:
Підготовка бокситу, що полягає в його дробленні та подрібненні в млинах; в млина подають боксит, їдкий луг і невелику кількість вапна, яке покращує виділення Al 2 O 3 ; отриману пульпу подають на вилуговування;
Вилужування бокситу (останнім часом застосовувані досі блоки автоклав круглої форми частково замінені трубчастими автоклавами, в яких при температурах 230-250°С (500-520 К) відбувається вилуговування), що полягає в його хімічному розкладанні від взаємодії з водним розчином лугу; гідрати окису алюмінію при взаємодії зі лугом переходять у розчин у вигляді алюмінію натрію:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH) 3 +NaOH→NaAlO 2 +2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H 2 O;
у розчині алюмінат натрію та силікат натрію утворюють нерозчинний натрієвий алюмосилікат; у нерозчинний залишок переходять окисли титану і заліза, що надають залишку червоного кольору; цей залишок називають червоним шламом. Після закінчення розчинення отриманий алюмінат натрію розбавляють водним розчином лугу при одночасному зниженні температури на 100°З;
Відділення алюмінатного розчину від червоного шламу зазвичай здійснюється шляхом промивання у спеціальних згущувачах; внаслідок цього червоний шлам осідає, а алюмінійний розчин зливають і потім фільтрують (освітлюють). В обмежених кількостях шлам знаходить застосування, наприклад як добавка до цементу. Залежно від сорту бокситів на 1 т одержаного окису алюмінію припадає 0,6-1,0 т червоного шламу (сухого залишку);
Розкладання алюмінатного розчину. Його фільтрують та перекачують у великі ємності з мішалками (декомпозери). З пересиченого розчину при охолодженні на 60°С (330 До) і постійному перемішуванні витягується гідроксид алюмінію Al(OH) 3 . Так як цей процес протікає повільно і нерівномірно, а формування і зростання кристалів гідроксиду алюмінію мають велике значення при її подальшій обробці, декомпозери додають велику кількість твердого гідроксиду - затравки:
Na 2 OּAl 2 O 3 +4H 2 O→Al(OH) 3 +2NaOH;
Виділення гідроксиду алюмінію та його класифікації; це відбувається у гідроциклонах та вакуум-фільтрах, де від алюмінатного розчину виділяють осад, що містить 50-60% частинок Al(OH). Значну частину гідроокису повертають у процес декомпозиції як затравний матеріал, яка залишається в обороті в незмінних кількостях. Залишок після промивання водою йде кальцинацію; фільтрат також повертається в оборот (після концентрації у випарних апаратах - для вилуговування нових бокситів);
Зневоднення гідроксиду алюмінію (кальцинації); це завершальна операція виробництва глинозему; її здійснюють у трубчастих обертових печах, а останнім часом також у печах з турбулентним рухом матеріалу при температурі 1150-1300 про З; сирий гідроксид алюмінію, проходячи через піч, що обертається, висушується і зневоднюється; при нагріванні відбуваються послідовно такі структурні перетворення:
| Al(OH) 3 →AlOOH→ γ-Al 2 O 3 → α-Al 2 O 3 |
В остаточно прожареному глиноземі міститься 30-50% -Al 2 O 3 (корунд), решта -Al 2 O 3 .
Цим способом витягується 85-87% від всього одержуваного глинозему. Отриманий окис алюмінію являє собою міцну хімічну сполуку з температурою плавлення 2050 про С.
1.2 Одержання алюмінію з його окису
Електролітичне відновлення окису алюмінію, розчиненого в розплаві на основі кріоліту, здійснюється за 950-970°С в електролізері. Електролізер складається з футерованої вуглецевими блоками ванни, до подіни якої підводиться електричний струм. Рідкий алюміній, що виділився на подині, що служить катодом, важчий за розплав солі електроліту, тому збирається на вугільній підставі, звідки його періодично відкачують (рис. 2). Зверху в електроліт занурені вугільні аноди, які згоряють в атмосфері кисню, що виділяється з окису алюмінію, виділяючи окис вуглецю (CO) або двоокис вуглецю (CO 2). На практиці знаходять застосування два типи анодів:
а) самопалюючі аноди Зедерберга, що складаються з брикетів, так званих «хлібів» маси Зедерберга (малозолильне вугілля з 25-35% кам'яновугільного пеку), набитих в алюмінієву оболонку; під дією високої температури анодна маса випалюється (спікається);
б) обпалені, або «безперервні», аноди з великих вугільних блоків (наприклад, 1900 600 500 мм масою близько 1,1 т).
Сила струму на електролізерах становить 150 000 А. Вони входять у мережу послідовно, т. е. виходить система (серія) - довгий ряд електролізерів.
Робоча напруга на ванні, що становить 4-5, значно вище напруги, при якому відбувається розкладання окису алюмінію, оскільки в процесі роботи неминучі втрати напруги в різних частинах системи. Баланс сировини та енергії при отриманні 1 т алюмінію представлений на рис. 3.
Електроліз хлориду алюмінію (метод фірми Алкоа)
У реакційній посудині окис алюмінію перетворюється спочатку на хлорид алюмінію. Потім у щільно ізольованій ванні відбувається електроліз AlCl 3 розчиненого в розплаві солей KCl, NaCl. Хлор, що виділяється при цьому, відсмоктується і подається для вторинного використання; алюміній осідає на катоді.
Перевагами даного методу перед існуючим електролізом рідкого кріолітоглиноземного розплаву (Al 2 O 3 розчинена в кріоліті Na 3 AlF 6) вважають: економію до 30% енергії; можливість застосування окису алюмінію, який не підходить для традиційного електролізу (наприклад, Al 2 O 3 з високим вмістом кремнію); заміну дорогого кріоліту дешевшими солями; зникнення небезпеки виділення фтору.
Відновлення хлориду алюмінію марганцем (Toth – метод)
При відновленні марганцем із хлориду алюмінію звільняється алюміній. Через керовану конденсацію з потоку хлориду марганцю виділяються пов'язані з хлором забруднення. При звільненні хлору хлорид марганцю окислюється в окис марганцю, який відновлюється до марганцю, придатного до вторинного застосування. Відомості в наявних публікаціях дуже неточні, тож у разі доведеться відмовитися від оцінки методу.


