30.08.2019
เทคโนโลยีการผลิตอลูมิเนียม กระบวนการทางเทคโนโลยีการผลิตอะลูมิเนียม
1.1 การรับอลูมินาจากแร่
อลูมินาผลิตได้สามวิธี: อัลคาไลน์ กรด และอิเล็กโทรไลต์ วิธีที่ใช้กันอย่างแพร่หลายที่สุดคือวิธีอัลคาไลน์ (วิธีของ K.I. ไบเออร์พัฒนาขึ้นในรัสเซียเมื่อปลายศตวรรษก่อนหน้านั้นและใช้สำหรับการประมวลผลบอกไซต์คุณภาพสูงที่มีซิลิกาจำนวนเล็กน้อย (มากถึง 5-6%) ตั้งแต่นั้นมา การใช้งานด้านเทคนิคก็ได้รับการปรับปรุงให้ดีขึ้นอย่างมาก แผนภาพการผลิตอลูมินาโดยใช้วิธีของไบเออร์แสดงไว้ในรูปที่ 1 1.
สาระสำคัญของวิธีการนี้คือสารละลายอะลูมิเนียมจะสลายตัวอย่างรวดเร็วเมื่อมีการนำอะลูมิเนียมไฮดรอกไซด์เข้าไปและสารละลายที่เหลือจากการสลายตัวหลังจากการระเหยภายใต้สภาวะการกวนอย่างเข้มข้นที่ 169-170 o C สามารถละลายอลูมินาที่มีอยู่ในอะลูมิเนียมได้อีกครั้ง วิธีนี้ประกอบด้วยการดำเนินการพื้นฐานดังต่อไปนี้:
การเตรียมอะลูมิเนียมซึ่งประกอบด้วยการบดและบดในโรงสี อะลูมิเนียม, ด่างกัดกร่อนและมะนาวจำนวนเล็กน้อยถูกส่งไปยังโรงงานซึ่งช่วยเพิ่มการปล่อย Al 2 O 3; เยื่อกระดาษที่ได้จะถูกป้อนเพื่อการชะล้าง
การชะล้างแร่อะลูมิเนียม (นิ้ว เมื่อเร็วๆ นี้บล็อกหม้อนึ่งความดันทรงกลมที่ใช้จนถึงขณะนี้ได้ถูกแทนที่ด้วยหม้อนึ่งความดันแบบท่อบางส่วน ซึ่งการชะล้างจะเกิดขึ้นที่อุณหภูมิ 230-250 ° C (500-520 K) ซึ่งประกอบด้วยการสลายตัวทางเคมีจากการมีปฏิสัมพันธ์กับ สารละลายที่เป็นน้ำด่าง; เมื่อทำปฏิกิริยากับอัลคาไล อะลูมิเนียมออกไซด์ไฮเดรตจะเข้าสู่สารละลายในรูปของโซเดียมอะลูมิเนต:
AlOOH+NaOH → NaAlO 2 +H 2 O
อัล(OH) 3 + NaOH → NaAlO 2 + 2H 2 O;
SiO 2 +2NaOH→นา 2 SiO 3 +H 2 O;
ในสารละลาย โซเดียมอะลูมิเนตและโซเดียมซิลิเกตทำให้เกิดโซเดียมอะลูมิโนซิลิเกตที่ไม่ละลายน้ำ ออกไซด์ของไทเทเนียมและเหล็กผ่านเข้าไปในสารตกค้างที่ไม่ละลายน้ำทำให้สารตกค้างมีสีแดง สารตกค้างนี้เรียกว่าโคลนแดง เมื่อการละลายเสร็จสิ้น โซเดียมอะลูมิเนตที่ได้จะถูกเจือจางด้วยสารละลายอัลคาไลที่เป็นน้ำในขณะเดียวกันก็ลดอุณหภูมิลง 100°C ในเวลาเดียวกัน
การแยกสารละลายอะลูมิเนตออกจากโคลนสีแดง มักดำเนินการโดยการล้างด้วยสารเพิ่มความข้นพิเศษ ผลที่ได้คือ โคลนสีแดงจะตกตะกอน และสารละลายอะลูมิเนตจะถูกระบายออกแล้วจึงกรอง (ทำให้กระจ่าง) ตัวอย่างเช่น มีการใช้ตะกอนในปริมาณที่จำกัด เป็นสารเติมแต่งให้กับซีเมนต์ อลูมิเนียมออกไซด์ที่ผลิตได้ 1 ตันขึ้นอยู่กับประเภทของแร่บอกไซต์ คิดเป็นโคลนแดง (กากแห้ง) 0.6-1.0 ตัน
การสลายตัวของสารละลายอะลูมิเนต มันถูกกรองและปั๊มลงในภาชนะขนาดใหญ่พร้อมเครื่องกวน (ตัวย่อยสลาย) อะลูมิเนียมไฮดรอกไซด์ Al(OH) 3 ถูกสกัดจากสารละลายอิ่มตัวยวดยิ่งเมื่อเย็นลงถึง 60°C (330 K) และกวนอย่างต่อเนื่อง เนื่องจากกระบวนการนี้ดำเนินไปอย่างช้าๆ และไม่สม่ำเสมอ และการก่อตัวและการเติบโตของผลึกอะลูมิเนียมไฮดรอกไซด์มีความสำคัญอย่างยิ่งในระหว่างการประมวลผลขั้นต่อไป จึงมีการเพิ่มไฮดรอกไซด์ที่เป็นของแข็งจำนวนมากซึ่งเป็นเมล็ดพืชเข้าไปในตัวย่อยสลาย:
นา 2 Oּอัล 2 O 3 +4H 2 O→อัล(OH) 3 +2NaOH;
การแยกอะลูมิเนียมไฮดรอกไซด์และการจำแนกประเภท สิ่งนี้เกิดขึ้นในไฮโดรไซโคลนและตัวกรองสุญญากาศ โดยที่ตะกอนที่มีอนุภาคอัล (OH) 50-60% จะถูกแยกออกจากสารละลายอะลูมิเนต ส่วนสำคัญของไฮดรอกไซด์จะถูกส่งกลับไปยังกระบวนการสลายตัวในฐานะวัสดุเมล็ดซึ่งยังคงหมุนเวียนอยู่ในปริมาณที่ไม่เปลี่ยนแปลง สารตกค้างหลังจากล้างด้วยน้ำจะถูกเผา การกรองจะถูกส่งกลับไปสู่การไหลเวียน (หลังจากความเข้มข้นในเครื่องระเหย - เพื่อชะล้างแร่อะลูมิเนียมใหม่)
การคายน้ำของอะลูมิเนียมไฮดรอกไซด์ (การเผา); นี่เป็นขั้นตอนสุดท้ายในการผลิตอลูมินา ดำเนินการในเตาเผาแบบหมุนแบบท่อและเมื่อเร็ว ๆ นี้ในเตาเผาที่มีการเคลื่อนย้ายวัสดุอย่างปั่นป่วนที่อุณหภูมิ 1,150-1300 o C; อะลูมิเนียมไฮดรอกไซด์ดิบที่ผ่านเตาเผาแบบหมุนทำให้แห้งและขาดน้ำ เมื่อได้รับความร้อน การเปลี่ยนแปลงโครงสร้างต่อไปนี้จะเกิดขึ้นตามลำดับ:
| อัล(OH) 3 →อัลOOH→ γ-อัล 2 O 3 → α-อัล 2 O 3 |
อลูมินาที่เผาในที่สุดจะมี 30-50% α-Al 2 O 3 (คอรันดัม) ส่วนที่เหลือคือγ-Al 2 O 3
วิธีนี้จะสกัดอลูมินาที่ผลิตได้ทั้งหมด 85-87% ส่งผลให้อะลูมิเนียมออกไซด์มีความทนทาน สารประกอบเคมีโดยมีจุดหลอมเหลว 2050 o C
1.2 การเตรียมอะลูมิเนียมจากออกไซด์
การลดอะลูมิเนียมออกไซด์ด้วยไฟฟ้าที่ละลายในการหลอมที่ใช้ไครโอไลท์จะดำเนินการที่อุณหภูมิ 950-970°C ในอิเล็กโทรไลเซอร์ อิเล็กโทรไลเซอร์ประกอบด้วยอ่างที่เรียงรายไปด้วยบล็อกคาร์บอน ซึ่งอยู่ด้านล่างของที่จ่ายกระแสไฟฟ้า อลูมิเนียมเหลวที่ปล่อยออกมาบนเตาซึ่งทำหน้าที่เป็นแคโทดนั้นหนักกว่าเกลือหลอมเหลวของอิเล็กโทรไลต์ดังนั้นจึงถูกรวบรวมบนฐานถ่านหินจากจุดที่ถูกสูบออกมาเป็นระยะ (รูปที่ 2) แอโนดคาร์บอนจะถูกจุ่มลงในอิเล็กโทรไลต์ที่อยู่ด้านบน ซึ่งจะเผาไหม้ในบรรยากาศของออกซิเจนที่ปล่อยออกมาจากอลูมิเนียมออกไซด์ และปล่อยก๊าซคาร์บอนมอนอกไซด์ (CO) หรือก๊าซคาร์บอนไดออกไซด์ (CO2) ออกมา ในทางปฏิบัติ มีการใช้แอโนดสองประเภท:
ก) แอโนด Zederberg ที่เผาไหม้ตัวเองซึ่งประกอบด้วยก้อนอิฐที่เรียกว่า "ขนมปัง" ของมวล Zederberg (ถ่านหินเถ้าต่ำที่มีระดับน้ำมันดินถ่านหิน 25-35%) ยัดลงในเปลือกอลูมิเนียม ภายใต้อิทธิพลของอุณหภูมิสูงมวลแอโนดจะถูกเผา (เผา)
b) แอโนดแบบอบหรือ "ต่อเนื่อง" ที่ทำจากบล็อกคาร์บอนขนาดใหญ่ (เช่น 1900x600x500 มม. หนักประมาณ 1.1 ตัน)
ความแรงของกระแสไฟฟ้าในอิเล็กโทรไลเซอร์คือ 150,000 A ซึ่งเชื่อมต่อกับเครือข่ายแบบอนุกรมนั่นคือได้รับระบบ (ซีรีย์) - อิเล็กโทรไลเซอร์แถวยาว
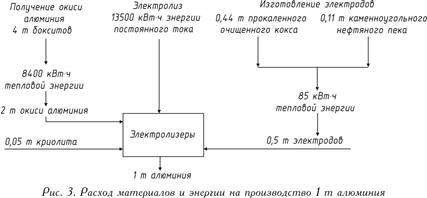
แรงดันไฟฟ้าที่ใช้งานบนอ่าง 4-5 V สูงกว่าแรงดันไฟฟ้าที่อะลูมิเนียมออกไซด์สลายตัวอย่างมาก เนื่องจากแรงดันไฟฟ้าสูญเสียใน ส่วนต่างๆระบบ ความสมดุลของวัตถุดิบและพลังงานในการผลิตอลูมิเนียม 1 ตันแสดงไว้ในรูปที่ 1 3.
อิเล็กโทรไลซิสของอะลูมิเนียมคลอไรด์ (วิธีแอลโค)
ในถังปฏิกิริยา อะลูมิเนียมออกไซด์จะถูกแปลงเป็นอะลูมิเนียมคลอไรด์ก่อน จากนั้น ในอ่างที่มีฉนวนอย่างแน่นหนา จะเกิดอิเล็กโทรไลซิสของ AlCl 3 ที่ละลายในเกลือหลอมเหลวที่มี KCl และ NaCl เกิดขึ้น คลอรีนที่ปล่อยออกมาในระหว่างกระบวนการนี้จะถูกดูดออกและนำไปรีไซเคิล อลูมิเนียมจะเกาะอยู่บนแคโทด
ประโยชน์ วิธีนี้ก่อนกระแสไฟฟ้าที่มีอยู่ของการหลอมไครโอไลท์-อลูมินาเหลว (Al 2 O 3 ละลายใน Na 3 AlF 6 cryolite) ให้พิจารณา: ประหยัดพลังงานได้มากถึง 30%; ความเป็นไปได้ของการใช้อลูมิเนียมออกไซด์ซึ่งไม่เหมาะสำหรับการอิเล็กโทรไลซิสแบบเดิม (เช่น Al 2 O 3 ด้วย เนื้อหาสูงซิลิคอน); แทนที่ไครโอไลท์ราคาแพงด้วยเกลือราคาถูก หายจากอันตรายจากการปล่อยฟลูออไรด์
การลดอะลูมิเนียมคลอไรด์ด้วยแมงกานีส (วิธี Toth)
เมื่อรีดิวซ์ด้วยแมงกานีส อลูมิเนียมจะถูกปล่อยออกมาจากอะลูมิเนียมคลอไรด์ สารปนเปื้อนที่เกี่ยวข้องกับคลอรีนจะถูกปล่อยออกจากกระแสแมงกานีสคลอไรด์ผ่านการควบคุมการควบแน่น เมื่อคลอรีนถูกปล่อยออกมา แมงกานีสคลอไรด์จะถูกออกซิไดซ์เป็นแมงกานีสออกไซด์ จากนั้นจึงรีดิวซ์เป็นแมงกานีส เหมาะสำหรับการใช้งานขั้นที่สอง ข้อมูลในสิ่งพิมพ์ที่มีอยู่ไม่ถูกต้องมาก ดังนั้นในกรณีนี้จำเป็นต้องละทิ้งการประเมินวิธีการดังกล่าว
ตำนานที่น่าสงสัยอย่างหนึ่งเล่าว่าวันหนึ่งมีชายคนหนึ่งมาหาจักรพรรดิแห่งโรมัน Tiberius (42 ปีก่อนคริสตกาล - 37 AD) พร้อมชามโลหะที่ไม่แตกหัก วัสดุของชามน่าจะมาจากอลูมินา (Al 2 O 3) และดังนั้นจึงต้องเป็นอะลูมิเนียม ด้วยความกลัวว่าโลหะที่ทำจากดินเหนียวอาจทำให้ทองคำและเงินเสื่อมราคา ทิเบเรียสจึงสั่งให้ตัดศีรษะของชายคนนั้นออก เผื่อไว้ แน่นอนว่าเรื่องราวนี้ยากที่จะเชื่อ: อะลูมิเนียมพื้นเมืองไม่ได้เกิดขึ้นในธรรมชาติ และในสมัยของจักรวรรดิโรมันก็ยังไม่มีวิธีการทางเทคนิคที่จะทำให้สามารถแยกอะลูมิเนียมออกจากสารประกอบได้
ในแง่ของความชุกในธรรมชาติ อลูมิเนียมเป็นอันดับแรกในบรรดาโลหะ เนื้อหาในเปลือกโลกคือ 7.45% อย่างไรก็ตาม แม้จะมีการเกิดขึ้นอย่างกว้างขวางในธรรมชาติ แต่อะลูมิเนียมก็ยังขึ้นอยู่กับ ปลาย XIXศตวรรษเป็นของโลหะหายาก ไม่พบอลูมิเนียมในรูปแบบบริสุทธิ์เนื่องจากมีฤทธิ์ทางเคมีสูง ส่วนใหญ่พบในรูปของสารประกอบที่มีออกซิเจนและซิลิคอน - อะลูมิโนซิลิเกต
มีเพียงหินที่อุดมไปด้วยอลูมินา (Al 2 O 3) และเกิดขึ้นเป็นจำนวนมากบนพื้นผิวโลกเท่านั้นที่สามารถทำหน้าที่เป็นแร่อะลูมิเนียมได้ หินเหล่านี้ได้แก่ บอกไซต์, เนฟีลีน - (Na, K) 2 OּAl 2 O 3 ּ2SiO 2, อะลูไนต์ - (Na, K) 2 SO 4 ּAl 2 (SO 4) 3 ּ4Al(OH) 3 และดินขาว (ดินเหนียว), สปาร์ฟิลด์ (ออร์โธเคลส) - K 2 OּAl 2 O 3 ּ6SiO 2 .
แร่หลักในการผลิตอะลูมิเนียมคือแร่บอกไซต์ ประกอบด้วยอลูมิเนียมในรูปของไฮดรอกไซด์ Al(OH), AlOOH, คอรันดัม Al 2 O 3 และ kaolinite Al 2 O 3 ּ2SiO 2 ּ2H 2 O องค์ประกอบทางเคมีอะลูมิเนียมประกอบด้วย: อลูมินา 28-70%; ซิลิกา 0.5-20%; เหล็กออกไซด์ 2-50%; ไทเทเนียมออกไซด์ 0.1-10% เมื่อเร็ว ๆ นี้ nephelines และ alunite ถูกใช้เป็นแร่
แร่บอกไซต์จำนวนมากตั้งอยู่ในเทือกเขาอูราลในเขต Tikhvin ของภูมิภาคเลนินกราดในดินแดนอัลไตและครัสโนยาสค์
เนฟีลีน (KּNa 2 OּAl 2 O 3 ּ2SiO 2) เป็นส่วนหนึ่งของหินอะพาไทต์เนฟิลีน (บนคาบสมุทรโคลา)
อะลูมิเนียมถูกแยกออกครั้งแรกในรูปแบบอิสระในปี พ.ศ. 2368 โดยนักฟิสิกส์ชาวเดนมาร์ก เออร์สเตด โดยทำปฏิกิริยาโพแทสเซียมอะมัลกัมกับอะลูมิเนียมคลอไรด์ ในปี พ.ศ. 2370 นักเคมีชาวเยอรมัน Wöhler ปรับปรุงวิธีการของ Oersted โดยแทนที่โพแทสเซียมอะมัลกัมด้วยโพแทสเซียมของโลหะ:
AlCl 3 + 3K→3KCl + Al (ปฏิกิริยาเกิดขึ้นเมื่อปล่อยความร้อน)
ในปี ค.ศ. 1854 Sainte-Clair Deville ในฝรั่งเศสใช้วิธีการของ Wöhler เป็นครั้งแรก การผลิตภาคอุตสาหกรรมอลูมิเนียมโดยใช้โซเดียมราคาถูกแทนโพแทสเซียมและแทนอลูมิเนียมคลอไรด์ที่ดูดความชื้น - คลอไรด์สองเท่าของอลูมิเนียมและโซเดียมที่เสถียรกว่า ในปี ค.ศ. 1865 นักเคมีกายภาพชาวรัสเซีย N. N. Beketov แสดงให้เห็นความเป็นไปได้ที่จะแทนที่อะลูมิเนียมด้วยแมกนีเซียมจากไครโอไลท์ที่หลอมละลาย ปฏิกิริยานี้ใช้ในปี พ.ศ. 2431 เพื่อผลิตอะลูมิเนียมที่โรงงานแห่งแรกในเยอรมันในเมือง Gmelingen การผลิตอะลูมิเนียมโดยวิธีที่เรียกว่า "เคมี" เหล่านี้ดำเนินการตั้งแต่ปี พ.ศ. 2397 ถึง พ.ศ. 2433 ตลอดระยะเวลา 35 ปี มีการผลิตอะลูมิเนียมทั้งหมดประมาณ 20 ตันโดยใช้วิธีการเหล่านี้
ในช่วงปลายทศวรรษที่ 80 ของศตวรรษก่อนหน้านั้น วิธีการทางเคมีแทนที่วิธีอิเล็กโทรไลต์ซึ่งทำให้สามารถลดต้นทุนของอลูมิเนียมได้อย่างมากและสร้างข้อกำหนดเบื้องต้นสำหรับการพัฒนาอย่างรวดเร็วของอุตสาหกรรมอลูมิเนียม Héroux ผู้ก่อตั้งวิธีการผลิตอะลูมิเนียมด้วยไฟฟ้าสมัยใหม่ Héroux ในฝรั่งเศสและ Hall ในสหรัฐอเมริกา ยื่นคำขอที่คล้ายกันโดยอิสระในปี พ.ศ. 2429 สำหรับการจดสิทธิบัตรวิธีการผลิตอะลูมิเนียมด้วยกระแสไฟฟ้าของอลูมินาที่ละลายในไครโอไลท์หลอมเหลว นับตั้งแต่การปรากฏตัวของสิทธิบัตรของ Heroux และ Hall อุตสาหกรรมอะลูมิเนียมยุคใหม่ก็เริ่มต้นขึ้น ซึ่งตลอดระยะเวลากว่า 115 ปีของการดำรงอยู่ได้เติบโตขึ้นจนกลายเป็นสาขาโลหะวิทยาที่ใหญ่ที่สุดแห่งหนึ่ง
กระบวนการทางเทคโนโลยีในการผลิตอะลูมิเนียมประกอบด้วยสามขั้นตอนหลัก:
1). การได้รับอลูมินา (Al 2 O 3) จากแร่อะลูมิเนียม
2). การผลิตอะลูมิเนียมจากอลูมินา
3). การกลั่นอลูมิเนียม
การได้รับอลูมินาจากแร่
อลูมินาผลิตได้สามวิธี: อัลคาไลน์ กรด และอิเล็กโทรไลต์ วิธีที่ใช้กันอย่างแพร่หลายที่สุดคือวิธีอัลคาไลน์ (วิธีของ K.I. ไบเออร์พัฒนาขึ้นในรัสเซียเมื่อปลายศตวรรษก่อนหน้านั้นและใช้สำหรับการประมวลผลบอกไซต์คุณภาพสูงที่มีซิลิกาจำนวนเล็กน้อย (มากถึง 5-6%) ตั้งแต่นั้นมา การใช้งานด้านเทคนิคก็ได้รับการปรับปรุงให้ดีขึ้นอย่างมาก แผนภาพการผลิตอลูมินาโดยใช้วิธีของไบเออร์แสดงไว้ในรูปที่ 1 1.
สาระสำคัญของวิธีการนี้คือสารละลายอะลูมิเนียมจะสลายตัวอย่างรวดเร็วเมื่อมีการนำอะลูมิเนียมไฮดรอกไซด์เข้าไปและสารละลายที่เหลือจากการสลายตัวหลังจากการระเหยภายใต้สภาวะการกวนอย่างเข้มข้นที่ 169-170 o C สามารถละลายอลูมินาที่มีอยู่ในอะลูมิเนียมได้อีกครั้ง วิธีนี้ประกอบด้วยการดำเนินการพื้นฐานดังต่อไปนี้:
1). การเตรียมอะลูมิเนียมซึ่งประกอบด้วยการบดและบดในโรงสี อะลูมิเนียม, ด่างกัดกร่อนและมะนาวจำนวนเล็กน้อยถูกส่งไปยังโรงงานซึ่งจะช่วยปรับปรุงการปล่อย Al 2 O 3 เยื่อกระดาษที่ได้จะถูกป้อนเพื่อการชะล้าง
2). การชะล้างแร่อะลูมิเนียม (เมื่อเร็ว ๆ นี้ บล็อกหม้อนึ่งความดันทรงกลมที่ยังคงใช้อยู่ได้ถูกแทนที่ด้วยหม้อนึ่งความดันแบบท่อบางส่วน ซึ่งการชะล้างเกิดขึ้นที่อุณหภูมิ 230-250 ° C (500-520 K) ซึ่งประกอบด้วยการสลายตัวทางเคมีจากปฏิกิริยากับ สารละลายอัลคาไลที่เป็นน้ำ เมื่อทำปฏิกิริยากับอัลคาไล อะลูมิเนียมออกไซด์ไฮเดรตจะเข้าสู่สารละลายในรูปของโซเดียมอะลูมิเนต:
AlOOH+NaOH → NaAlO 2 +H 2 O
อัล(OH) 3 + NaOH → NaAlO 2 + 2H 2 O;
SiO 2 +2NaOH→นา 2 SiO 3 +H 2 O;
ในสารละลาย โซเดียมอะลูมิเนตและโซเดียมซิลิเกตทำให้เกิดโซเดียมอะลูมิโนซิลิเกตที่ไม่ละลายน้ำ ออกไซด์ของไทเทเนียมและเหล็กผ่านเข้าไปในสารตกค้างที่ไม่ละลายน้ำทำให้สารตกค้างมีสีแดง สารตกค้างนี้เรียกว่าโคลนแดง เมื่อการละลายเสร็จสิ้น โซเดียมอะลูมิเนตที่ได้จะถูกเจือจางด้วยสารละลายอัลคาไลที่เป็นน้ำในขณะเดียวกันก็ลดอุณหภูมิลง 100°C ในเวลาเดียวกัน
3). การแยกสารละลายอะลูมิเนตออกจากโคลนสีแดง มักดำเนินการโดยการล้างด้วยสารเพิ่มความข้นพิเศษ ผลที่ได้คือ โคลนสีแดงจะตกตะกอน และสารละลายอะลูมิเนตจะถูกระบายออกแล้วจึงกรอง (ทำให้กระจ่าง) ตัวอย่างเช่น มีการใช้ตะกอนในปริมาณที่จำกัด เป็นสารเติมแต่งให้กับซีเมนต์ อลูมิเนียมออกไซด์ที่ผลิตได้ 1 ตันขึ้นอยู่กับประเภทของแร่บอกไซต์ คิดเป็นโคลนแดง (กากแห้ง) 0.6-1.0 ตัน
4) การสลายตัวของสารละลายอะลูมิเนต มันถูกกรองและปั๊มลงในภาชนะขนาดใหญ่พร้อมเครื่องกวน (ตัวย่อยสลาย) อะลูมิเนียมไฮดรอกไซด์ Al(OH) 3 ถูกสกัดจากสารละลายอิ่มตัวยวดยิ่งเมื่อเย็นลงถึง 60°C (330 K) และกวนอย่างต่อเนื่อง เนื่องจากกระบวนการนี้ดำเนินไปอย่างช้าๆ และไม่สม่ำเสมอ และการก่อตัวและการเติบโตของผลึกอะลูมิเนียมไฮดรอกไซด์มีความสำคัญอย่างยิ่งในระหว่างการประมวลผลขั้นต่อไป จึงมีการเพิ่มไฮดรอกไซด์ที่เป็นของแข็งจำนวนมากซึ่งเป็นเมล็ดพืชเข้าไปในตัวย่อยสลาย:
นา 2 Oּอัล 2 O 3 +4H 2 O→อัล(OH) 3 +2NaOH;
5). การแยกอะลูมิเนียมไฮดรอกไซด์และการจำแนกประเภท สิ่งนี้เกิดขึ้นในไฮโดรไซโคลนและตัวกรองสุญญากาศ โดยที่ตะกอนที่มีอนุภาคอัล (OH) 50-60% จะถูกแยกออกจากสารละลายอะลูมิเนต ส่วนสำคัญของไฮดรอกไซด์จะถูกส่งกลับไปยังกระบวนการสลายตัวในฐานะวัสดุเมล็ดซึ่งยังคงหมุนเวียนอยู่ในปริมาณที่ไม่เปลี่ยนแปลง สารตกค้างหลังจากล้างด้วยน้ำจะถูกเผา การกรองจะถูกส่งกลับไปสู่การไหลเวียน (หลังจากความเข้มข้นในเครื่องระเหย - เพื่อชะล้างแร่อะลูมิเนียมใหม่)
6). การคายน้ำของอะลูมิเนียมไฮดรอกไซด์ (การเผา); นี่เป็นขั้นตอนสุดท้ายในการผลิตอลูมินา ดำเนินการในเตาเผาแบบหมุนแบบท่อและเมื่อเร็ว ๆ นี้ในเตาเผาที่มีการเคลื่อนย้ายวัสดุอย่างปั่นป่วนที่อุณหภูมิ 1,150-1300 o C; อะลูมิเนียมไฮดรอกไซด์ดิบที่ผ่านเตาเผาแบบหมุนทำให้แห้งและขาดน้ำ เมื่อได้รับความร้อน การเปลี่ยนแปลงโครงสร้างต่อไปนี้จะเกิดขึ้นตามลำดับ:
| อัล(OH) 3 →อัลOOH→ γ-อัล 2 O 3 → α-อัล 2 O 3 | |||
| 200 o C– | 950 หรือ C– | 1200 องศาเซลเซียส | |
อลูมินาที่เผาในที่สุดจะมี 30-50% α-Al 2 O 3 (คอรันดัม) ส่วนที่เหลือคือγ-Al 2 O 3
วิธีนี้จะสกัดอลูมินาที่ผลิตได้ทั้งหมด 85-87% อลูมิเนียมออกไซด์ที่ได้จะเป็นสารประกอบเคมีชนิดเข้มข้นที่มีจุดหลอมเหลว 2,050 o C
การเตรียมอะลูมิเนียมจากออกไซด์
อิเล็กโทรไลซิสของอะลูมิเนียมออกไซด์
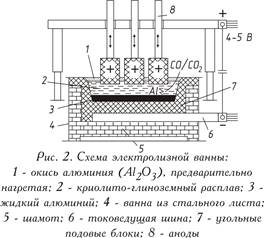 การลดอะลูมิเนียมออกไซด์ด้วยไฟฟ้าที่ละลายในการหลอมที่ใช้ไครโอไลท์จะดำเนินการที่อุณหภูมิ 950-970°C ในอิเล็กโทรไลเซอร์ อิเล็กโทรไลเซอร์ประกอบด้วยอ่างที่เรียงรายไปด้วยบล็อกคาร์บอน ซึ่งอยู่ด้านล่างของที่จ่ายกระแสไฟฟ้า อลูมิเนียมเหลวที่ปล่อยออกมาบนเตาซึ่งทำหน้าที่เป็นแคโทดนั้นหนักกว่าเกลือหลอมเหลวของอิเล็กโทรไลต์ดังนั้นจึงถูกรวบรวมบนฐานถ่านหินจากจุดที่ถูกสูบออกมาเป็นระยะ (รูปที่ 2) แอโนดคาร์บอนจะถูกจุ่มลงในอิเล็กโทรไลต์ที่อยู่ด้านบน ซึ่งจะเผาไหม้ในบรรยากาศของออกซิเจนที่ปล่อยออกมาจากอลูมิเนียมออกไซด์ และปล่อยก๊าซคาร์บอนมอนอกไซด์ (CO) หรือก๊าซคาร์บอนไดออกไซด์ (CO2) ออกมา ในทางปฏิบัติ มีการใช้แอโนดสองประเภท:
การลดอะลูมิเนียมออกไซด์ด้วยไฟฟ้าที่ละลายในการหลอมที่ใช้ไครโอไลท์จะดำเนินการที่อุณหภูมิ 950-970°C ในอิเล็กโทรไลเซอร์ อิเล็กโทรไลเซอร์ประกอบด้วยอ่างที่เรียงรายไปด้วยบล็อกคาร์บอน ซึ่งอยู่ด้านล่างของที่จ่ายกระแสไฟฟ้า อลูมิเนียมเหลวที่ปล่อยออกมาบนเตาซึ่งทำหน้าที่เป็นแคโทดนั้นหนักกว่าเกลือหลอมเหลวของอิเล็กโทรไลต์ดังนั้นจึงถูกรวบรวมบนฐานถ่านหินจากจุดที่ถูกสูบออกมาเป็นระยะ (รูปที่ 2) แอโนดคาร์บอนจะถูกจุ่มลงในอิเล็กโทรไลต์ที่อยู่ด้านบน ซึ่งจะเผาไหม้ในบรรยากาศของออกซิเจนที่ปล่อยออกมาจากอลูมิเนียมออกไซด์ และปล่อยก๊าซคาร์บอนมอนอกไซด์ (CO) หรือก๊าซคาร์บอนไดออกไซด์ (CO2) ออกมา ในทางปฏิบัติ มีการใช้แอโนดสองประเภท:
ก) แอโนด Zederberg ที่เผาไหม้ตัวเองซึ่งประกอบด้วยก้อนอิฐที่เรียกว่า "ขนมปัง" ของมวล Zederberg (ถ่านหินเถ้าต่ำที่มีระดับน้ำมันดินถ่านหิน 25-35%) ยัดลงในเปลือกอลูมิเนียม ภายใต้อิทธิพลของอุณหภูมิสูงมวลแอโนดจะถูกเผา (เผา)
b) แอโนดแบบอบหรือ "ต่อเนื่อง" ที่ทำจากบล็อกคาร์บอนขนาดใหญ่ (เช่น 1900x600x500 มม. หนักประมาณ 1.1 ตัน)
ความแรงของกระแสในอิเล็กโทรไลเซอร์คือ 150,000 A ซึ่งเชื่อมต่อกับเครือข่ายแบบอนุกรมนั่นคือได้รับระบบ (ซีรีย์) - อิเล็กโทรไลเซอร์แถวยาว
แรงดันไฟฟ้าที่ใช้งานบนอ่าง 4-5 V สูงกว่าแรงดันไฟฟ้าที่อะลูมิเนียมออกไซด์สลายตัวอย่างมาก เนื่องจากการสูญเสียแรงดันไฟฟ้าในส่วนต่างๆ ของระบบเป็นสิ่งที่หลีกเลี่ยงไม่ได้ระหว่างการทำงาน ความสมดุลของวัตถุดิบและพลังงานในการผลิตอลูมิเนียม 1 ตันแสดงไว้ในรูปที่ 1 3.
อิเล็กโทรไลซิสของอะลูมิเนียมคลอไรด์ (วิธีแอลโค)
 ในถังปฏิกิริยา อะลูมิเนียมออกไซด์จะถูกแปลงเป็นอะลูมิเนียมคลอไรด์ก่อน จากนั้น ในอ่างที่มีฉนวนอย่างแน่นหนา จะเกิดอิเล็กโทรไลซิสของ AlCl 3 ที่ละลายในเกลือหลอมเหลวที่มี KCl และ NaCl เกิดขึ้น คลอรีนที่ปล่อยออกมาในระหว่างกระบวนการนี้จะถูกดูดออกและนำไปรีไซเคิล อลูมิเนียมจะเกาะอยู่บนแคโทด
ในถังปฏิกิริยา อะลูมิเนียมออกไซด์จะถูกแปลงเป็นอะลูมิเนียมคลอไรด์ก่อน จากนั้น ในอ่างที่มีฉนวนอย่างแน่นหนา จะเกิดอิเล็กโทรไลซิสของ AlCl 3 ที่ละลายในเกลือหลอมเหลวที่มี KCl และ NaCl เกิดขึ้น คลอรีนที่ปล่อยออกมาในระหว่างกระบวนการนี้จะถูกดูดออกและนำไปรีไซเคิล อลูมิเนียมจะเกาะอยู่บนแคโทด
ข้อดีของวิธีนี้เหนืออิเล็กโทรลิซิสที่มีอยู่ของการหลอมไครโอไลท์-อลูมินาเหลว (อัล 2 O 3 ละลายในไครโอไลท์ Na 3 AlF 6) คือ: ประหยัดพลังงานได้มากถึง 30%; ความเป็นไปได้ของการใช้อะลูมิเนียมออกไซด์ซึ่งไม่เหมาะสำหรับอิเล็กโทรไลซิสแบบเดิม (เช่น Al 2 O 3 ที่มีปริมาณซิลิคอนสูง) แทนที่ไครโอไลท์ราคาแพงด้วยเกลือราคาถูก หายจากอันตรายจากการปล่อยฟลูออไรด์
การลดอะลูมิเนียมคลอไรด์ด้วยแมงกานีส (วิธี Toth)
 เมื่อรีดิวซ์ด้วยแมงกานีส อลูมิเนียมจะถูกปล่อยออกมาจากอะลูมิเนียมคลอไรด์ สารปนเปื้อนที่เกี่ยวข้องกับคลอรีนจะถูกปล่อยออกจากกระแสแมงกานีสคลอไรด์ผ่านการควบคุมการควบแน่น เมื่อคลอรีนถูกปล่อยออกมา แมงกานีสคลอไรด์จะถูกออกซิไดซ์เป็นแมงกานีสออกไซด์ จากนั้นจึงรีดิวซ์เป็นแมงกานีส เหมาะสำหรับการใช้งานขั้นที่สอง ข้อมูลในสิ่งพิมพ์ที่มีอยู่ไม่ถูกต้องมาก ดังนั้นในกรณีนี้จำเป็นต้องละทิ้งการประเมินวิธีการดังกล่าว
เมื่อรีดิวซ์ด้วยแมงกานีส อลูมิเนียมจะถูกปล่อยออกมาจากอะลูมิเนียมคลอไรด์ สารปนเปื้อนที่เกี่ยวข้องกับคลอรีนจะถูกปล่อยออกจากกระแสแมงกานีสคลอไรด์ผ่านการควบคุมการควบแน่น เมื่อคลอรีนถูกปล่อยออกมา แมงกานีสคลอไรด์จะถูกออกซิไดซ์เป็นแมงกานีสออกไซด์ จากนั้นจึงรีดิวซ์เป็นแมงกานีส เหมาะสำหรับการใช้งานขั้นที่สอง ข้อมูลในสิ่งพิมพ์ที่มีอยู่ไม่ถูกต้องมาก ดังนั้นในกรณีนี้จำเป็นต้องละทิ้งการประเมินวิธีการดังกล่าว
การได้รับอลูมิเนียมบริสุทธิ์
สำหรับอะลูมิเนียม การกลั่นอิเล็กโทรไลซิสด้วยการสลายตัวของสารละลายเกลือในน้ำนั้นเป็นไปไม่ได้ เนื่องจากเพื่อวัตถุประสงค์บางประการระดับการทำให้บริสุทธิ์ของอลูมิเนียมอุตสาหกรรม (Al 99.5 - Al 99.8) ที่ได้จากอิเล็กโทรไลซิสของการหลอมด้วยไครโอไลท์ - อลูมินานั้นไม่เพียงพอแม้แต่อลูมิเนียมที่บริสุทธิ์กว่า (Al 99, 99 R) ก็ได้จากอลูมิเนียมอุตสาหกรรมหรือเศษโลหะด้วย การกลั่น วิธีการกลั่นที่รู้จักกันดีที่สุดคือการอิเล็กโทรไลซิสแบบสามชั้น
กลั่นด้วยกระแสไฟฟ้าสามชั้น
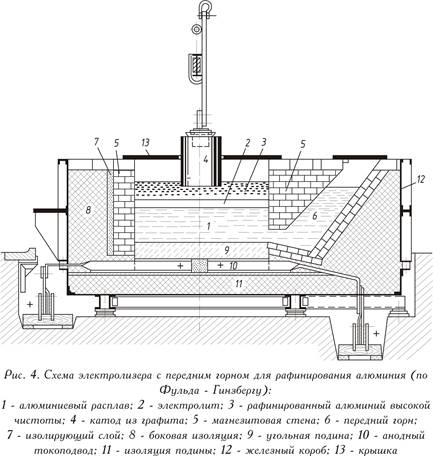
หุ้มด้วยแผ่นเหล็กซึ่งทำงานด้วยไฟฟ้ากระแสตรง (แสดงในรูปที่ 4 - ดูด้านบน) อ่างกลั่นประกอบด้วยเตาถ่านหินที่มีสายไฟในปัจจุบันและบุด้วยแมกนีไซต์ที่เป็นฉนวนความร้อน ตรงกันข้ามกับการแยกสลายด้วยไฟฟ้าของการหลอมไครโอไลท์-อลูมินา ตามกฎแล้วขั้วบวกคือโลหะหลอมเหลวที่ได้รับการขัดเกลา (ชั้นขั้วบวกด้านล่าง) อิเล็กโทรไลต์ประกอบด้วยฟลูออไรด์บริสุทธิ์หรือส่วนผสมของแบเรียมคลอไรด์กับอะลูมิเนียมและโซเดียมฟลูออไรด์ (ชั้นกลาง) อะลูมิเนียมที่ละลายจากชั้นแอโนดในอิเล็กโทรไลต์ ถูกปล่อยออกมาเหนืออิเล็กโทรไลต์ (ชั้นแคโทดด้านบน) โลหะบริสุทธิ์ทำหน้าที่เป็นแคโทด กระแสไฟฟ้าจะถูกส่งไปยังชั้นแคโทดโดยอิเล็กโทรดกราไฟท์
อ่างทำงานที่อุณหภูมิ 750-800°C ปริมาณการใช้ไฟฟ้าคือ 20 kWh ต่ออะลูมิเนียมบริสุทธิ์ 1 กิโลกรัม ซึ่งสูงกว่าอะลูมิเนียมอิเล็กโทรไลซิสทั่วไปเล็กน้อย
โลหะแอโนดมี Cu 25-35%; สังกะสี 7-12%; 6-9% ศรี; Fe มากถึง 5% และแมงกานีส นิกเกิล ตะกั่วและดีบุกจำนวนเล็กน้อย ส่วนที่เหลือ (40-55%) เป็นอลูมิเนียม โลหะหนักและซิลิคอนทั้งหมดจะยังคงอยู่ในชั้นแอโนดระหว่างการกลั่น การมีแมกนีเซียมในอิเล็กโทรไลต์ทำให้เกิดการเปลี่ยนแปลงที่ไม่พึงประสงค์ในองค์ประกอบของอิเล็กโทรไลต์หรือเกิดตะกรันอย่างรุนแรง ในการกำจัดแมกนีเซียม ตะกรันที่มีแมกนีเซียมจะถูกบำบัดด้วยฟลักซ์หรือก๊าซคลอรีน
จากการกลั่น ทำให้ได้อะลูมิเนียมบริสุทธิ์ (99.99%) และผลิตภัณฑ์แยก (ผลิตภัณฑ์ Ziger) ซึ่งประกอบด้วยโลหะหนักและซิลิคอน และถูกปล่อยออกมาในรูปของสารละลายอัลคาไลน์และกากผลึก สารละลายอัลคาไลน์ถือเป็นของเสีย และกากของแข็งจะถูกใช้สำหรับการดีออกซิเดชัน
อลูมิเนียมบริสุทธิ์มักจะมีองค์ประกอบดังต่อไปนี้%: Fe 0.0005-0.002; ศรี 0.002-0.005; ลูกบาศ์ก 0.0005-0.002; สังกะสี 0.0005-0.002; ร่องรอยมก.; อัลส่วนที่เหลือ
อลูมิเนียมที่ผ่านการกลั่นแล้วจะถูกแปรรูปเป็นผลิตภัณฑ์กึ่งสำเร็จรูปในองค์ประกอบที่ระบุหรือเจือด้วยแมกนีเซียม (ดูตารางที่ 1.2)
ตารางที่ 1.2องค์ประกอบทางเคมีของอะลูมิเนียมที่มีความบริสุทธิ์สูงและอะลูมิเนียมปฐมภูมิตาม ดิน 1712, แผ่นที่ 1.
| ยี่ห้อ | ตัวเลข | สิ่งเจือปนที่อนุญาต*, % | |||||||
| ทั้งหมด | รวมทั้ง | ||||||||
| ศรี | เฟ | Ti | ลูกบาศ์ก | สังกะสี | อื่น | ||||
| A199.99R | 3.0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 | |
| A199.9H | 3.0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 | |
| A199.8H | 3.0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199.7H | 3.0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199.5H** | 3.0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 | |
| A199H | 3.0200 | 1,0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 | |
* เท่าที่เป็นไปได้ในการพิจารณาโดยใช้วิธีการวิจัยแบบเดิม ** อลูมิเนียมบริสุทธิ์สำหรับวิศวกรรมไฟฟ้า (ตัวนำอลูมิเนียม) มีจำหน่ายในรูปของอะลูมิเนียมปฐมภูมิ 99.5 โดยมีปริมาณไม่เกิน 0.03% (Ti + Cr + V + Mn) ในกรณีนี้เรียกว่า E-A1 หมายเลขวัสดุ 3.0256 มิฉะนั้นจะเป็นไปตามมาตรฐาน VDE-0202 |
|||||||||
การกลั่นด้วยสารประกอบออร์กาโนอลูมิเนียมและการถลุงโซน
อลูมิเนียมที่มีระดับความบริสุทธิ์สูงกว่าเกรด A1 99.99 R สามารถรับได้โดยการกลั่นด้วยไฟฟ้าของอลูมิเนียมบริสุทธิ์หรือบริสุทธิ์ในเชิงพาณิชย์โดยใช้สารประกอบออร์กาโนอลูมิเนียมเชิงซ้อนของอลูมิเนียมเป็นอิเล็กโทรไลต์ อิเล็กโทรไลซิสเกิดขึ้นที่อุณหภูมิประมาณ 1,000°C ระหว่างอิเล็กโทรไลต์อะลูมิเนียมที่เป็นของแข็ง และมีหลักการคล้ายกับการกลั่นอิเล็กโทรไลซิสของทองแดง ลักษณะของอิเล็กโทรไลต์เป็นตัวกำหนดความจำเป็นในการทำงานโดยไม่มีอากาศเข้าถึงและมีความหนาแน่นกระแสต่ำ
อิเล็กโทรไลซิสเพื่อการกลั่นชนิดนี้ ซึ่งเริ่มแรกใช้เฉพาะในระดับห้องปฏิบัติการเท่านั้น และได้ดำเนินการแล้วในระดับอุตสาหกรรมขนาดเล็ก โดยมีการผลิตโลหะหลายตันต่อปี ระดับการทำให้บริสุทธิ์เล็กน้อยของโลหะที่ได้คือ 99.999-99.9999% การใช้งานที่เป็นไปได้สำหรับโลหะที่มีความบริสุทธิ์นี้ ได้แก่ วิศวกรรมไฟฟ้าและอิเล็กทรอนิกส์แบบแช่แข็ง
สามารถใช้วิธีการกลั่นที่ได้รับการพิจารณาในการชุบด้วยไฟฟ้าได้
ความบริสุทธิ์ที่สูงกว่า - ในนามสูงถึง A1 99.99999 - สามารถรับได้จากการหลอมโลหะในโซนที่ตามมา เมื่อแปรรูปอะลูมิเนียมที่มีความบริสุทธิ์สูงเป็นผลิตภัณฑ์กึ่งสำเร็จรูป แผ่นหรือสายไฟ จำเป็นต้องคำนึงถึง อุณหภูมิต่ำการตกผลึกของโลหะ ให้ใช้ความระมัดระวังเป็นพิเศษ คุณสมบัติที่โดดเด่นของโลหะที่ผ่านการกลั่นแล้วคือค่าการนำไฟฟ้าสูงในช่วงอุณหภูมิแช่แข็ง
การผลิตอะลูมิเนียมทุติยภูมิ
การรีไซเคิลวัตถุดิบทุติยภูมิและของเสียจากการผลิตนั้นให้ผลกำไรเชิงเศรษฐกิจ โลหะผสมทุติยภูมิที่ได้นั้นสามารถตอบสนองความต้องการอลูมิเนียมได้ประมาณ 25%
 พื้นที่ที่สำคัญที่สุดในการใช้งานโลหะผสมทุติยภูมิคือการผลิตการหล่อรูปทรงอลูมิเนียม ใน DIN 1725 แผ่นที่ 2 พร้อมด้วยเกรดโลหะผสมมาตรฐาน มีการระบุเกรดโลหะผสมจำนวนมากที่ผลิตโดยโรงหล่อไว้ด้วย รายชื่อโลหะผสมที่ผลิตโดยโรงงานเหล่านี้ประกอบด้วยโลหะผสมที่ไม่ได้มาตรฐานบางชนิดนอกเหนือจากโลหะผสมมาตรฐาน
พื้นที่ที่สำคัญที่สุดในการใช้งานโลหะผสมทุติยภูมิคือการผลิตการหล่อรูปทรงอลูมิเนียม ใน DIN 1725 แผ่นที่ 2 พร้อมด้วยเกรดโลหะผสมมาตรฐาน มีการระบุเกรดโลหะผสมจำนวนมากที่ผลิตโดยโรงหล่อไว้ด้วย รายชื่อโลหะผสมที่ผลิตโดยโรงงานเหล่านี้ประกอบด้วยโลหะผสมที่ไม่ได้มาตรฐานบางชนิดนอกเหนือจากโลหะผสมมาตรฐาน
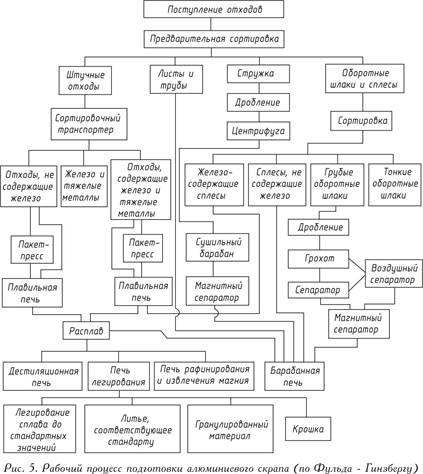
การเตรียมเศษอะลูมิเนียมอย่างไร้ที่ติในสัดส่วนที่หลากหลายสามารถทำได้ในโรงถลุงที่มีอุปกรณ์พิเศษเท่านั้น แนวคิดเกี่ยวกับกระบวนการทำงานที่ซับซ้อนในโรงงานดังกล่าวแสดงไว้ในรูปที่ 1 5.
ของเสียจะถูกละลายหลังจากการคัดแยกเบื้องต้นอย่างคร่าวๆ เหล็ก, นิกเกิลหรือทองแดงที่มีอยู่ในของเสียนี้ซึ่งมีจุดหลอมเหลวซึ่งสูงกว่าจุดหลอมเหลวของอลูมิเนียมเมื่อละลายในเตาหลอมจะยังคงอยู่ในนั้นและอลูมิเนียมจะถูกหลอม ในการกำจัดสิ่งเจือปนที่ไม่ใช่โลหะ เช่น ออกไซด์ ไนไตรด์ คาร์ไบด์ หรือก๊าซ ออกจากของเสีย โลหะหลอมเหลวจะถูกบำบัดด้วยเกลือหรือเป่าด้วยก๊าซ - คลอรีนหรือไนโตรเจน (อย่างสมเหตุสมผล)
ทราบวิธีการต่างๆ ในการกำจัดสิ่งเจือปนของโลหะออกจากโลหะหลอม เช่น วิธีเติมแมกนีเซียมและการดูดฝุ่น - วิธี Becksche การเติมสังกะสีหรือปรอทตามด้วยการอพยพ - วิธีซับฮาโลเจน การกำจัดแมกนีเซียมถูกจำกัดโดยการนำคลอรีนเข้าไปในโลหะหลอมเหลว ด้วยการแนะนำสารเติมแต่งที่กำหนดอย่างแม่นยำโดยองค์ประกอบของการหลอมละลาย จะได้โลหะผสมหล่อที่กำหนด
การผลิตอะลูมิเนียมที่มีความบริสุทธิ์ทางเทคนิค
วิธีการอิเล็กโทรไลต์เป็นวิธีเดียวที่ใช้กันทั่วโลกสำหรับการผลิตโลหะอลูมิเนียมที่มีความบริสุทธิ์ทางเทคนิค วิธีการอื่นๆ ทั้งหมด (ซิงค์ความร้อน คาร์บิโดเทอร์มอล ซับคลอไรด์ ไนไตรด์ ฯลฯ) ซึ่งสามารถสกัดอะลูมิเนียมจากแร่อะลูมิเนียมได้ได้รับการพัฒนาในห้องปฏิบัติการและระดับอุตสาหกรรมนำร่อง แต่ยังไม่พบการประยุกต์ใช้ในทางปฏิบัติ
ในการผลิตโลหะผสมอลูมิเนียมซิลิกอนนั้นใช้วิธีการความร้อนด้วยไฟฟ้าซึ่งพัฒนาและนำไปใช้ในระดับอุตสาหกรรมในสหภาพโซเวียตเป็นครั้งแรกซึ่งประสบความสำเร็จ ประกอบด้วยสองขั้นตอน: ในระยะแรกโลหะผสมอลูมิเนียม - ซิลิคอนหลักที่มี 60-63% Al ได้มาจากการลดแร่อลูมิเนียม - ซิลิคอนโดยตรงในเตาไฟฟ้าแร่ความร้อน ในขั้นตอนที่สอง โลหะผสมปฐมภูมิจะถูกเจือจางด้วยอะลูมิเนียมเชิงเทคนิค ทำให้เกิดไซลูมินและโลหะผสมอะลูมิเนียม-ซิลิคอนหล่อและขึ้นรูปอื่นๆ การวิจัยอยู่ระหว่างดำเนินการเพื่อสกัดอะลูมิเนียมที่มีความบริสุทธิ์ทางเทคนิคจากโลหะผสมปฐมภูมิ
โดยทั่วไป การผลิตอะลูมิเนียมโดยวิธีอิเล็กโตรไลติก ได้แก่ การผลิตอลูมินา (อะลูมิเนียมออกไซด์) จากแร่อะลูมิเนียม การผลิตเกลือฟลูออไรด์ (ไครโอไลท์ อะลูมิเนียมฟลูออไรด์ และโซเดียมฟลูออไรด์) การผลิตมวลแอโนดคาร์บอน แอโนดคาร์บอนที่ถูกเผา และ บล็อกแคโทดและวัสดุซับในอื่นๆ รวมถึงการผลิตอะลูมิเนียมด้วยไฟฟ้าซึ่งเป็นขั้นตอนสุดท้ายของโลหะวิทยาอะลูมิเนียมสมัยใหม่
ลักษณะเฉพาะสำหรับการผลิตอลูมินาเกลือฟลูออไรด์และผลิตภัณฑ์คาร์บอนเป็นข้อกำหนดสำหรับระดับความบริสุทธิ์สูงสุดของวัสดุเหล่านี้เนื่องจากการหลอมของไครโอไลท์ - อลูมินาภายใต้กระบวนการอิเล็กโทรไลซิสไม่ควรมีสิ่งเจือปนขององค์ประกอบทางไฟฟ้ามากกว่าอลูมิเนียมซึ่งปล่อยออกมาที่แคโทดใน อันดับแรกจะก่อให้เกิดมลพิษต่อโลหะ
ในเกรดอลูมินา G-00, G-0 และ G-1 ซึ่งส่วนใหญ่ใช้ในการอิเล็กโทรไลซิส ปริมาณ SiO 2 คือ 0.02-0.05%, aFe 2 O 3 - 0.03-0.05% Cryolite ประกอบด้วย SiO 2 โดยเฉลี่ย 0.36-0.38% และ 0.05-0.06% Fe 2 O 3 อลูมิเนียมฟลูออไรด์ประกอบด้วย 0.30-0.35% (SiO 2 + Fe 2 O 3) มวลแอโนดประกอบด้วย SiO 2 ไม่เกิน 0.25% และ Fe 2 O 3 0.20%
แร่อลูมิเนียมที่สำคัญที่สุดในการสกัดอลูมินาคือแร่บอกไซต์ ในอะลูมิเนียมมีอะลูมิเนียมอยู่ในรูปของอะลูมิเนียมไฮดรอกไซด์ ในสหภาพโซเวียต นอกเหนือจากแร่อะลูมิเนียมแล้ว หินเนฟีลีนยังใช้ในการผลิตอลูมินา - โซเดียมและโพแทสเซียมอะลูมิโนซิลิเกต เช่นเดียวกับหินอลูไนต์ซึ่งพบอลูมิเนียมในรูปของซัลเฟต วัตถุดิบสำหรับการผลิตมวลแอโนดและบล็อกแอโนดแบบอบคือวัสดุคาร์บอนบริสุทธิ์ - ปิโตรเลียมหรือพิตช์โค้กและพิตช์น้ำมันถ่านหินเป็นสารยึดเกาะ และสำหรับการผลิตไครโอไลท์และเกลือฟลูออไรด์อื่นๆ - แคลเซียมฟลูออไรด์ (ฟลูออร์สปาร์)
ในระหว่างการผลิตอลูมิเนียมด้วยไฟฟ้า อลูมินา Al 2 O 3 ซึ่งละลายในไครโอไลท์ Na 3 AlF 6 หลอมละลาย จะสลายตัวทางเคมีไฟฟ้าด้วยการปล่อยประจุบวกของอะลูมิเนียมที่แคโทด (อลูมิเนียมเหลว) และไอออนที่มีออกซิเจน (ไอออนออกซิเจน) ที่คาร์บอน ขั้วบวก.
โดย ความคิดที่ทันสมัย, ไครโอไลท์ในสถานะหลอมเหลวแยกตัวออกเป็นไอออน และ: และ อลูมินา - เป็นไอออนเชิงซ้อน และ: ![]() ซึ่งอยู่ในสมดุลกับไอออนเชิงเดี่ยว:
ซึ่งอยู่ในสมดุลกับไอออนเชิงเดี่ยว: ![]() ,
, ![]() .
.
กระบวนการหลักที่เกิดขึ้นที่แคโทดคือการลดไอออนของอะลูมิเนียมไตรวาเลนท์: Al 3+ + 3 จ→ อัล (I)
นอกเหนือจากกระบวนการหลักแล้ว ยังสามารถปล่อยไอออนอะลูมิเนียมไตรวาเลนต์ที่ไม่สมบูรณ์ได้ด้วยการก่อตัวของไอออนโมโนวาเลนท์: Al 3+ + 2 จ→ Al + (II) และสุดท้ายคือการปล่อยไอออนโมโนวาเลนต์พร้อมกับการปล่อยโลหะ: Al + + จ→ อัล(III)
ภายใต้เงื่อนไขบางประการ (ความเข้มข้นของ Na + ไอออนค่อนข้างสูง ความร้อนฯลฯ) อาจเกิดการคายประจุของโซเดียมไอออนเมื่อมีการปล่อยโลหะ: Na + + จ→ นา(IV) ปฏิกิริยา (II) และ (IV) ทำให้กระแสเอาต์พุตของอะลูมิเนียมลดลง
ไอออนออกซิเจนจะถูกปล่อยออกมาที่ขั้วบวกของคาร์บอน: 2O 2– – 4 จ→ โอ 2 . อย่างไรก็ตาม ออกซิเจนจะไม่ถูกปล่อยออกมาในรูปแบบอิสระ เนื่องจากมันจะออกซิไดซ์คาร์บอนของขั้วบวกจนกลายเป็นส่วนผสมของ CO 2 และ CO
ปฏิกิริยาโดยรวมที่เกิดขึ้นในอิเล็กโทรไลเซอร์สามารถแสดงได้ด้วยสมการ Al 2 O 3 + xค ↔ 2อัล + (2 x–3)คาร์บอนไดออกไซด์ + (3– x)CO2 .
องค์ประกอบของอิเล็กโทรไลต์ของอิเล็กโทรไลเซอร์อลูมิเนียมอุตสาหกรรมนอกเหนือจากส่วนประกอบหลัก - ไครโอไลท์, อลูมิเนียมฟลูออไรด์และอลูมินาแล้วยังรวมถึงเกลืออื่น ๆ ในปริมาณเล็กน้อย (รวมมากถึง 8-9%) - CaF 2, MgF 2, NaCl และ LiF (สารเติมแต่ง) ซึ่งปรับปรุงคุณสมบัติทางกายภาพและเคมีบางอย่างของอิเล็กโทรไลต์ และด้วยเหตุนี้จึงเพิ่มประสิทธิภาพของอิเล็กโทรไลเซอร์ ปริมาณอลูมินาสูงสุดในอิเล็กโทรไลต์มักจะอยู่ที่ 6-8% ซึ่งจะลดลงในระหว่างกระบวนการอิเล็กโทรไลซิส เมื่ออิเล็กโทรไลต์หมดอลูมินา จะมีการนำอลูมินาอีกส่วนหนึ่งเข้าไป สำหรับการทำงานปกติของอิเล็กโทรไลเซอร์อะลูมิเนียม อัตราส่วน NaF:AlF 3 ในอิเล็กโทรไลต์จะคงอยู่ภายในช่วง 2.7-2.8 โดยการเติมไครโอไลท์และอะลูมิเนียมฟลูออไรด์บางส่วน
ในการผลิตอะลูมิเนียม จะใช้อิเล็กโทรไลเซอร์ที่มีคาร์บอนแอโนดอบเองและจ่ายกระแสไฟด้านข้างหรือด้านบน เช่นเดียวกับอิเล็กโทรไลเซอร์ที่มีคาร์บอนแอโนดอบล่วงหน้า การออกแบบอิเล็กโตรไลเซอร์ที่มีแนวโน้มมากที่สุดพร้อมขั้วบวกแบบอบ ซึ่งทำให้สามารถเพิ่มกำลังหน่วยของยูนิตได้ ลดการใช้ไฟฟ้ากระแสตรงเฉพาะสำหรับอิเล็กโทรลิซิส รับโลหะที่บริสุทธิ์ยิ่งขึ้น ปรับปรุงสภาพการทำงานที่ถูกสุขลักษณะและถูกสุขลักษณะ และลดการปล่อยสารที่เป็นอันตราย สู่ชั้นบรรยากาศ
พารามิเตอร์ทางเทคนิคหลักและตัวบ่งชี้ประสิทธิภาพของอิเล็กโทรไลเซอร์อะลูมิเนียมประเภทต่างๆ แสดงไว้ในตาราง 1 1.3.
ตารางที่ 1.3
พารามิเตอร์ทางเทคนิคหลักและตัวบ่งชี้ประสิทธิภาพของอะลูมิเนียมอิเล็กโทรไลเซอร์
| พารามิเตอร์และตัวบ่งชี้ | ด้วยขั้วบวกที่อบเอง | ด้วยขั้วบวกอบ | |
ด้านข้าง อุปทานในปัจจุบัน |
อุปทานปัจจุบันบน | ||
| ความแรงปัจจุบัน kA | 60-120 | 60-155 | 160-255 |
| ผลผลิตรายวันของอิเล็กโทรไลเซอร์, t | 0,42-0,85 | 0,40-1,10 | 1,10-1,74 |
| ความหนาแน่นกระแสขั้วบวก, A/cm 2 | 0,80-0,90 | 0,65-0,70 | 0,70-0,89 |
| แรงดันไฟฟ้าเฉลี่ยบนอิเล็กโทรไลเซอร์, V | 4,45-4,65 | 4,50-4,70 | 4,30-4,50 |
| เอาท์พุตปัจจุบัน % | 85-88 | 84-86 | 85-89 |
| ค่าสัมประสิทธิ์การบริโภคต่ออลูมิเนียม 1 ตัน: | |||
| ไฟฟ้ากระแสตรง, กิโลวัตต์ชั่วโมง | 15100-16200 | 15500-17300 | 14500-15500 |
| อลูมินากก | 1920-1940 | 1920-1940 | 1920-1940 |
| มวลแอโนด, กก | 520-560 | 560-620 | - |
| แอโนดอบกก | - | - | 540-600 |
| เกลือฟลูออไรด์ในรูปของฟลูออรีน, กก | 20-30 | 25-35 | 15-25 |
อลูมิเนียมปฐมภูมิที่สกัดจากอิเล็กโทรไลเซอร์ (อลูมิเนียมดิบ) มีสารเจือปนจำนวนหนึ่ง ซึ่งสามารถแบ่งออกเป็นสามกลุ่ม: อโลหะ (เกลือฟลูออไรด์ α- และ γ-อลูมินา, อลูมิเนียมคาร์ไบด์และไนไตรด์, อนุภาคคาร์บอนที่ถูกกักขังโดยกลไกเมื่อเทโลหะจากอิเล็กโทรไลเซอร์) โลหะ (เหล็ก ซิลิคอน) ที่มาจากวัตถุดิบ วัสดุถ่านหิน และองค์ประกอบโครงสร้างของอิเล็กโทรไลเซอร์ ก๊าซ - ไฮโดรเจนส่วนใหญ่ซึ่งเกิดขึ้นในโลหะอันเป็นผลมาจากการสลายตัวด้วยไฟฟ้าของน้ำที่เข้าสู่อิเล็กโทรไลต์ด้วยวัตถุดิบ
ในบรรดาโลหะเจือปน นอกเหนือจากเหล็กและซิลิคอนแล้ว ยังมีแกลเลียม สังกะสี ไทเทเนียม แมงกานีส โซเดียม วาเนเดียม โครเมียม และทองแดงในปริมาณมากที่สุดอีกด้วย เนื้อหาของสิ่งเหล่านี้และสิ่งสกปรกขนาดเล็กอื่นๆ ของโลหะใน อลูมิเนียมด้วยไฟฟ้าได้รับด้านล่าง %:
แหล่งที่มาหลักของโลหะปนเปื้อนขนาดเล็กในอะลูมิเนียมคืออลูมินา ซึ่งอาจมีแกลเลียม สังกะสี โพแทสเซียม ฟอสฟอรัส ซัลเฟอร์ วาเนเดียม ไทเทเนียม และโครเมียม ขึ้นอยู่กับประเภทของวัตถุดิบ วัสดุคาร์บอน (มวลแอโนด แอโนดอบ ผลิตภัณฑ์แคโทด) ทำหน้าที่เป็นแหล่งของสิ่งเจือปนขนาดเล็ก เช่น วาเนเดียม ไทเทเนียม แมงกานีส สังกะสี
ด้วยกระแสไฟฟ้าของการหลอมไครโอไลท์-อลูมินา โดยมีเงื่อนไขว่าต้องใช้วัสดุตั้งต้นบริสุทธิ์ (โดยหลักแล้วคือวัสดุอลูมินาและคาร์บอน) จึงเป็นไปได้ที่จะได้อะลูมิเนียมดิบเกรด A85 และ A8 (99.85 และ 99.80%) โลหะส่วนใหญ่ในเกรดเหล่านี้ (60-70% ของผลผลิตทั้งหมด) ผลิตในอิเล็กโทรไลเซอร์ที่มีขั้วบวกแบบอบ เช่นเดียวกับในอิเล็กโทรไลเซอร์ที่มีกระแสไฟด้านข้าง (มากถึง 70% ของการผลิตทั้งหมด) ในอิเล็กโทรไลเซอร์ที่มีขั้วบวกแบบอบตัวเองและมีกระแสไฟบน เอาต์พุตของอะลูมิเนียมดิบเกรด A8 จะต่ำ (1-3%) และไม่สามารถรับเกรดโลหะ A85 ได้เนื่องจากมีเหล็กเจือปนจำนวนมากเข้าสู่อะลูมิเนียมจากแหล่งที่ไม่ใช่วัตถุดิบ (หมุดแอโนด, ส่วนเหล็กหล่อของตัวสะสมก๊าซ, เครื่องมือทางเทคโนโลยี, หน่วยแคโทด)
อะลูมิเนียมปฐมภูมิหลอมเหลวซึ่งสกัดจากเครื่องอิเล็กโตรไลเซอร์โดยใช้กระบวยสุญญากาศ เข้าสู่แผนกโรงหล่อเพื่อทำการกลั่นเพื่อกำจัดสิ่งเจือปนที่ไม่ใช่โลหะและก๊าซ และนำไปแปรรูปเป็นผลิตภัณฑ์เชิงพาณิชย์ (หมู แท่งทรงกระบอกและแท่งแบน เหล็กลวด ฯลฯ) ก่อนการหล่อ อลูมิเนียมดิบจะถูกเก็บไว้ในสถานะหลอมเหลวในเตาต้านทานไฟฟ้า (เครื่องผสม) หรือในเตาก๊าซสะท้อนกลับ ในเตาเผาเหล่านี้ พวกเขาไม่เพียงแต่ผสมส่วนของอลูมิเนียมเหลวที่มีองค์ประกอบต่างๆ อย่างมีเหตุผล แต่ยังทำความสะอาดบางส่วนจากการรวมตัวที่ไม่ใช่โลหะ ฟิล์มออกไซด์ และโซเดียมอีกด้วย
อลูมิเนียมถูกหล่อจากเครื่องผสมให้เป็นแท่งโลหะโดยใช้เครื่องหล่อแบบสายพานลำเลียง แท่งทรงกระบอกและแท่งแบนผลิตโดยการหล่อแบบกึ่งต่อเนื่อง และใช้หน่วยพิเศษของการหล่อและการรีดแบบรวมเพื่อผลิตเหล็กลวด
ที่โรงถลุงอะลูมิเนียมในประเทศ เมื่อทำการหล่อหลอม อลูมิเนียมที่มาจากเครื่องผสมลงในเครื่องตกผลึกของเครื่องหล่อจะต้องผ่านกระบวนการกลั่นที่ง่ายที่สุด โดยกรองการหลอมผ่านตาข่ายไฟเบอร์กลาสที่มีเซลล์ขนาดตั้งแต่ 0.6 × 0.6 ถึง 1.7 × 1.7 มม. วิธีนี้ช่วยให้คุณทำความสะอาดอะลูมิเนียมได้เฉพาะเมื่อมีออกไซด์ที่หยาบมากเท่านั้น วิธีการขั้นสูงกว่านั้นคือการกรองของเหลวที่หลอมละลายผ่านตาข่ายไฟเบอร์กลาสในการไหลขึ้น ด้วยวิธีการกรองนี้ อนุภาคของออกไซด์ที่รวมอยู่ซึ่งชนกับตาข่ายจะไม่ถูกดักจับโดยการไหลของของเหลว แต่จะถูกสะสมไว้ที่ด้านล่างของร่องหล่อ
หากต้องการทำให้อะลูมิเนียมบริสุทธิ์จากทั้งสิ่งเจือปนที่ไม่ใช่โลหะและไฮโดรเจนไปพร้อมๆ กัน จึงใช้วิธีการกรองผ่านตัวกรองฟลักซ์ร่วมกับการไล่ไนโตรเจนได้สำเร็จ อิเล็กโทรไลต์ที่เป็นกรดของอิเล็กโทรไลเซอร์อะลูมิเนียมสามารถใช้เป็นฟลักซ์ได้ จากผลของการทำให้บริสุทธิ์นี้ ปริมาณไฮโดรเจนในอลูมิเนียมจะลดลงจาก 0.22 เป็น 0.16 ซม. 3 ต่อโลหะ 100 กรัม
ในอะลูมิเนียมปฐมภูมิที่ใช้ในการผลิตโลหะผสมของระบบ Al-Mg ปริมาณโซเดียมไม่ควรเกิน 0.001% นี่เป็นเพราะความจริงที่ว่าการมีโซเดียมในโลหะผสมเหล่านี้ทำให้คุณสมบัติทางกลและประสิทธิภาพอื่น ๆ ของผลิตภัณฑ์ที่ใช้ในหลายภาคส่วนของเศรษฐกิจของประเทศแย่ลง
ที่สุด วิธีการที่มีประสิทธิภาพการกลั่นอะลูมิเนียมพร้อมกันจากโซเดียม ไฮโดรเจน และสิ่งสกปรกที่ไม่ใช่โลหะ เป่าโลหะหลอมเหลวด้วยส่วนผสมก๊าซไนโตรเจนกับคลอรีน 2-10% นำเข้าสู่การหลอมในรูปของฟองขนาดเล็กโดยใช้อุปกรณ์พิเศษ วิธีการกลั่นนี้ทำให้สามารถลดปริมาณโซเดียมในอะลูมิเนียมลงเหลือ 0.0003-0.001% โดยใช้ส่วนผสมก๊าซ 0.8 ถึง 1.5 ม.3 /ตันของโลหะ
ปริมาณการใช้ไฟฟ้าสำหรับการผลิตอลูมิเนียมเชิงพาณิชย์ 1 ตันจากโลหะดิบโดยใช้เตาไฟฟ้าคือ 150-200 kWh การสูญเสียโลหะที่แก้ไขไม่ได้ในขั้นตอนการหล่อจะเท่ากับ 1.5-5% ขึ้นอยู่กับประเภทของผลิตภัณฑ์เชิงพาณิชย์
ผลิตอะลูมิเนียมที่มีความบริสุทธิ์สูง
เพื่อให้ได้อะลูมิเนียมที่มีความบริสุทธิ์สูง (เกรด A995-A95) อลูมิเนียมปฐมภูมิที่มีความบริสุทธิ์ทางเทคนิคจะต้องผ่านการกลั่นด้วยไฟฟ้า ทำให้สามารถลดปริมาณโลหะและก๊าซเจือปนในอลูมิเนียมได้ และส่งผลให้ค่าการนำไฟฟ้า ความเหนียว การสะท้อนแสง และความต้านทานการกัดกร่อนเพิ่มขึ้นอย่างมาก
การกลั่นอลูมิเนียมด้วยไฟฟ้าจะดำเนินการโดยอิเล็กโทรไลซิสของเกลือหลอมเหลวโดยใช้วิธีสามชั้น สาระสำคัญของวิธีการมีดังนี้ อิเล็กโทรไลเซอร์สำหรับการกลั่นมีชั้นหลอมเหลวสามชั้น ส่วนล่างที่หนักที่สุดจะอยู่ที่ด้านล่างที่เป็นสื่อกระแสไฟฟ้าและทำหน้าที่เป็นขั้วบวก เรียกว่าโลหะผสมแอโนดและเป็นโลหะผสมของอลูมิเนียมกลั่นกับทองแดง ซึ่งเพิ่มเข้าไปเพื่อทำให้ชั้นมีน้ำหนักมากขึ้น ชั้นกลางคืออิเล็กโทรไลต์หลอมเหลว ความหนาแน่นของมันน้อยกว่าความหนาแน่นของโลหะผสมแอโนดและสูงกว่าความหนาแน่นของอะลูมิเนียมที่ผ่านการกลั่นบริสุทธิ์ (แคโทด) ซึ่งอยู่เหนืออิเล็กโทรไลต์ (ชั้นของเหลวชั้นบนและชั้นที่สาม)
ในระหว่างการละลายขั้วบวก สิ่งเจือปนทั้งหมดที่มีอิเล็กโตรบวกมากกว่าอะลูมิเนียม (Fe, Si, Ti, Cu ฯลฯ) จะยังคงอยู่ในอัลลอยด์ขั้วบวกโดยไม่ผ่านเข้าไปในอิเล็กโทรไลต์ มีเพียงอะลูมิเนียมเท่านั้นที่จะละลายในขั้วบวก ซึ่งอยู่ในรูปของไอออน Al 3+ ผ่านเข้าไปในอิเล็กโทรไลต์: Al– 3 จ→ อัล 3+ .
ในระหว่างอิเล็กโทรไลซิส ไอออนของอลูมิเนียมจะถูกถ่ายโอนไปยังแคโทด ซึ่งจะถูกปล่อยออกมา: อัล 3+ + 3 จ→ อัล เป็นผลให้ชั้นของอะลูมิเนียมกลั่นหลอมเหลวสะสมอยู่บนแคโทด
หากโลหะผสมแอโนดมีสิ่งเจือปนที่มีอิเลคโตรเนกาติวิตีมากกว่าอะลูมิเนียม (เช่น Ba, Na, Mg, Ca) พวกมันก็สามารถละลายทางเคมีไฟฟ้าที่ขั้วบวกพร้อมกับอะลูมิเนียมและส่งผ่านเข้าไปในอิเล็กโทรไลต์ในรูปของไอออน เนื่องจากปริมาณสิ่งเจือปนทางอิเล็กโทรเนกาติวิตีในอะลูมิเนียมดิบมีน้อย จึงไม่สะสมอยู่ในอิเล็กโทรไลต์ในปริมาณที่เห็นได้ชัดเจน ในทางปฏิบัติแล้วไม่มีการคายประจุไอออนเหล่านี้ที่แคโทด เนื่องจากศักย์ไฟฟ้าของพวกมันมีประจุไฟฟ้ามากกว่าอะลูมิเนียม
อิเล็กโทรไลต์ที่ใช้ในการกลั่นอลูมิเนียมด้วยไฟฟ้าในสหภาพโซเวียตและในประเทศส่วนใหญ่เป็นอิเล็กโทรไลต์ฟลูออไรด์ - คลอไรด์ซึ่งมีองค์ประกอบคือ 55-60% BaCl 2, 35-40% AlF 4 + NaF และ 0-4% NaCl . อัตราส่วนโมลของ NaF: AlF 3 คงไว้ที่ 1.5-2.0; อุณหภูมิหลอมละลายของอิเล็กโทรไลต์ 720-730°C; อุณหภูมิของกระบวนการอิเล็กโทรไลซิสอยู่ที่ประมาณ 800°C; ความหนาแน่นของอิเล็กโทรไลต์ 2.7 g/cm3
โลหะผสมแอโนดเตรียมจากอลูมิเนียมปฐมภูมิและทองแดงบริสุทธิ์ (99.90-99.95% Cu) ซึ่งใส่เข้าไปในโลหะในปริมาณ 30-40% ความหนาแน่นของโลหะผสมแอโนดเหลวขององค์ประกอบนี้คือ 3-3.5 g/cm3 3 ; ความหนาแน่นของอะลูมิเนียมแคโทดหลอมเหลวบริสุทธิ์คือ 2.3 g/cm3 ด้วยอัตราส่วนความหนาแน่นนี้ เงื่อนไขที่จำเป็นสำหรับการแยกชั้นหลอมเหลวทั้งสามชั้นที่ดีจึงถูกสร้างขึ้น
ในระบบควอเทอร์นารี Al-Cu-Fe-Si ซึ่งรวมถึงโลหะผสมแอโนด ยูเทคติกจะเกิดขึ้นโดยมีจุดหลอมเหลวที่ 520°C โดยการหล่อเย็นโลหะผสมขั้วบวกที่มีสิ่งเจือปนของเหล็กและซิลิคอนในปริมาณที่สูงกว่าความเข้มข้นของยูเทคติก จึงเป็นไปได้ที่จะปล่อยเหล็กและซิลิคอนเข้าสู่สถานะของแข็งในรูปของสารประกอบระหว่างโลหะ FeSiAl 5 และ Cu 2 FeAl 7 เนื่องจากอุณหภูมิของโลหะผสมแอโนดในช่องของอิเล็กโตรไลเซอร์อยู่ที่ 30-40°C ต่ำกว่าอุณหภูมิของโลหะผสมแอโนดในพื้นที่ทำงานของอ่าง การสะสมตัวของโลหะระหว่างโลหะจะถูกปล่อยออกมา (เนื่องจากเหล็กและซิลิคอนสะสมอยู่ใน โลหะผสมแอโนด) ด้วยการเอาคราบเหล่านี้ออกเป็นระยะๆ โลหะผสมแอโนดจะถูกทำความสะอาด (โดยไม่ต้องอัพเดต) จากสิ่งสกปรกของเหล็กและซิลิคอน เนื่องจากแกลเลียมมีความเข้มข้นในโลหะผสมแอโนด ตะกอนที่สกัดจากอิเล็กโทรไลเซอร์ (30-40 กิโลกรัมต่ออะลูมิเนียม 1 ตัน) จึงสามารถใช้เป็นแหล่งที่มาของโลหะนี้ได้
สำหรับการกลั่นด้วยไฟฟ้านั้น จะใช้อิเล็กโทรไลเซอร์ ซึ่งในการออกแบบจะมีลักษณะคล้ายกับอิเล็กโทรไลเซอร์ที่มีแอโนดแบบอบสำหรับการผลิตอะลูมิเนียมปฐมภูมิด้วยไฟฟ้า แต่มีการเชื่อมต่อขั้วที่แตกต่างกัน: เตาทำหน้าที่เป็นแอโนดและอิเล็กโทรดแถวบนทำหน้าที่เป็นแคโทด อิเล็กโทรไลเซอร์สมัยใหม่สำหรับการกลั่นอะลูมิเนียมด้วยไฟฟ้าได้รับการออกแบบสำหรับความแรงของกระแสไฟฟ้าสูงถึง 75 kA
ด้านล่างนี้เป็นตัวชี้วัดทางเทคนิคและเศรษฐกิจหลักของอิเล็กโตรไลเซอร์ในปี 1979 ซึ่งประสบความสำเร็จโดยองค์กรในประเทศ (1, 2, 3)
ประสิทธิภาพกระแสไฟฟ้าเคมีซึ่งคำนวณจากโลหะที่เทจากอิเล็กโทรไลเซอร์คือ 97-98% ประสิทธิภาพปัจจุบันที่แท้จริงซึ่งคำนวณตามปริมาณโลหะเชิงพาณิชย์คือ 92-96%
| ความแรงปัจจุบัน kA | 23,5 | 62,9 | 69,8* |
| แรงดันไฟฟ้าเฉลี่ย, V | 5,43 | 5,68 | 5,69 |
| เอาท์พุตปัจจุบัน % | 95,7 | 93,0 | 92,7 |
| การใช้พลังงานไฟฟ้ากระแสตรง, กิโลวัตต์ ּ ชั่วโมง/ที | 17 370 | 18 700 | 19 830 |
| กำลังไฟฟ้ากระแสสลับทั้งหมด, กิโลวัตต์ ּ ชั่วโมง/ที | 18 670 | 19 590 | 20 780 |
| ระดับ ซม | |||
| แคโทดอลูมิเนียม | 16,6 | 12,9 | 14,6 |
| อิเล็กโทรไลต์ | 13,3 | 11,6 | 14,2 |
| โลหะผสมขั้วบวก | 40,1 | 29,5 | 30,0 |
| ค่าสัมประสิทธิ์การบริโภค กก./ตัน: | |||
| แบเรียมคลอไรด์ | 40,5 | 41,5 | 27,0 |
| ไครโอไลท์ | 27,7 | 21,0 | 16,5 |
| อลูมิเนียมฟลูออไรด์ | 6,7 | 13,1 | 3,8 |
| เกลือแกง | 1,0 | 4,8 | - |
| อลูมิเนียมดิบ | 1020 | 1028 | 1032 |
| กราไฟท์ | 11,9 | 11,5 | 16,6 |
| ทองแดง | 9,8 | 15,5 | 16,4 |
| การผลิตอะลูมิเนียมที่มีความบริสุทธิ์สูง % เกรด: | |||
| A995 | 47,8** | 3,5 | 2,1 |
| A99 | 30,4 | 67,1 | 54,2 |
| A97 | 8,3 | 21,5 | 43,7 |
| A95 | 10,4 | 7,9 | - |
| ต่ำกว่า A95 | 3,1 | - | - |
* ตัวชี้วัดการผลิตอลูมิเนียมที่มีความบริสุทธิ์สูง **เกรดตามอิเล็กโตรไลเซอร์ไม่มีการสลายตัว |
|||
ปัจจัยหลักที่ลดประสิทธิภาพในปัจจุบัน นอกเหนือจากการสูญเสียกระแสตรงอันเนื่องมาจากการปล่อยไอออนอิเลคโตรเนกาติตีมากขึ้น การสูญเสียโลหะอันเนื่องมาจากการเกิดออกซิเดชันและการสูญเสียทางกลของอลูมิเนียมคือการทำงานของอิเล็กโทรไลเซอร์ด้วยการปล่อยโลหะคุณภาพต่ำ ซึ่งจะถูกส่งกลับไปยังโลหะผสมแอโนดเพื่อการกลั่นในภายหลัง ระยะเวลาการทำงานของอิเล็กโตรไลเซอร์เหล่านี้เกิดขึ้นระหว่างการเริ่มต้นอิเล็กโทรไลเซอร์และการละเมิดระบอบเทคโนโลยี
การกลั่นอะลูมิเนียมด้วยไฟฟ้าเป็นกระบวนการที่ใช้พลังงานมาก ปริมาณการใช้ไฟฟ้าในไฟฟ้ากระแสสลับรวมถึงพลังงานที่ใช้ในการเตรียมอิเล็กโทรไลต์และโลหะผสมแอโนดการทำงานของอุปกรณ์ระบายอากาศและยานพาหนะตลอดจนการสูญเสียในการแปลงกระแสสลับเป็นไฟฟ้ากระแสตรงคือ 18.5-21.0 พันกิโลวัตต์ชั่วโมงต่อ 1 ตัน อลูมิเนียม ประสิทธิภาพการใช้พลังงานของอิเล็กโทรไลเซอร์ในการกลั่นไม่เกิน 5-7% นั่นคือ 93-95% ของพลังงานถูกใช้ไปในรูปแบบของการสูญเสียความร้อน ซึ่งส่วนใหญ่ปล่อยออกมาในชั้นอิเล็กโทรไลต์ (ประมาณ 80-85% ของความร้อนที่ป้อนทั้งหมด) ดังนั้น วิธีหลักในการลดการใช้พลังงานจำเพาะสำหรับการกลั่นอลูมิเนียมด้วยไฟฟ้าด้วยไฟฟ้าคือการปรับปรุงฉนวนกันความร้อนของอิเล็กโทรไลเซอร์ (โดยเฉพาะส่วนบนของโครงสร้าง) และลดชั้นอิเล็กโทรไลต์ (ลดระยะห่างระหว่างอิเล็กโทรด)
ความบริสุทธิ์ของอลูมิเนียมที่กลั่นโดยใช้วิธีสามชั้นคือ 99.995% มันถูกกำหนดโดยความแตกต่างกับสิ่งสกปรกหลักห้าประการ - เหล็ก, ซิลิคอน, ทองแดง, สังกะสีและไทเทเนียม ปริมาณโลหะของเกรดนี้ได้อยู่ที่ 45-48% ของผลผลิตทั้งหมด (โดยไม่มีการสลายตัวด้วยเกรดที่ต่ำกว่า)
อย่างไรก็ตาม ควรสังเกตว่าอะลูมิเนียมที่ผ่านการกลั่นด้วยไฟฟ้าประกอบด้วยโลหะอื่นเจือปนในปริมาณที่น้อยกว่า ซึ่งจะลดความบริสุทธิ์สัมบูรณ์ของอะลูมิเนียมดังกล่าว การวิเคราะห์กัมมันตภาพรังสีทำให้สามารถตรวจจับสิ่งเจือปนในอะลูมิเนียมที่ผ่านการกลั่นด้วยไฟฟ้าได้มากถึง 30 ชนิด ซึ่งมีปริมาณรวมประมาณ 60ּ10–4% ดังนั้นความบริสุทธิ์ของอลูมิเนียมที่ผ่านการกลั่นแล้วเมื่อเทียบกับสิ่งเจือปนเหล่านี้คือ 99.994%
นอกจากสิ่งเจือปนที่ GOST ระบุไว้ (ดูตารางที่ 1.1) เกรดที่พบมากที่สุด (A99) ของอลูมิเนียมที่ผ่านการกลั่นด้วยไฟฟ้าแล้วยังมี %: Cr 0.00016; วี 0.0001; กา 0.0006; หน้า 0.002; เอสเอ็น 0.00005; แคลิฟอร์เนีย 0.002-0.003; นา 0.001-0.008; ล้าน 0.001-0.007; มก. 0.001-0.007; เช่น<0,0001; Sb<0,00002; Bi<0,00001; Cd<0,000001; S 0,0007.
แหล่งที่มาของการปนเปื้อนอะลูมิเนียมแคโทดประการหนึ่งคือตัวนำกระแสไฟฟ้ากราไฟต์ซึ่งประกอบด้วยเหล็กและซิลิคอนออกไซด์และสัมผัสกับอะลูมิเนียมที่ผ่านการกลั่นอยู่ตลอดเวลา หากกระแสไฟถูกส่งไปยังอะลูมิเนียมแคโทดโดยตรงด้วยแท่งอะลูมิเนียม และใช้เครื่องมือที่ทำจากกราไฟต์บริสุทธิ์มาก ก็เป็นไปได้ที่จะได้โลหะที่มีความบริสุทธิ์ 99.999% โดยความแตกต่างกับสิ่งเจือปนที่ตรวจพบได้ (Fe, Si, Cu, Zn และติ) โลหะนี้มีค่าเฉลี่ย %: Si 0.0002; เฟ 0.00032; ลูกบาศ์ก 0.0002; สังกะสี 0.0002 และ Ti 0.00005 อย่างไรก็ตาม เนื่องจากปัญหาทางเทคนิค วิธีการจ่ายกระแสไฟฟ้าด้วยวิธีนี้ยังไม่พบการประยุกต์ใช้ทางอุตสาหกรรมในวงกว้าง
การผลิตอะลูมิเนียมที่มีความบริสุทธิ์สูง
อลูมิเนียมที่มีความบริสุทธิ์สูง (เกรด A999) สามารถผลิตได้สามวิธี: การถลุงแบบโซน การกลั่นผ่านซับฮาไลด์ และการแยกสลายด้วยไฟฟ้าของสารประกอบอะลูมิเนียม-อินทรีย์ จากวิธีการที่ระบุไว้ในการผลิตอะลูมิเนียมที่มีความบริสุทธิ์สูง วิธีการหลอมโซนได้รับการนำไปใช้จริงในสหภาพโซเวียต
หลักการของการหลอมโซนคือการผ่านโซนหลอมเหลวไปตามแท่งอลูมิเนียมซ้ำๆ ตามค่าสัมประสิทธิ์การกระจาย เค=สโทรทัศน์ /กับว (ที่ไหน กับทีวี - ความเข้มข้นของสิ่งเจือปนในของแข็งและ กับ g - ในเฟสของเหลว) ซึ่งส่วนใหญ่กำหนดประสิทธิภาพของการทำให้บริสุทธิ์จากสิ่งสกปรก สิ่งสกปรกเหล่านี้สามารถแบ่งออกเป็นสามกลุ่ม กลุ่มแรกประกอบด้วยสิ่งเจือปนที่ทำให้จุดหลอมเหลวของอลูมิเนียมลดลง พวกเขามี ถึง<1 ในระหว่างการหลอมโซน จะถูกรวมตัวอยู่ในโซนหลอมเหลวและถ่ายโอนไปยังส่วนสุดท้ายของแท่งโลหะ สิ่งเจือปนเหล่านี้ ได้แก่ Ga, Sn, Be, Sb, Ca, Th, Fe, Co, Ni, Ce, Te, Ba, Pt, Au, Bi, Pb, Cd, In, Na, Mg, Cu, Si, Ge, Zn . กลุ่มที่สองประกอบด้วยสิ่งเจือปนที่เพิ่มจุดหลอมเหลวของอลูมิเนียม พวกเขามีลักษณะเฉพาะ เค>1และในระหว่างการหลอมโซน พวกมันจะกระจุกตัวอยู่ในส่วนที่เป็นของแข็ง (เริ่มต้น) ของแท่งโลหะ สิ่งเจือปนเหล่านี้ ได้แก่ Nb, Ta, Cr, Ti, Mo, V กลุ่มที่สามประกอบด้วยสิ่งเจือปนที่มีค่าสัมประสิทธิ์การกระจายใกล้กับความสามัคคีมาก (Mn, Sc) สิ่งเจือปนเหล่านี้จะไม่ถูกกำจัดออกไปในระหว่างการหลอมโซนของอะลูมิเนียม
อะลูมิเนียมที่มีไว้สำหรับการหลอมแบบโซนนั้นต้องผ่านการเตรียมการบางอย่าง ซึ่งประกอบด้วยการกรอง การกำจัดก๊าซ และการดอง จำเป็นต้องกรองเพื่อขจัดฟิล์มออกไซด์ที่ทนไฟและทนทานที่กระจายตัวอยู่ในโลหะออกจากอลูมิเนียม อะลูมิเนียมออกไซด์ที่มีอยู่ในอะลูมิเนียมหลอมเหลวสามารถสร้างจุดศูนย์กลางการตกผลึกในระหว่างการแข็งตัว ซึ่งนำไปสู่การผลิตแท่งโลหะโพลีคริสตัลไลน์ และการหยุดชะงักของผลกระทบของการกระจายตัวของสิ่งเจือปนระหว่างโลหะแข็งและโซนหลอมเหลว อลูมิเนียมถูกกรองในสุญญากาศ (ความดันตกค้าง 0.1-0.4 Pa) ผ่านรูที่ด้านล่างของเบ้าหลอมกราไฟท์ที่มีเส้นผ่านศูนย์กลาง 1.5-2 มม. การไล่แก๊สอะลูมิเนียมเบื้องต้นก่อนการหลอมโซน (รวมถึงการให้ความร้อนในสุญญากาศด้วย) จะดำเนินการเพื่อป้องกันการกระเด็นของโลหะเมื่อโซนละลายหากดำเนินการในสุญญากาศสูง ขั้นตอนสุดท้ายของการเตรียมอะลูมิเนียมสำหรับการหลอมโซนคือการกัดพื้นผิวด้วยส่วนผสมของกรดไฮโดรคลอริกเข้มข้นและกรดไนตริก
เนื่องจากอะลูมิเนียมมีฤทธิ์ทางเคมีที่สำคัญ และโดยเฉพาะอย่างยิ่งกราไฟท์บริสุทธิ์จึงถูกใช้เป็นวัสดุหลักสำหรับบรรจุภัณฑ์ (เรือ) การหลอมโซนของอะลูมิเนียมจึงดำเนินการในสุญญากาศหรือในบรรยากาศของก๊าซเฉื่อย (อาร์กอน ฮีเลียม)
การหลอมแบบโซนในสุญญากาศทำให้อะลูมิเนียมมีความบริสุทธิ์มากขึ้น เนื่องจากการระเหยของสิ่งเจือปนบางส่วนในระหว่างการอพยพ (แมกนีเซียม สังกะสี แคดเมียม โลหะอัลคาไล และอัลคาไลน์เอิร์ธ) และยังช่วยขจัดการปนเปื้อนของโลหะบริสุทธิ์ด้วยสิ่งเจือปนอันเป็นผลมาจากการใช้ ก๊าซเฉื่อยป้องกัน การหลอมอะลูมิเนียมแบบโซนในสุญญากาศสามารถทำได้ด้วยการปั๊มท่อควอทซ์อย่างต่อเนื่อง โดยวางเรือกราไฟท์ที่มีแท่งอลูมิเนียมไว้ เช่นเดียวกับในหลอดควอตซ์แบบปิดผนึก ซึ่งอากาศจะถูกสูบออกสู่แรงดันตกค้างในขั้นแรก ประมาณ 1ּ10 –3 Pa
ในการสร้างโซนหลอมเหลวบนแท่งอะลูมิเนียมระหว่างโซนหลอมเหลว สามารถใช้การให้ความร้อนโดยใช้เตาต้านทานขนาดเล็กหรือกระแสความถี่สูง การจ่ายไฟให้กับเตาต้านทานไฟฟ้าไม่จำเป็นต้องใช้อุปกรณ์ที่ซับซ้อน เตาใช้งานง่าย ข้อเสียเปรียบประการเดียวของวิธีการให้ความร้อนนี้คือส่วนตัดขวางเล็กๆ ของแท่งอะลูมิเนียมที่กำลังทำให้บริสุทธิ์
การทำความร้อนด้วยการเหนี่ยวนำด้วยกระแสความถี่สูงเป็นวิธีที่เหมาะในการสร้างบริเวณหลอมเหลวบนแท่งโลหะระหว่างการหลอมโซน วิธีการให้ความร้อนความถี่สูง (นอกเหนือจากข้อเท็จจริงที่ว่ามันช่วยให้โซนหลอมแท่งโลหะที่มีหน้าตัดขนาดใหญ่ได้) มีข้อได้เปรียบที่สำคัญคือโลหะหลอมเหลวจะถูกผสมอย่างต่อเนื่องในโซน สิ่งนี้เอื้อต่อการแพร่กระจายของอะตอมที่ไม่บริสุทธิ์จากด้านหน้าของการตกผลึกไปสู่ส่วนลึกของการหลอมละลาย
นับเป็นครั้งแรกที่การผลิตทางอุตสาหกรรมของอะลูมิเนียมที่มีความบริสุทธิ์สูงโดยการหลอมแบบโซนได้รับการควบคุมที่โรงถลุงอะลูมิเนียม Volkhov ในปี 1965 โดยใช้การติดตั้ง UZPI-3 ที่พัฒนาโดย VAMI การติดตั้งนี้ติดตั้งเครื่องรีทอร์คควอตซ์สี่ตัวพร้อมระบบทำความร้อนแบบเหนี่ยวนำ ในขณะที่ตัวเหนี่ยวนำสามารถเคลื่อนย้ายได้ และภาชนะที่มีโลหะอยู่นิ่ง ผลผลิตคือโลหะ 20 กิโลกรัมต่อรอบการทำความสะอาด ต่อมาได้มีการสร้างการติดตั้ง UZPI-4 ที่เป็นโลหะทั้งหมดที่มีประสิทธิภาพสูงยิ่งขึ้นและเปิดดำเนินการเชิงพาณิชย์ในปี พ.ศ. 2515 ที่โรงหลอมอลูมิเนียม Volkhov
ประสิทธิภาพของการทำให้อะลูมิเนียมบริสุทธิ์ในระหว่างการหลอมโซนสามารถแสดงลักษณะเฉพาะได้จากข้อมูลต่อไปนี้ หากปริมาณสิ่งเจือปนทั้งหมดในอะลูมิเนียมที่ผ่านการกลั่นด้วยไฟฟ้าคือ (30۞60)ּ10–4% จากนั้นหลังจากการหลอมโซนจะลดลงเป็น (2.8۞3.2)ּ10–4% เช่น 15-20 เท่า ซึ่งสอดคล้องกับความต้านทานไฟฟ้าตกค้างของอลูมิเนียม ρ ○ (ที่อุณหภูมิฮีเลียมเหลว 4.2 K) ตามลำดับ (20۞40)ּ10 –10 และ (1.8۞2.1)ּ10 –10 หรือมีความบริสุทธิ์ 99.997-99.994 และ 99.9997% . ในตาราง 1.4 (ดูด้านล่าง) แสดงข้อมูลการวิเคราะห์กัมมันตภาพรังสีเกี่ยวกับเนื้อหาของสิ่งเจือปนบางอย่างในอะลูมิเนียมที่ผ่านการทำให้บริสุทธิ์แบบโซนและที่ผ่านการกลั่นด้วยไฟฟ้า ข้อมูลเหล่านี้บ่งชี้ว่าปริมาณสิ่งเจือปนส่วนใหญ่ลดลงอย่างมาก แม้ว่าสิ่งเจือปน เช่น แมงกานีสและสแกนเดียมจะไม่ได้ถูกกำจัดออกไปในระหว่างการหลอมโซนก็ตาม
ในช่วงไม่กี่ปีที่ผ่านมา VAMI ได้พัฒนาและทดสอบเทคโนโลยีสำหรับการผลิตอะลูมิเนียมที่มีความบริสุทธิ์ 99.9999% ในสภาวะอุตสาหกรรมโดยใช้วิธีการหลอมแบบคาสเคดโซน สาระสำคัญของวิธีการหลอมโซนแบบคาสเคดก็คือ การทำให้อะลูมิเนียมตั้งต้นที่มีความบริสุทธิ์ A999 บริสุทธิ์จะดำเนินการโดยวงจรการทำซ้ำตามลำดับ (แบบเรียงซ้อน) ของแถบโซน ในกรณีนี้ วัสดุตั้งต้นสำหรับน้ำตกแต่ละชั้นที่ตามมาคือส่วนที่ตรงกลางและบริสุทธิ์ที่สุดของแท่งโลหะที่ได้รับอันเป็นผลมาจากรอบการทำให้บริสุทธิ์ครั้งก่อน
ตารางที่ 1.4
| สิ่งเจือปน | อลูมิเนียมดิบ (กลั่นด้วยไฟฟ้า 99.993-99.994%) | อลูมิเนียมหลังโซนละลาย | |
| กราไฟท์, สูญญากาศ | อัลลันด์, อากาศ | ||
| ทองแดง | 1,9 | 0,02 | 0,08 |
| สารหนู | 0,15 | 0,0015 | 0,001 |
| พลวง | 1,2 | 0,03 | 0,02 |
| ดาวยูเรนัส | 0,002 | - | - |
| เหล็ก | 3 | ≤0,2 | ≤0,3 |
| กาเลี่ยม | 0,3 | 0,02 | 0,05 |
| แมงกานีส | 0,2-0,3 | 0,1-0,2 | 0,15 |
| สแกนเดียม | 0,4-0,5 | 0,4-0,5 | 0,4-0,5 |
| อิตเทรียม | 0,02-0,04 | <<0,001 | <<0,001 |
| ลูทีเทียม | 0,002-0,004 | <<0,0001 | <<0,0001 |
| โฮลเมียม | 0,005-0,01 | <<0,0001 | <<0,0001 |
| แกโดลิเนียม | 0,02-0,04 | <<0,01 | <<0,01 |
| เทอร์เบียม | 0,003-0,006 | <<0,001 | <<0,001 |
| ซาแมเรียม | 0,05-0,01 | <<0,0001 | <<0,0001 |
| นีโอไดเมียม | 0,1-0,2 | <<0,01 | <<0,01 |
| พราซีโอดิเมียม | 0,05-0,1 | <<0,001 | <<0,001 |
| ซีเรียม | 0,3-0,6 | <<0,01 | <<0,01 |
| แลนทานัม | 0,01 | <<0,001 | <<0,001 |
| นิกเกิล | 2,3 | - | <1 |
| แคดเมียม | 3,5 | <<0,01 | 0,02-0,07 |
| สังกะสี | 20 | <<0,05 | 1 |
| โคบอลต์ | 0,01 | <<0,01 | <<0,01 |
| โซเดียม | 1-2 | <0,2 | <0,2 |
| โพแทสเซียม | 0,05 | 0,01 | 0,01 |
| แบเรียม | 6 | - | - |
| คลอรีน | 0,01 | <0,01 | <0,01 |
| ฟอสฟอรัส | 3 | 0,04 | - |
| กำมะถัน | 15 | 0,5-1,5 | - |
| คาร์บอน | 1-2 | - | 1-2 |
| บันทึก. ปริมาณเทลลูเรียม บิสมัท เงิน โมลิบดีนัม โครเมียม เซอร์โคเนียม แคลเซียม สตรอนเซียม รูบิเดียม ซีเรียม อินเดียม ซีลีเนียม และปรอทในอลูมิเนียมหลังการถลุงโซนจะต่ำกว่าความไวของการวิเคราะห์กัมมันตภาพรังสี | |||
ในตาราง 1.5 (ดูด้านล่าง) แสดงผลการวิเคราะห์และการวัดมวลสเปกตรัม ร 293 พัน / รอะลูมิเนียม 4.2 K เกิดจากการหลอมแบบคาสเคดโซน จากข้อมูลที่นำเสนอ เราสามารถสรุปได้ว่าความบริสุทธิ์ของอะลูมิเนียมดังกล่าว ซึ่งพิจารณาจากความแตกต่างกับสิ่งเจือปนหลัก 10 ชนิด (Si, Fe, Mg, Mn, Ti, Cu, Cr, Zn, Na และ V) อยู่ที่ >99.9999% . ข้อสรุปนี้ได้รับการยืนยันทางอ้อมด้วยคุณค่า ร 293 พัน / ร 4.2 K ซึ่งในทุกตัวอย่างคือ >30ּ10 3
เพื่อให้ได้โลหะที่มีความบริสุทธิ์ 99.9999% ก็เพียงพอที่จะดำเนินการละลายโซนสองครั้ง (ดูตารางที่ 1.5) การเพิ่มจำนวนลดหลั่นอีกไม่ได้เพิ่มความบริสุทธิ์ของอะลูมิเนียม แม้ว่าจะเพิ่มผลผลิตโดยรวมของโลหะด้วยความบริสุทธิ์ 99.9999% ก็ตาม
กระบวนการที่เป็นไปได้อีกประการหนึ่งในการได้รับอะลูมิเนียมที่มีความบริสุทธิ์สูงคือการกลั่นผ่านซับฮาไลด์ โดยเฉพาะอย่างยิ่งผ่านอะลูมิเนียมซับฟลูออไรด์
ความดันไออิ่มตัวของโลหะอะลูมิเนียมไม่สูงพอที่จะทำการกลั่นโดยตรงในอัตราที่ยอมรับได้ในทางปฏิบัติ อย่างไรก็ตาม เมื่อให้ความร้อนในสุญญากาศ (ที่ 1,000-1,050°C) ด้วย AlF 3 อะลูมิเนียมจะเกิดเป็นซับฟลูออไรด์ AlF ที่มีความผันผวนสูง ซึ่งถูกกลั่นลงในโซนเย็น (800°C) ซึ่งจะสลายตัวอีกครั้ง (ไม่สมส่วน) เมื่อปล่อยออกมา อะลูมิเนียมบริสุทธิ์:
ความเป็นไปได้ของการทำให้อะลูมิเนียมบริสุทธิ์อย่างล้ำลึกจากสิ่งเจือปนนั้นมีสาเหตุหลักมาจากความน่าจะเป็นของการก่อตัวของสารประกอบย่อยของอะลูมิเนียมนั้นมากกว่าความน่าจะเป็นของการก่อตัวของสารประกอบย่อยของสิ่งเจือปน
ตารางที่ 1.5
ผลการวิเคราะห์และการวัดสเปกตรัมมวล ร 293 พัน / ร 4.2 K การหลอมโซนอะลูมิเนียม CASCADE
| จำนวนขั้นตอน | ปริมาณสิ่งเจือปน ×10 –4% | ||||||
| ศรี | เฟ | มก | มน | Ti | ผลรวม | ||
| ต้นฉบับ | 18,3 | 0,210 | <0,103 | 0,89 | <0,061 | 0,069 | 1,544 |
| A999 | |||||||
| 2 | 36,5 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 38,0 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 39,5 | 0,073 | <0,103 | 0,045 | <0,061 | 0,07 | 0,563 |
| 3 | 32,0 | 0,204 | <0,103 | 0,006 | <0,061 | 0,017 | 0,502 |
| 3 | 30,0 | 0,073 | 0,100 | 0,006 | 0,020 | 0,07 | 0,480 |
| 3 | 32,0 | 0,052 | 0,100 | 0,006 | 0,061 | 0,07 | 0,500 |
| 4 | 40,0 | <0,021 | <0,103 | 0,006 | 0,061 | 0,07 | 0,472 |
| 4 | 30,5 | 0,031 | 0,100 | 0,006 | 0,061 | 0,07 | 0,479 |
| 5 | 34,0 | 0,104 | <0,060 | 0,006 | 0,061 | 0,017 | 0,459 |
| หมายเหตุ: 1. ปริมาณของสิ่งเจือปนจะพิจารณาจากสิ่งเจือปนอื่น ๆ ซึ่งมีเนื้อหาในตัวอย่างทั้งหมดคือ ×10 –4%:<0,071 Cu; <0,038 Cr; 0,048 Zn; 0,017 Na; 0,037 V. 2. При подсчете суммы примесей принимали их максимальное значение, равное пределу чувствительности анализа, например <0,061 считали как 0,061. | |||||||
เนื้อหาของสิ่งเจือปนในอะลูมิเนียมที่กลั่นผ่านซับฟลูออไรด์มีความสัมพันธ์แบบผกผันกับมวลของแท่งโลหะที่เกิดขึ้น ในแท่งโลหะที่มีน้ำหนัก 1.5-1.7 กก. ปริมาณสิ่งสกปรกทั้งหมด (Si, Fe, Cu, Mg) คือ 11ּ10–4% และปริมาณก๊าซคือ 0.007 ซม. 3 /100 กรัม ความต้านทานตกค้างจำเพาะ (ρ ○) ที่ฮีเลียมเหลว อุณหภูมิของโลหะดังกล่าวคือ (1.7÷2.0)ּ10 –10 โอห์มซม. การกลั่นอะลูมิเนียมผ่านซับฟลูออไรด์มีข้อเสียหลายประการ (ผลผลิตค่อนข้างต่ำ การทำแมกนีเซียมให้บริสุทธิ์อย่างล้ำลึกไม่เพียงพอ ฯลฯ) ดังนั้นวิธีการนี้จึงไม่ได้รับการพัฒนาทางอุตสาหกรรม
นอกจากนี้ ยังมีการพัฒนาวิธีการสำหรับการผลิตอะลูมิเนียมที่มีความบริสุทธิ์สูงโดยอิเล็กโทรไลซิสของสารประกอบออร์กาโนอะลูมิเนียมเชิงซ้อน ซึ่งมีองค์ประกอบของอิเล็กโทรไลต์ต่างกัน ตัวอย่างเช่น ในประเทศเยอรมนี พวกเขาใช้วิธีการอิเล็กโทรไลซิสของสารละลาย NaFּ2Al (C 2 H 5) 3 50% ในโทลูอีน การกลั่นจะดำเนินการที่อุณหภูมิ 100°C แรงดันไฟฟ้าอิเล็กโตรไลเซอร์ 1.0-1.5 V และความหนาแน่นกระแส 0.3-0.5 A/dm 2 โดยใช้อิเล็กโทรดอะลูมิเนียม ประสิทธิภาพกระแสแคโทด 99% การกลั่นด้วยเคมีไฟฟ้าในอิเล็กโทรไลต์ออร์กาโนอลูมิเนียมช่วยลดปริมาณแมงกานีสและสแกนเดียมลงอย่างมาก ซึ่งในทางปฏิบัติแล้วจะไม่ถูกกำจัดออกไปในระหว่างการทำให้โซนบริสุทธิ์ ข้อเสียของวิธีนี้คือให้ผลผลิตต่ำและมีอันตรายจากไฟไหม้สูง
หากต้องการทำให้อะลูมิเนียมบริสุทธิ์ได้ลึกยิ่งขึ้นและได้โลหะที่มีความบริสุทธิ์ตั้งแต่ 99.99999% ขึ้นไป คุณสามารถใช้วิธีการข้างต้นร่วมกันได้: การอิเล็กโทรลิซิสของสารประกอบออร์กาโนอะลูมิเนียม หรือการระเหิดผ่านซับฟลูออไรด์ ตามด้วยการโซนการหลอมของอะลูมิเนียมที่เกิดขึ้น ตัวอย่างเช่น โดยการทำให้อะลูมิเนียมบริสุทธิ์แบบโซนซ้ำๆ ที่ได้จากกระบวนการอิเล็กโทรลิซิสของสารประกอบออร์กาโนอะลูมิเนียม ก็เป็นไปได้ที่จะได้โลหะที่มีความบริสุทธิ์สูงโดยมีปริมาณสิ่งเจือปน ×10–9%: Fe 50; ศรี<500; Cu 10; Mg 30; Mn5; Ti <500; Cr 20; Zn <50; Co <1; Ag <5; Sb <1 и Se 3.
แอปพลิเคชัน
การรวมกันของคุณสมบัติทางกายภาพ ทางกล และทางเคมีของอะลูมิเนียม กำหนดการใช้งานอย่างแพร่หลายในเกือบทุกด้านของเทคโนโลยี โดยเฉพาะอย่างยิ่งในรูปของโลหะผสมกับโลหะอื่นๆ ในด้านวิศวกรรมไฟฟ้า อลูมิเนียมสามารถแทนที่ทองแดงได้สำเร็จ โดยเฉพาะอย่างยิ่งในการผลิตตัวนำขนาดใหญ่ เช่น ในสายไฟเหนือศีรษะ สายเคเบิลไฟฟ้าแรงสูง บัสบาร์สวิตช์เกียร์ หม้อแปลงไฟฟ้า (ค่าการนำไฟฟ้าของอะลูมิเนียมสูงถึง 65.5% ของค่าการนำไฟฟ้าของทองแดง และ มันเบากว่าทองแดงมากกว่าสามเท่าด้วยหน้าตัดที่ให้ค่าการนำไฟฟ้าเท่ากันมวลของเส้นลวดอะลูมิเนียมจึงมีมวลครึ่งหนึ่งของทองแดง) อลูมิเนียมบริสุทธิ์พิเศษใช้ในการผลิตตัวเก็บประจุไฟฟ้าและวงจรเรียงกระแสซึ่งการกระทำนั้นขึ้นอยู่กับความสามารถของฟิล์มอลูมิเนียมออกไซด์ในการส่งกระแสไฟฟ้าในทิศทางเดียวเท่านั้น อลูมิเนียมบริสุทธิ์พิเศษที่บริสุทธิ์โดยการหลอมโซน ใช้สำหรับการสังเคราะห์สารประกอบเซมิคอนดักเตอร์ประเภท A III B V ซึ่งใช้ในการผลิตอุปกรณ์เซมิคอนดักเตอร์ อลูมิเนียมบริสุทธิ์ใช้ในการผลิตกระจกสะท้อนแสงประเภทต่างๆ อลูมิเนียมที่มีความบริสุทธิ์สูงใช้เพื่อปกป้องพื้นผิวโลหะจากการกัดกร่อนในชั้นบรรยากาศ (การหุ้ม สีอลูมิเนียม) อะลูมิเนียมมีหน้าตัดการดูดกลืนนิวตรอนค่อนข้างต่ำ จึงใช้เป็นวัสดุโครงสร้างในเครื่องปฏิกรณ์นิวเคลียร์
ถังอะลูมิเนียมความจุขนาดใหญ่จัดเก็บและขนส่งก๊าซเหลว (มีเทน ออกซิเจน ไฮโดรเจน ฯลฯ) กรดไนตริกและอะซิติก น้ำสะอาด ไฮโดรเจนเปอร์ออกไซด์ และน้ำมันที่บริโภคได้ อะลูมิเนียมถูกนำมาใช้กันอย่างแพร่หลายในอุปกรณ์และเครื่องมือในอุตสาหกรรมอาหาร สำหรับบรรจุภัณฑ์อาหาร (ในรูปของฟอยล์) และสำหรับการผลิตผลิตภัณฑ์ในครัวเรือนประเภทต่างๆ การใช้อะลูมิเนียมในการตกแต่งอาคาร สถาปัตยกรรม โครงสร้างการขนส่งและการกีฬาเพิ่มขึ้นอย่างรวดเร็ว
ในทางโลหะวิทยา อะลูมิเนียม (นอกเหนือจากโลหะผสมที่มีส่วนประกอบดังกล่าว) เป็นหนึ่งในสารเติมแต่งโลหะผสมที่พบมากที่สุดในโลหะผสมที่มี Cu, Mg, Ti, Ni, Zn และ Fe อลูมิเนียมยังใช้ในการกำจัดออกซิไดซ์เหล็กก่อนที่จะเทลงในแม่พิมพ์ เช่นเดียวกับในกระบวนการผลิตโลหะบางชนิดโดยใช้ความร้อนจากอะลูมิเนียม SAP (ผงอะลูมิเนียมเผาผนึก) ผลิตจากอะลูมิเนียมโดยใช้ผงโลหะวิทยา ซึ่งมีความต้านทานความร้อนสูงที่อุณหภูมิสูงกว่า 300°C
อลูมิเนียมใช้ในการผลิตวัตถุระเบิด (แอมโมนัล, อะลูโมทอล) สารประกอบอลูมิเนียมหลายชนิดมีการใช้กันอย่างแพร่หลาย
การผลิตและการบริโภคอะลูมิเนียมมีการเติบโตอย่างต่อเนื่อง ซึ่งแซงหน้าอัตราการเติบโตของการผลิตเหล็ก ทองแดง ตะกั่ว และสังกะสีอย่างมาก
DIN (DeutschIndustrienorm) - มาตรฐานอุตสาหกรรมของประเทศเยอรมนี
กระบวนการทางเทคโนโลยีของการผลิตอะลูมิเนียมประกอบด้วยสามขั้นตอนหลัก:
1. การสร้างอลูมินาจากแร่อะลูมิเนียม
2. การสร้างอะลูมิเนียมจากอลูมินา
3. กระบวนการกลั่นอลูมิเนียม
และในกรณีนี้จำเป็นต้องใช้อุปกรณ์ดังต่อไปนี้:
อุปกรณ์สำหรับระบบจำหน่ายอลูมินาส่วนกลาง
อิเล็กโทรไลเซอร์;
บัสบาร์แคโทด;
การติดตั้งทำความสะอาดแก๊สแห้ง
เครนประกอบ เทคโนโลยี และเครนหล่อ
หน่วยความทะเยอทะยาน;
อุปกรณ์โรงหล่อ
อุปกรณ์ร้านประกอบแอโนด
โครงสร้างโลหะของอาคารการผลิต
การสร้างอลูมินาจากแร่ - ขั้นตอนการผลิตอะลูมิเนียม
อลูมินาสามารถผลิตได้สามวิธี: กรด ด่าง และอิเล็กโทรไลต์ วิธีที่นิยมมากที่สุดคือวิธีอัลคาไลน์ สาระสำคัญของวิธีนี้คือสารละลายอลูมิเนียมเริ่มสลายตัวอย่างรวดเร็วด้วยการแนะนำอะลูมิเนียมไฮดรอกไซด์และสารละลายที่เหลือจากการสลายตัวหลังจากการระเหยด้วยการกวนอย่างเข้มข้นที่อุณหภูมิ 170 C ก็สามารถละลายอลูมินาที่มีอยู่ในบอกไซต์ได้อีกครั้ง วิธีนี้มีขั้นตอนหลักดังต่อไปนี้:
1. การเตรียมอะลูมิเนียมซึ่งเกี่ยวข้องกับการบดและบดในโรงงานพิเศษ ด่างกัดกร่อน บอกไซต์ และมะนาวบางส่วนถูกส่งไปยังโรงสี เยื่อกระดาษที่ได้จะถูกส่งไปชะล้าง
2. การชะล้างแร่บอกไซต์เกี่ยวข้องกับการสลายตัวทางเคมีจากการผสมกับสารละลายด่างที่เป็นน้ำ ในกรณีนี้อะลูมิเนียมออกไซด์ไฮเดรตเมื่อรวมกับอัลคาไลจะเข้าสู่สารละลายในรูปของโซเดียมอะลูมิเนตและซิลิกาซึ่งมีอยู่ในแร่บอกไซต์เมื่อรวมกับอัลคาไลจะเข้าสู่สารละลายในรูปของโซเดียมซิลิเกต ในสารละลาย สารประกอบเหล่านี้: โซเดียมอะลูมิเนตและโซเดียมซิลิเกตทำให้เกิดโซเดียมอะลูมิโนซิลิเกตที่ไม่ละลายน้ำ สารตกค้างนี้ประกอบด้วยออกไซด์ของเหล็กและไทเทเนียม ซึ่งทำให้สารตกค้างมีโทนสีแดง สารตกค้างนี้เป็นโคลนแดง เมื่อการละลายของโซเดียมอะลูมิเนตที่เกิดขึ้นเสร็จสมบูรณ์ จะถูกเจือจางด้วยสารละลายอัลคาไลที่เป็นน้ำในขณะที่อุณหภูมิลดลงเหลือ 100°C
3. การแยกโคลนแดงและสารละลายอะลูมิเนตออกจากกันเกิดขึ้นเนื่องจากการล้างด้วยสารเพิ่มความข้น หลังจากนั้นโคลนสีแดงจะตกตะกอน และสารละลายอะลูมิเนตที่เหลือจะถูกกรอง
4. การสลายตัวของสารละลายอะลูมิเนต กรองและส่งไปยังภาชนะขนาดใหญ่พร้อมเครื่องผสม อะลูมิเนียมไฮดรอกไซด์จะถูกปล่อยออกมาจากสารละลายนี้เมื่อทำให้เย็นลงถึง 60°C และคนอย่างต่อเนื่อง เนื่องจากกระบวนการดำเนินไปอย่างไม่สม่ำเสมอและช้ามากและการเติบโตของผลึกอะลูมิเนียมไฮดรอกไซด์มีความสำคัญมากในระหว่างการประมวลผลเพิ่มเติม ไฮดรอกไซด์ที่เป็นของแข็งจำนวนมากจะถูกเติมลงในภาชนะเหล่านี้ด้วยเครื่องผสม - ตัวย่อยสลาย
5. อะลูมิเนียมไฮดรอกไซด์ผลิตในตัวกรองสุญญากาศและไฮโดรไซโคลน ไฮดรอกไซด์ส่วนใหญ่เป็นวัสดุเมล็ดจะถูกส่งกลับไปยังกระบวนการสลายตัว หลังจากล้างน้ำแล้ว สารตกค้างจะถูกส่งไปเผา และสารกรองก็กลับเข้าสู่กระบวนการเช่นกัน
6. การคายน้ำของอะลูมิเนียมไฮดรอกไซด์เป็นขั้นตอนสุดท้ายของการผลิตอลูมินา มันเกิดขึ้นในเตาเผาแบบท่อที่หมุนตลอดเวลา อะลูมิเนียมไฮดรอกไซด์ดิบจะถูกทำให้แห้งสนิทและถูกทำให้ขาดน้ำเมื่อผ่านเตาเผา
การสร้างอะลูมิเนียมจากอลูมินาในระหว่างการผลิตยังเกิดขึ้นในหลายขั้นตอนเช่นกัน
1. อิเล็กโทรไลซิสของอลูมิเนียมออกไซด์เกิดขึ้นที่อุณหภูมิในอิเล็กโทรไลเซอร์ 970°C อิเล็กโทรไลเซอร์มีอ่างที่เรียงรายไปด้วยบล็อกคาร์บอนสำหรับเชื่อมต่อกับกระแสไฟฟ้า อลูมิเนียมเหลวที่ปล่อยออกมาจะถูกรวบรวมบนฐานถ่านหินและจากนั้นจะถูกสูบออกเป็นประจำ แอโนดคาร์บอนจะถูกจุ่มลงในอิเล็กโทรไลต์ที่อยู่ด้านบน เผาไหม้ในบรรยากาศของออกซิเจน ซึ่งปล่อยออกมาจากอะลูมิเนียมออกไซด์ และในขณะเดียวกันก็ปล่อยคาร์บอนมอนอกไซด์หรือไดออกไซด์ออกมา
2. การแยกอะลูมิเนียมคลอไรด์ด้วยไฟฟ้าทำได้โดยการแปลงอะลูมิเนียมออกไซด์ในถังปฏิกิริยาให้เป็นอะลูมิเนียมคลอไรด์ หลังจากนั้นอะลูมิเนียมคลอไรด์จะถูกอิเล็กโทรไลต์ในอ่างที่มีฉนวน คลอรีนที่ปล่อยออกมาจะถูกดูดออกและส่งไปรีไซเคิล และอะลูมิเนียมจะตกตะกอนบนแคโทด
3. ลดอะลูมิเนียมคลอไรด์ด้วยแมงกานีสซึ่งปล่อยอะลูมิเนียมออกมา การควบแน่นที่มีการควบคุมจะขจัดสิ่งปนเปื้อนที่เกี่ยวข้องกับคลอรีนออกจากกระแสแมงกานีสคลอไรด์ เมื่อคลอรีนถูกปล่อยออกมา แมงกานีสคลอไรด์จะถูกแปลงเป็นแมงกานีสออกไซด์ ซึ่งจากนั้นจะถูกรีดิวซ์เป็นแมงกานีสซึ่งสามารถรีไซเคิลได้
กระบวนการกลั่นอะลูมิเนียมในการผลิตอะลูมิเนียม
การกลั่นด้วยกระแสไฟฟ้าด้วยการสลายตัวของน้ำ สารละลายน้ำเกลือเป็นไปไม่ได้สำหรับอลูมิเนียม เนื่องจากระดับการทำให้บริสุทธิ์ของอะลูมิเนียมอุตสาหกรรม ซึ่งได้จากการอิเล็กโทรไลซิสของการหลอมด้วยไครโอไลท์-อลูมินา จะไม่เพียงพอสำหรับวัตถุประสงค์บางประการ แม้แต่อะลูมิเนียมที่บริสุทธิ์กว่าก็ยังได้มาจากเศษโลหะและอะลูมิเนียมอุตสาหกรรมเนื่องจากการทำให้บริสุทธิ์ วิธีการทำให้บริสุทธิ์ที่พบบ่อยที่สุดคือการอิเล็กโทรลิซิสสามชั้น
อลูมิเนียมใช้ในการผลิตวัตถุระเบิด (alumotol, ammonal) มีการใช้สารประกอบอลูมิเนียมหลายชนิดกันอย่างแพร่หลาย การผลิตและการบริโภคอะลูมิเนียมมีการเติบโตอย่างต่อเนื่อง ซึ่งแซงหน้าอัตราการเติบโตของการผลิตทองแดง เหล็ก สังกะสี และตะกั่วอย่างมาก
เพื่อให้ได้ทองแดง จะใช้แร่ทองแดง รวมถึงของเสียทองแดงและโลหะผสม แร่ประกอบด้วยทองแดง 1–6% แร่ที่มีทองแดงน้อยกว่า 0.5% จะไม่ถูกประมวลผลเนื่องจากด้วยเทคโนโลยีระดับปัจจุบันการแยกทองแดงออกมาไม่ได้ประโยชน์
ในแร่พบทองแดงในรูปของสารประกอบกำมะถัน (CuFeS 2 - chalcopyrite, Cu 2 S - chalcocite, CuS - โคเวลีน), ออกไซด์ (CuO, CuO) และไฮโดรคาร์บอเนต
แร่ gangue ประกอบด้วยไพไรต์ (FeS 2), ควอตซ์ (SiO 2), สารประกอบต่างๆ ที่มี Al 2 O 3, MgO, CaO และเหล็กออกไซด์
บางครั้งแร่อาจมีโลหะอื่นๆ เป็นจำนวนมาก (สังกะสี ทอง เงิน และอื่นๆ)
มีสองวิธีที่ทราบในการรับทองแดงจากแร่:
- ไฮโดรเมทัลโลหการ;
- ไพโรเมทัลโลหการ
ไม่พบการใช้งานที่กว้างขวางเนื่องจากไม่สามารถสกัดโลหะมีค่าพร้อมกับทองแดงได้
วิธีการไพโรเมทัลโลจิคัลเหมาะสำหรับการแปรรูปแร่ทั้งหมดและรวมถึงการดำเนินการต่อไปนี้:
- การเตรียมแร่เพื่อการถลุง
- ละลายเป็นด้าน;
- การแปลงด้าน
- การกลั่นทองแดง
การเตรียมแร่สำหรับการหลอม
การเตรียมแร่เกี่ยวข้องกับการทำให้บริสุทธิ์และการคั่ว การเสริมสมรรถนะแร่ทองแดงทำได้โดยการลอยอยู่ในน้ำ ผลลัพธ์ที่ได้คือทองแดงเข้มข้นที่ประกอบด้วยทองแดงมากถึง 35% และกำมะถันสูงถึง 50% สารเข้มข้นมักจะถูกเผาในเตาเผาฟลูอิไดซ์เบดเพื่อลดปริมาณกำมะถันให้เป็นค่าที่เหมาะสมที่สุด ในระหว่างการเผา ซัลเฟอร์จะถูกออกซิไดซ์ที่อุณหภูมิ 750–800 °C และกำมะถันบางส่วนจะถูกกำจัดออกไปพร้อมกับก๊าซ ผลลัพธ์ที่ได้คือผลิตภัณฑ์ที่เรียกว่าถ่าน
ละลายเป็นแมท
การหลอมสำหรับเนื้อด้านจะดำเนินการในเตาเผาแบบสะท้อนกลับหรือเตาไฟฟ้าที่อุณหภูมิ 1250 – 1300 °C แร่ทองแดงเข้มข้นที่เผาแล้วจะถูกส่งไปในการหลอม ในระหว่างการให้ความร้อน ซึ่งเกิดปฏิกิริยารีดักชันของคอปเปอร์ออกไซด์และออกไซด์ของเหล็กที่สูงขึ้น
6CuO + FeS = 3Cu 2 O + FeO + SO 2
เฟ2S + 3Fe3 O 4 + 5SiO 2 = 5(2FeO SiO 2) + SO 2
อันเป็นผลมาจากปฏิสัมพันธ์ของ Cu 2 O กับ FeS ทำให้ Cu 2 S เกิดขึ้นตามปฏิกิริยา:
Cu 2 O + FeS = Cu 2 S + FeO
ทองแดงและเหล็กซัลไฟด์หลอมรวมเข้าด้วยกันจนเกิดเป็นด้าน และซิลิเกตของเหล็กหลอมละลายซึ่งจะละลายออกไซด์อื่นๆ ให้เกิดเป็นตะกรัน ด้านมี Cu 15 – 55%; 15 – 50% เฟอ; S. Slag 20 – 30% ประกอบด้วย SiO 2, FeO, CaO, Al 2 O 3 เป็นส่วนใหญ่
ด้านและตะกรันจะถูกปล่อยออกมาเมื่อสะสมผ่านรูพิเศษ
แปลงแมท
การแปลงสภาพด้านจะดำเนินการในเครื่องหลอมทองแดง (รูปที่ 44) โดยการเป่าด้วยอากาศเพื่อออกซิไดซ์เหล็กซัลไฟด์ เปลี่ยนเหล็กเป็นตะกรันและแยกทองแดงพุพอง
คอนเวอร์เตอร์มีความยาว 6 - 10 ม. และเส้นผ่านศูนย์กลางภายนอก 3 - 4 ม. การเทด้านที่หลอมละลายการระบายผลิตภัณฑ์ที่หลอมละลายและการกำจัดก๊าซจะดำเนินการผ่านคอที่อยู่ตรงกลางของตัวคอนเวอร์เตอร์ ในการเป่าผ่านด้านนั้น อากาศอัดจะถูกส่งผ่าน tuyeres ซึ่งอยู่ตามแนวคอนเวอร์เตอร์เจเนราทริกซ์ ในผนังด้านหนึ่งของตัวแปลงมีรูสำหรับการโหลดฟลักซ์ควอทซ์แบบนิวแมติกซึ่งจำเป็นในการเอาเหล็กออกจากตะกรัน
กระบวนการล้างจะดำเนินการในสองช่วง ในช่วงแรก มีการเทด้านลงในคอนเวอร์เตอร์และจ่ายฟลักซ์ควอทซ์ ในช่วงเวลานี้จะเกิดปฏิกิริยาออกซิเดชันของซัลไฟด์
เฟอร์ริกออกไซด์ที่เกิดขึ้นจะทำปฏิกิริยากับฟลักซ์ควอทซ์และถูกกำจัดออกไปในตะกรัน
เมื่อตะกรันสะสม มันก็จะถูกระบายออกบางส่วนและส่วนใหม่ของการเคลือบด้านเดิมจะถูกเทลงในคอนเวอร์เตอร์ เพื่อรักษาระดับของการเคลือบในคอนเวอร์เตอร์ไว้ในระดับหนึ่ง ในช่วงที่สอง cuprous ออกไซด์จะทำปฏิกิริยากับคอปเปอร์ซัลไฟด์ เกิดเป็นทองแดงที่เป็นโลหะ
ดังนั้นจากการเป่าจึงได้ทองแดงพุพองที่มี Cu 98.4 - 99.4% ทองแดงพุพองที่เกิดขึ้นจะถูกเทลงในแม่พิมพ์แบนบนเครื่องหล่อสายพาน
เทคโนโลยีการผลิตแมกนีเซียม
วิธีหลักในการผลิตแมกนีเซียมคืออิเล็กโทรไลต์ การผลิตแมกนีเซียมด้วยไฟฟ้าจากสารละลายที่เป็นน้ำเป็นไปไม่ได้ เนื่องจากศักยภาพทางเคมีไฟฟ้าของแมกนีเซียมนั้นเป็นลบมากกว่าศักยภาพของการปล่อยไอออนไฮโดรเจนที่แคโทด ดังนั้นอิเล็กโทรลิซิสของแมกนีเซียมจึงดำเนินการจากเกลือหลอมเหลว
ส่วนประกอบหลักของอิเล็กโทรไลต์คือแมกนีเซียมคลอไรด์ MgCl2 และเพื่อลดจุดหลอมเหลวของอิเล็กโทรไลต์และเพิ่มการนำไฟฟ้า จึงมีการนำ NaCl, CaCl2, KCl และ NaF และ CaF2 จำนวนเล็กน้อยเข้าไป
วัตถุดิบหลักสำหรับการผลิตแมกนีเซียม ได้แก่ คาร์นัลไลท์ (MgCl2 KCl 6H2O), แมกนีไซต์ (MgCO3), โดโลไมต์ (CaCO3 MgCO3), บิสโชไฟต์ (MgCl2 6H2O) แมกนีเซียมปริมาณมากที่สุดได้มาจากคาร์นัลไลท์
ขั้นตอนหลักของการผลิตแมกนีเซียม:
1. คาร์นัลไลท์;
2. การเสริมคุณค่าของคาร์นัลไลท์
3. การคายน้ำของคาร์นัลไลท์
4. การผลิตแมกนีเซียมด้วยไฟฟ้า
5. การกลั่นแมกนีเซียม
6. แมกนีเซียม
การเสริมคาร์นัลไลท์เป็นขั้นตอนแรกของการแปรรูป สาระสำคัญของกระบวนการเสริมสมรรถนะอยู่ที่การแยก KCl และสิ่งเจือปนที่ไม่ละลายน้ำโดยการถ่ายโอน MgCl2 และ KCl ลงในสารละลายที่เป็นน้ำ เมื่อสารละลายที่ได้ถูกทำให้เย็นลงในเครื่องตกผลึกแบบสุญญากาศ ผลึกของคาร์นัลไลต์เทียม MgCl2 KCl 6H2O จะตกตะกอน ซึ่งถูกแยกออกจากกันโดยการกรอง
คาร์นัลไลท์จะถูกทำให้ขาดน้ำในสองขั้นตอน ขั้นตอนแรกดำเนินการในเตาเผาแบบท่อหรือเตาเผาฟลูอิไดซ์เบดที่อุณหภูมิ 550-600 ° C ภายใต้อิทธิพลของความร้อนของก๊าซร้อนคาร์นัลไลต์จะถูกทำให้แห้งและหลังการบำบัดดังกล่าวจะมีความชื้น 3-4%
ขั้นตอนที่สองของการขาดน้ำจะดำเนินการโดยการละลายคาร์นัลไลต์ที่ได้รับหลังจากขั้นตอนแรกในเตาไฟฟ้าตามด้วยการตกตะกอนของแมกนีเซียมออกไซด์หรือโดยการคลอรีนคาร์นัลไลต์ในสถานะหลอมเหลว
การผลิตแมกนีเซียมด้วยไฟฟ้า เพื่อจุดประสงค์นี้ มีการใช้อิเล็กโทรไลเซอร์ซึ่งบุด้วยอิฐไฟร์เคลย์ด้านใน แอโนดเป็นแผ่นกราไฟท์ และแคโทดเป็นแผ่นเหล็กที่อยู่ทั้งสองด้านของแอโนด
สำหรับการสลายตัวด้วยไฟฟ้าของแมกนีเซียมคลอไรด์กระแสไฟฟ้า 2.7-2.8 V จะถูกส่งผ่านอิเล็กโทรไลต์
ผลจากการสลายตัวด้วยไฟฟ้าของแมกนีเซียมคลอไรด์ ไอออนของคลอรีนจึงเกิดขึ้น ซึ่งเคลื่อนที่ไปยังขั้วบวก และหลังจากปล่อยออกมา จะทำให้เกิดฟองคลอรีนที่โผล่ออกมาจากอิเล็กโทรไลต์ ไอออนแมกนีเซียมจะเคลื่อนที่ไปที่แคโทด และหลังจากปล่อยออกมาจะถูกปล่อยออกมาบนพื้นผิว ทำให้เกิดเป็นหยดของแมกนีเซียมเหลว แมกนีเซียมมีความหนาแน่นต่ำกว่าอิเล็กโทรไลต์ ดังนั้นจึงลอยไปที่พื้นผิวในช่องแคโทด จากจุดที่ถูกดึงออกเป็นระยะๆ โดยใช้ทัพพีสุญญากาศ
ในระหว่างกระบวนการอิเล็กโทรไลซิส ความเข้มข้นของคลอไรด์อื่นๆ ในอิเล็กโทรไลต์จะเพิ่มขึ้นเนื่องจากการสิ้นเปลือง MgCl2 ดังนั้นส่วนหนึ่งของอิเล็กโทรไลต์ที่ใช้แล้วจะถูกลบออกจากอ่างเป็นระยะ ๆ และเท MgCl2 หรือคาร์นัลไลท์ที่ละลายลงไปแทน อันเป็นผลมาจากการสลายตัวของสิ่งสกปรกบางส่วน ตะกอนจะเกิดขึ้นที่ด้านล่างของอ่าง ซึ่งจะถูกกำจัดออกจากอ่างเป็นประจำ
การกลั่นแมกนีเซียม ในอ่างอิเล็กโทรไลซิส จะได้แมกนีเซียมดิบซึ่งมีสารเจือปน 5% ได้แก่ สารเจือปนที่เป็นโลหะ (Fe, Na, K, Al, Ca) และสารเจือปนที่ไม่ใช่โลหะ (MgCl2, KCl, NaCl, CaCl2, MgO) แมกนีเซียมถูกทำให้บริสุทธิ์ (บริสุทธิ์) โดยการละลายด้วยฟลักซ์


