07.06.2019
Deskripsi produk aluminium yang diproduksi. Proses teknologi produksi aluminium
Proses teknologi Produksi aluminium mencakup tiga tahap utama:
1. Pembuatan alumina dari bijih aluminium;
2. Pembuatan aluminium dari alumina;
3. Proses pemurnian aluminium.
Dan dalam hal ini perlu menggunakan peralatan berikut:
peralatan untuk sistem distribusi alumina terpusat;
elektroliser;
busbar katoda;
instalasi pembersihan gas kering;
derek perakitan, teknologi dan pengecoran;
unit aspirasi;
peralatan pengecoran;
peralatan bengkel perakitan anoda;
struktur logam bangunan produksi.
Pembuatan alumina dari bijih merupakan tahap produksi aluminium
Alumina dapat diproduksi dengan tiga metode: asam, basa, dan elektrolitik. Yang paling populer adalah metode alkaline. Inti dari metode ini adalah larutan aluminium dengan sangat cepat mulai terurai dengan masuknya aluminium hidroksida, dan larutan yang tersisa dari penguraian setelah penguapan dengan pengadukan intensif pada suhu 170 C dapat kembali melarutkan alumina yang terkandung dalam bauksit. Metode ini memiliki tahapan utama sebagai berikut:
1. Persiapan bauksit, yang melibatkan penghancuran dan penggilingan di pabrik khusus. Alkali kaustik, bauksit dan sedikit kapur dikirim ke pabrik. Pulp yang dihasilkan dikirim untuk pencucian.
2. Pencucian bauksit berarti dekomposisi kimianya dari kombinasi dengan larutan berair alkali. Dalam hal ini, aluminium oksida hidrat bila digabungkan dengan alkali akan menjadi larutan dalam bentuk natrium aluminat, dan silika yang terkandung dalam bauksit bila digabungkan dengan alkali akan menjadi larutan dalam bentuk natrium silikat. Dalam larutan, senyawa berikut: natrium aluminat dan natrium silikat membentuk natrium aluminosilikat yang tidak larut. Residu ini mengandung oksida besi dan titanium, yang memberikan warna merah pada residu. Residu ini adalah lumpur merah. Ketika pelarutan natrium aluminat yang dihasilkan selesai, natrium aluminat diencerkan dengan larutan alkali berair sementara suhu diturunkan hingga 100°C.
3. Pemisahan lumpur merah dan larutan aluminat satu sama lain terjadi akibat pencucian dalam pengental. Setelah itu lumpur merah mengendap, dan sisa larutan aluminat disaring.
4. Penguraian larutan aluminat. Itu disaring dan dikirim ke wadah besar dengan mixer. Dari dari solusi ini ketika didinginkan hingga 60°C dan diaduk terus-menerus, aluminium hidroksida dilepaskan. Karena proses berlangsung tidak merata dan sangat lambat, dan pertumbuhan kristal aluminium hidroksida sangat penting selama pemrosesan lebih lanjut, banyak hidroksida padat juga ditambahkan ke wadah ini dengan pencampur - pengurai.
5. Aluminium hidroksida diproduksi dalam filter vakum dan hidrosiklon. Sebagian besar hidroksida sebagai bahan benih dikembalikan ke prosedur dekomposisi. Setelah dicuci dengan air, residu dikirim untuk kalsinasi; dan filtratnya juga kembali ke proses.
6. Dehidrasi aluminium hidroksida merupakan tahap akhir produksi alumina. Itu terjadi di tungku berbentuk tabung yang terus berputar. Aluminium hidroksida mentah dikeringkan sepenuhnya dan didehidrasi ketika melewati tungku.
Pembuatan aluminium dari alumina selama produksi juga berlangsung dalam beberapa tahap.
1. Elektrolisis aluminium oksida terjadi pada suhu dalam elektroliser 970°C. Elektroliser memiliki bak yang dilapisi dengan blok karbon, yang dihubungkan dengan arus listrik. Aluminium cair yang dilepaskan dikumpulkan di atas dasar batubara, dan dari sana dipompa keluar secara teratur. Anoda karbon direndam dalam elektrolit di atas, oksigen terbakar di atmosfer, yang dilepaskan dari aluminium oksida, dan pada saat yang sama karbon monoksida atau dioksida dilepaskan.
2.Elektrolisis aluminium klorida dilakukan dengan mengubah aluminium oksida dalam bejana reaksi menjadi aluminium klorida. Setelah itu, aluminium klorida dielektrolisis dalam bak berinsulasi. Klorin yang dilepaskan disedot dan dikirim untuk didaur ulang. Dan aluminium mengendap di katoda.
3. Reduksi aluminium klorida dengan mangan, yang melepaskan aluminium. Kondensasi yang terkendali menghilangkan kontaminan terkait klorin dari aliran mangan klorida. Ketika klorin dilepaskan, mangan klorida diubah menjadi oksida mangan, yang kemudian direduksi menjadi mangan, yang dapat didaur ulang.
Proses pemurnian aluminium dalam produksi aluminium
Pemurnian elektrolisis dengan dekomposisi larutan garam berair tidak mungkin dilakukan untuk aluminium. Karena tingkat pemurnian aluminium industri, yang diperoleh dengan elektrolisis lelehan kriolit-alumina, tidak akan mencukupi untuk beberapa tujuan, bahkan aluminium yang lebih murni diperoleh dari limbah logam dan aluminium industri melalui pemurnian. Metode pemurnian yang paling umum adalah elektrolisis tiga lapis.
Aluminium digunakan dalam pembuatan bahan peledak (alumatol, ammonal). Berbagai senyawa aluminium banyak digunakan. Produksi dan konsumsi aluminium terus meningkat, jauh melampaui laju pertumbuhan produksi tembaga, baja, seng, dan timbal.
Untuk memperoleh tembaga digunakan bijih tembaga, serta limbah tembaga dan paduannya. Bijihnya mengandung 1–6% tembaga. Bijih yang mengandung kurang dari 0,5% tembaga tidak diproses, karena dengan tingkat teknologi saat ini, mengekstraksi tembaga darinya tidak menguntungkan.
Dalam bijih, tembaga ditemukan dalam bentuk senyawa belerang (CuFeS 2 - kalkopirit, Cu 2 S - kalkosit, CuS - coveline), oksida (CuO, CuO) dan hidrokarbonat
Bijih gangue terdiri dari pirit (FeS 2), kuarsa (SiO 2), berbagai senyawa yang mengandung Al 2 O 3, MgO, CaO, dan oksida besi.
Bijih terkadang mengandung sejumlah besar logam lain (seng, emas, perak, dan lain-lain).
Ada dua metode yang diketahui untuk memperoleh tembaga dari bijih:
- hidrometalurgi;
- pirometalurgi.
Hidrometalurgi belum banyak diterapkan karena ketidakmampuan mengekstraksi logam mulia bersama dengan tembaga.
Metode pirometalurgi cocok untuk memproses semua bijih dan mencakup operasi berikut:
- persiapan bijih untuk peleburan;
- meleleh menjadi matte;
- konversi matte;
- pemurnian tembaga.
Mempersiapkan bijih untuk peleburan
Persiapan bijih melibatkan benefisiasi dan pemanggangan. Pengayaan bijih tembaga dilakukan dengan cara flotasi. Hasilnya adalah konsentrat tembaga yang mengandung hingga 35% tembaga dan hingga 50% belerang. Konsentrat biasanya dibakar dalam tungku fluidized bed untuk mengurangi kandungan sulfur ke nilai optimal. Selama pembakaran, belerang dioksidasi pada suhu 750–800 °C, dan sebagian belerang dihilangkan dengan gas. Hasilnya adalah produk yang disebut cinder.
Meleleh untuk matte
Peleburan matte dilakukan di tungku reverberatori atau listrik pada suhu 1250 – 1300 °C. Konsentrat bijih tembaga yang dikalsinasi memasuki proses peleburan, selama pemanasan dimana reaksi reduksi oksida tembaga dan oksida yang lebih tinggi kelenjar
6CuO + FeS = 3Cu 2 O + FeO + SO 2
FeS + 3Fe 3 O 4 + 5SiO 2 = 5(2FeO SiO 2) + SO 2
Akibat interaksi Cu 2 O dengan FeS, terbentuk Cu 2 S menurut reaksi:
Cu 2 O + FeS = Cu 2 S + FeO
Tembaga dan besi sulfida menyatu satu sama lain untuk membentuk matte, dan besi silikat cair, melarutkan oksida lainnya, membentuk terak. Matte mengandung 15 – 55% Cu; 15 – 50% Fe; 20 – 30% S. Terak sebagian besar terdiri dari SiO 2, FeO, CaO, Al 2 O 3.
Matte dan terak dilepaskan saat terakumulasi melalui lubang khusus.
Mengubah matte
Konversi matte dilakukan dalam konverter peleburan tembaga (Gambar 44) dengan meniupkannya dengan udara untuk mengoksidasi besi sulfida, mengubah besi menjadi terak dan memisahkan tembaga melepuh.
Konverter memiliki panjang 6 - 10 m dan diameter luar 3 - 4 m.Penuangan matte cair, pengeringan produk leleh dan pembuangan gas dilakukan melalui leher yang terletak di bagian tengah badan konverter. Untuk meniup matte, udara bertekanan disuplai melalui tuyere yang terletak di sepanjang generatrix konverter. Di salah satu dinding ujung konverter terdapat lubang di mana fluks kuarsa dimuat secara pneumatik, yang diperlukan untuk menghilangkan besi ke dalam terak.
Proses purging dilakukan dalam dua periode. Pada periode pertama, matte dituangkan ke dalam konverter dan fluks kuarsa disuplai. Selama periode ini, reaksi oksidasi sulfida terjadi
Oksida besi yang dihasilkan bereaksi dengan fluks kuarsa dan dihilangkan menjadi terak.
Saat terak terakumulasi, sebagian terkuras dan sebagian baru dari matte asli dituangkan ke dalam konverter, mempertahankan tingkat matte tertentu di dalam konverter. Pada periode kedua, oksida tembaga bereaksi dengan tembaga sulfida membentuk logam tembaga
Jadi, dari hasil peniupan diperoleh tembaga melepuh yang mengandung 98,4 - 99,4% Cu. Tembaga melepuh yang dihasilkan dituangkan ke dalam cetakan datar pada mesin pengecoran sabuk.
Teknologi produksi magnesium
Metode utama produksi magnesium adalah elektrolitik. Produksi magnesium secara elektrolitik dari larutan berair tidak mungkin dilakukan, karena potensi elektrokimia magnesium jauh lebih negatif daripada potensi pelepasan ion hidrogen di katoda. Oleh karena itu, elektrolisis magnesium dilakukan dari garam cairnya.
Komponen utama elektrolit adalah magnesium klorida MgCl2, dan untuk mengurangi titik leleh elektrolit dan meningkatkan konduktivitas listriknya, NaCl, CaCl2, KCl dan sejumlah kecil NaF dan CaF2 dimasukkan ke dalamnya.
Bahan baku utama produksi magnesium adalah karnalit (MgCl2 KCl 6H2O), magnesit (MgCO3), dolomit (CaCO3 MgCO3), bischofite (MgCl2 6H2O). Jumlah magnesium terbesar diperoleh dari karnalit.
Tahapan utama produksi magnesium:
1. Karnalit;
2. Pengayaan karnalit;
3. Dehidrasi karnalit;
4. Produksi magnesium secara elektrolitik;
5. Pemurnian magnesium;
6. magnesium.
Pengayaan karnalit adalah tahap pertama pengolahannya. Inti dari proses pengayaan adalah pemisahan KCl dan pengotor yang tidak larut dengan mentransfer MgCl2 dan KCl ke dalam larutan berair. Ketika larutan yang dihasilkan didinginkan dalam alat kristalisasi vakum, kristal karnalit buatan MgCl2 KCl 6H2O mengendap, yang dipisahkan dengan penyaringan.
Karnalit mengalami dehidrasi dalam dua tahap. Tahap pertama dilakukan dalam tungku tabung atau tungku fluidized bed pada suhu 550-600 °C. Di bawah pengaruh panas gas yang dipanaskan, karnalit mengalami dehidrasi dan setelah perlakuan tersebut mengandung 3-4% uap air.
Dehidrasi tahap kedua dilakukan dengan melelehkan karnalit yang diperoleh setelah tahap pertama dalam tungku listrik, diikuti dengan pengendapan magnesium oksida, atau dengan mengklorinasi karnalit dalam keadaan cair.
Produksi magnesium secara elektrolitik. Untuk tujuan ini, digunakan elektroliser, yang dilapisi dengan batu bata fireclay di bagian dalam. Anoda adalah pelat grafit, dan katoda adalah pelat baja yang terletak di kedua sisi anoda.
Untuk dekomposisi elektrolitik magnesium klorida, arus 2,7-2,8 V dilewatkan melalui elektrolit.
Sebagai hasil dari dekomposisi elektrolitik magnesium klorida, ion klor terbentuk, yang berpindah ke anoda dan, setelah dibuang, menciptakan gelembung klor yang muncul dari elektrolit. Ion magnesium berpindah ke katoda dan, setelah dilepaskan, dilepaskan ke permukaan, membentuk tetesan magnesium cair. Magnesium memiliki kepadatan yang lebih rendah daripada elektrolit, sehingga ia mengapung ke permukaannya di ruang katoda, kemudian dikeluarkan secara berkala menggunakan sendok vakum.
Selama proses elektrolisis, konsentrasi klorida lain dalam elektrolit meningkat karena konsumsi MgCl2. Oleh karena itu, secara berkala sebagian elektrolit bekas dikeluarkan dari bak dan sebagai gantinya dituangkan lelehan MgCl2 atau karnalit. Sebagai hasil penguraian sebagian pengotor, lumpur terbentuk di dasar bak, yang secara teratur dikeluarkan dari bak.
Pemurnian magnesium. Dalam rendaman elektrolisis, diperoleh magnesium mentah, yang mengandung 5% pengotor: pengotor logam (Fe, Na, K, Al, Ca) dan pengotor non-logam (MgCl2, KCl, NaCl, CaCl2, MgO). Magnesium dimurnikan (dimurnikan) dengan cara peleburan dengan fluks.
Salah satu legenda yang sangat meragukan menceritakan bahwa suatu hari seorang pria mendatangi kaisar Romawi Tiberius (42 SM - 37 M) dengan membawa mangkuk logam yang tidak bisa pecah. Bahan mangkuk tersebut diduga berasal dari alumina (Al 2 O 3) dan oleh karena itu pastilah aluminium. Khawatir logam yang terbuat dari tanah liat tersebut akan mendevaluasi emas dan perak, Tiberius memerintahkan agar kepala pria itu dipenggal, untuk berjaga-jaga. Tentu saja, cerita ini sulit dipercaya: aluminium asli tidak terdapat di alam, dan pada zaman Kekaisaran Romawi tidak mungkin ada sarana teknis yang memungkinkan untuk mengekstraksi aluminium dari senyawanya.
Dalam hal prevalensinya di alam, aluminium menempati urutan pertama di antara logam; kandungannya di kerak bumi adalah 7,45%. Namun, meskipun tersebar luas di alam, aluminium merupakan salah satu logam langka hingga akhir abad ke-19. Aluminium tidak ditemukan dalam bentuk murni karena aktivitas kimianya yang tinggi. Hal ini terutama ditemukan dalam bentuk senyawa dengan oksigen dan silikon - aluminosilikat.
Hanya batuan yang kaya akan alumina (Al 2 O 3) dan terdapat dalam jumlah besar di permukaan bumi yang dapat dijadikan sebagai bijih aluminium. Batuan tersebut antara lain bauksit, nepheline - (Na, K) 2 OּAl 2 O 3 ּ2SiO 2, alunit - (Na, K) 2 SO 4 ּAl 2 (SO 4) 3 ּ4Al(OH) 3 dan kaolin (tanah liat), field spar (ortoklas) - K 2 OּAl 2 O 3 ּ6SiO 2 .
Bijih utama untuk memproduksi aluminium adalah bauksit. Mengandung aluminium dalam bentuk hidroksida Al(OH), AlOOH, korundum Al 2 O 3 dan kaolinit Al 2 O 3 ּ2SiO 2 ּ2H 2 O. Komposisi kimia bauksit terdiri dari: 28-70% alumina; 0,5-20% silika; 2-50% besi oksida; 0,1-10% titanium oksida. DI DALAM Akhir-akhir ini Nepheline dan alunit mulai digunakan sebagai bijih.
Deposit besar bauksit terletak di Ural, di distrik Tikhvin di wilayah Leningrad, di wilayah Altai dan Krasnoyarsk.
Nepheline (KּNa 2 OּAl 2 O 3 ּ2SiO 2) merupakan bagian dari batuan nepheline apatit (di Semenanjung Kola).
Aluminium pertama kali diisolasi dalam bentuk bebasnya pada tahun 1825 oleh fisikawan Denmark Oersted dengan mereaksikan amalgam kalium dengan aluminium klorida. Pada tahun 1827 Ahli kimia Jerman Wöhler menyempurnakan metode Oersted dengan mengganti amalgam kalium dengan kalium logam:
AlCl 3 + 3K→3KCl + Al (Reaksi berlangsung dengan pelepasan panas).
Pada tahun 1854, Sainte-Clair Deville di Perancis pertama kali menggunakan metode Wöhler untuk produksi industri aluminium, menggunakan natrium yang lebih murah daripada kalium, dan sebagai pengganti aluminium klorida higroskopis - klorida ganda yang lebih stabil dari aluminium dan natrium. Pada tahun 1865, ahli kimia fisik Rusia N. N. Beketov menunjukkan kemungkinan menggantikan aluminium dengan magnesium dari kriolit cair. Reaksi ini digunakan pada tahun 1888 untuk memproduksi aluminium di pabrik Jerman pertama di Gmelingen. Produksi aluminium dengan apa yang disebut metode “kimia” ini dilakukan dari tahun 1854 hingga 1890. Selama 35 tahun, total sekitar 20 ton aluminium diproduksi dengan menggunakan metode ini.
Pada akhir tahun 80-an abad sebelumnya metode kimia menggantikan metode elektrolitik, yang memungkinkan penurunan tajam biaya aluminium dan menciptakan prasyarat bagi pesatnya perkembangan industri aluminium. Pendiri metode elektrolitik modern dalam produksi aluminium, Héroux di Prancis dan Hall di AS, secara independen mengajukan permohonan serupa pada tahun 1886 untuk mematenkan metode memproduksi aluminium dengan elektrolisis alumina yang dilarutkan dalam kriolit cair. Sejak munculnya paten Heroux dan Hall, industri aluminium modern dimulai, yang selama lebih dari 115 tahun keberadaannya telah berkembang menjadi salah satu cabang metalurgi terbesar.
Proses teknologi produksi aluminium terdiri dari tiga tahap utama:
1). Memperoleh alumina (Al 2 O 3) dari bijih aluminium;
2). Produksi aluminium dari alumina;
3). Pemurnian aluminium.
Memperoleh alumina dari bijih.
Alumina diproduksi dengan tiga cara: basa, asam dan elektrolitik. Yang paling luas adalah metode alkaline (metode K.I. Bayer, dikembangkan di Rusia pada akhir abad sebelumnya dan digunakan untuk memproses bauksit bermutu tinggi dengan sejumlah kecil (hingga 5-6%) silika). Sejak itu, implementasi teknisnya telah ditingkatkan secara signifikan. Diagram produksi alumina menggunakan metode Bayer ditunjukkan pada Gambar. 1.
Inti dari metode ini adalah larutan aluminium cepat terurai ketika aluminium hidroksida dimasukkan ke dalamnya, dan larutan sisa dekomposisi setelah penguapan dalam kondisi pengadukan intensif pada suhu 169-170 o C dapat kembali melarutkan alumina yang terkandung dalam bauksit. Metode ini terdiri dari operasi dasar berikut:
1). Persiapan bauksit, yang terdiri dari penghancuran dan penggilingan di pabrik; pabrik disuplai dengan bauksit, alkali kaustik dan tidak sejumlah besar kapur, yang meningkatkan pelepasan Al 2 O 3; pulp yang dihasilkan diumpankan untuk pencucian;
2). Pencucian bauksit (saat ini, blok autoklaf berbentuk bulat yang masih digunakan telah sebagian digantikan oleh autoklaf berbentuk tabung, dimana pencucian terjadi pada suhu 230-250 ° C (500-520 K), yang terdiri dari dekomposisi kimianya dari interaksi dengan larutan alkali berair; Ketika bereaksi dengan alkali, aluminium oksida hidrat masuk ke dalam larutan dalam bentuk natrium aluminat:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH) 3 + NaOH → NaAlO 2 + 2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H 2 O;
dalam larutan, natrium aluminat dan natrium silikat membentuk natrium aluminosilikat yang tidak larut; oksida titanium dan besi masuk ke dalam residu yang tidak larut, memberikan warna merah pada residu; residu ini disebut lumpur merah. Setelah pelarutan selesai, natrium aluminat yang dihasilkan diencerkan dengan larutan alkali berair sekaligus menurunkan suhu sebesar 100°C;
3). Pemisahan larutan aluminat dari lumpur merah, biasanya dilakukan dengan cara dicuci dengan pengental khusus; Akibatnya lumpur merah mengendap, dan larutan aluminat ditiriskan lalu disaring (diklarifikasi). Dalam jumlah terbatas, lumpur digunakan, misalnya sebagai bahan tambahan semen. Tergantung pada jenis bauksit, 1 ton aluminium oksida yang dihasilkan menghasilkan 0,6-1,0 ton lumpur merah (residu kering);
4). Dekomposisi larutan aluminat. Itu disaring dan dipompa ke dalam wadah besar dengan agitator (pengurai). Aluminium hidroksida Al(OH) 3 diekstraksi dari larutan lewat jenuh setelah pendinginan hingga 60°C (330 K) dan pengadukan konstan. Karena proses ini berlangsung lambat dan tidak merata, dan pembentukan serta pertumbuhan kristal aluminium hidroksida sangat penting selama pemrosesan lebih lanjut, sejumlah besar hidroksida padat - sebutir - ditambahkan ke pengurai:
Na 2 OּAl 2 O 3 +4H 2 O→Al(OH) 3 +2NaOH;
5). Isolasi aluminium hidroksida dan klasifikasinya; hal ini terjadi pada hidrosiklon dan filter vakum, dimana endapan yang mengandung 50-60% partikel Al(OH) dipisahkan dari larutan aluminat. Sebagian besar hidroksida dikembalikan ke proses dekomposisi sebagai bahan benih, yang tetap beredar dalam jumlah yang tidak berubah. Residu setelah dicuci dengan air menuju kalsinasi; filtrat juga dikembalikan ke sirkulasi (setelah konsentrasi dalam evaporator - untuk pencucian bauksit baru);
6). Dehidrasi aluminium hidroksida (kalsinasi); Ini adalah langkah terakhir dalam produksi alumina; ini dilakukan dalam tanur putar berbentuk tabung, dan baru-baru ini juga dalam tanur dengan pergerakan material yang turbulen pada suhu 1150-1300 o C; aluminium hidroksida mentah, melewati tanur putar, dikeringkan dan didehidrasi; Ketika dipanaskan, transformasi struktural berikut terjadi secara berurutan:
| Al(OH) 3 →AlOOH→ γ-Al 2 O 3 → α-Al 2 O 3 | |||
| 200 o C– | 950 o C– | 1200 oC. | |
Akhirnya alumina yang dikalsinasi mengandung 30-50% α-Al 2 O 3 (korundum), sisanya γ-Al 2 O 3.
Metode ini mengekstraksi 85-87% dari total alumina yang dihasilkan. Aluminium oksida yang dihasilkan bersifat tahan lama senyawa kimia dengan titik leleh 2050 o C.
Pembuatan aluminium dari oksidanya
Elektrolisis aluminium oksida
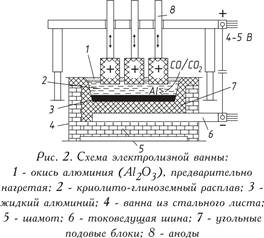
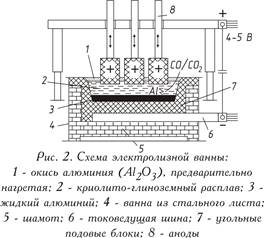 Reduksi elektrolitik aluminium oksida yang dilarutkan dalam lelehan berbasis kriolit dilakukan pada suhu 950-970°C dalam elektroliser. Elektroliser terdiri dari bak yang dilapisi dengan blok karbon, di bagian bawahnya disuplai arus listrik. Aluminium cair yang dilepaskan di tungku, yang berfungsi sebagai katoda, lebih berat daripada garam cair elektrolit, oleh karena itu aluminium dikumpulkan di dasar batubara, yang kemudian dipompa keluar secara berkala (Gbr. 2). Anoda karbon direndam dalam elektrolit di atasnya, yang terbakar dalam atmosfer oksigen yang dilepaskan dari aluminium oksida, melepaskan karbon monoksida (CO) atau karbon dioksida (CO2). Dalam prakteknya, dua jenis anoda digunakan:
Reduksi elektrolitik aluminium oksida yang dilarutkan dalam lelehan berbasis kriolit dilakukan pada suhu 950-970°C dalam elektroliser. Elektroliser terdiri dari bak yang dilapisi dengan blok karbon, di bagian bawahnya disuplai arus listrik. Aluminium cair yang dilepaskan di tungku, yang berfungsi sebagai katoda, lebih berat daripada garam cair elektrolit, oleh karena itu aluminium dikumpulkan di dasar batubara, yang kemudian dipompa keluar secara berkala (Gbr. 2). Anoda karbon direndam dalam elektrolit di atasnya, yang terbakar dalam atmosfer oksigen yang dilepaskan dari aluminium oksida, melepaskan karbon monoksida (CO) atau karbon dioksida (CO2). Dalam prakteknya, dua jenis anoda digunakan:
a) anoda Zederberg yang dapat terbakar sendiri, terdiri dari briket, yang disebut “roti” massa Zederberg (batubara abu rendah dengan kadar tar batubara 25-35%), dimasukkan ke dalam cangkang aluminium; di bawah pengaruh suhu tinggi, massa anoda dibakar (disinter);
b) anoda yang dipanggang atau “kontinu” yang terbuat dari balok karbon besar (misalnya, 1900x600x500 mm dengan berat sekitar 1,1 ton).
Kekuatan arus dalam elektroliser adalah 150.000 A. Mereka dihubungkan ke jaringan secara seri, yaitu, suatu sistem (seri) diperoleh - deretan elektroliser yang panjang.
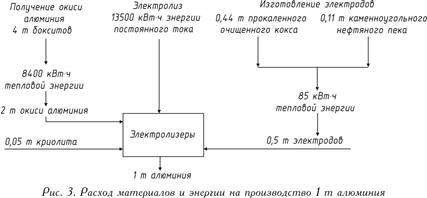
Tegangan operasi pada bak, 4-5 V, secara signifikan lebih tinggi daripada tegangan penguraian aluminium oksida, karena rugi-rugi tegangan pada berbagai bagian sistem. Keseimbangan bahan baku dan energi pada produksi 1 ton aluminium disajikan pada Gambar. 3.
Elektrolisis aluminium klorida (metode Alcoa)
 Dalam bejana reaksi, aluminium oksida diubah terlebih dahulu menjadi aluminium klorida. Kemudian, dalam bak berinsulasi rapat, terjadi elektrolisis AlCl 3 yang dilarutkan dalam garam cair KCl dan NaCl. Klorin yang dilepaskan selama proses ini disedot dan disuplai untuk didaur ulang; aluminium diendapkan pada katoda.
Dalam bejana reaksi, aluminium oksida diubah terlebih dahulu menjadi aluminium klorida. Kemudian, dalam bak berinsulasi rapat, terjadi elektrolisis AlCl 3 yang dilarutkan dalam garam cair KCl dan NaCl. Klorin yang dilepaskan selama proses ini disedot dan disuplai untuk didaur ulang; aluminium diendapkan pada katoda.
Manfaat metode ini sebelum elektrolisis lelehan kriolit-alumina cair (Al 2 O 3 dilarutkan dalam kriolit Na 3 AlF 6) pertimbangkan: menghemat energi hingga 30%; kemungkinan menggunakan aluminium oksida, yang tidak cocok untuk elektrolisis tradisional (misalnya, Al 2 O 3 dengan konten tinggi silikon); mengganti kriolit yang mahal dengan garam yang lebih murah; hilangnya bahaya pelepasan fluorida.
Reduksi aluminium klorida dengan mangan (metode Toth)
 Ketika direduksi dengan mangan, aluminium dilepaskan dari aluminium klorida. Melalui kondensasi terkendali, kontaminan terkait klorin dilepaskan dari aliran mangan klorida. Ketika klorin dilepaskan, mangan klorida dioksidasi menjadi oksida mangan, yang kemudian direduksi menjadi mangan, cocok untuk penggunaan sekunder. Informasi dalam publikasi yang ada sangat tidak akurat pada kasus ini Anda harus mengabaikan evaluasi metode ini.
Ketika direduksi dengan mangan, aluminium dilepaskan dari aluminium klorida. Melalui kondensasi terkendali, kontaminan terkait klorin dilepaskan dari aliran mangan klorida. Ketika klorin dilepaskan, mangan klorida dioksidasi menjadi oksida mangan, yang kemudian direduksi menjadi mangan, cocok untuk penggunaan sekunder. Informasi dalam publikasi yang ada sangat tidak akurat pada kasus ini Anda harus mengabaikan evaluasi metode ini.
Memperoleh aluminium olahan
Untuk aluminium, pemurnian elektrolisis dengan dekomposisi larutan garam berair tidak mungkin dilakukan. Karena untuk beberapa tujuan tingkat pemurnian aluminium industri (Al 99,5 - Al 99,8), yang diperoleh dengan elektrolisis lelehan kriolit-alumina, tidak mencukupi, bahkan aluminium yang lebih murni (Al 99, 99 R) diperoleh dari aluminium industri atau limbah logam dengan pengilangan. Metode pemurnian yang paling terkenal adalah elektrolisis tiga lapis.
Pemurnian dengan elektrolisis tiga lapis
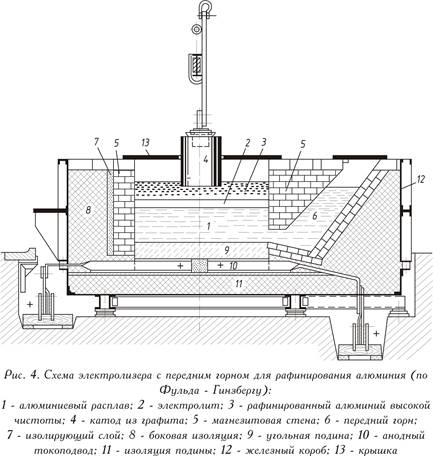
Dilapisi dengan lembaran baja, beroperasi dengan arus searah (ditunjukkan pada Gambar 4 - lihat di atas), bak pemurnian terdiri dari perapian batubara dengan kabel arus dan lapisan magnesit insulasi panas. Berbeda dengan elektrolisis lelehan kriolit-alumina, anoda di sini biasanya adalah logam cair yang dimurnikan (lapisan anoda bawah). Elektrolitnya terdiri dari fluorida murni atau campuran barium klorida dan aluminium dan natrium fluorida (lapisan tengah). Aluminium, yang larut dari lapisan anoda ke dalam elektrolit, dilepaskan di atas elektrolit (lapisan katoda atas). Logam murni berfungsi sebagai katoda. Arus disuplai ke lapisan katoda oleh elektroda grafit.
Bak mandi beroperasi pada suhu 750-800°C, konsumsi listrik 20 kWh per 1 kg aluminium murni, yaitu sedikit lebih tinggi dibandingkan dengan elektrolisis aluminium konvensional.
Logam anoda mengandung 25-35% Cu; 7-12% Zn; 6-9% Si; Fe sampai 5% dan sedikit mangan, nikel, timbal dan timah, sisanya (40-55%) adalah aluminium. Semua logam berat dan silikon tetap berada di lapisan anoda selama pemurnian. Kehadiran magnesium dalam elektrolit menyebabkan perubahan komposisi elektrolit yang tidak diinginkan atau slagging yang parah. Untuk menghilangkan magnesium, terak yang mengandung magnesium diolah dengan fluks atau gas klor.
Hasil pemurnian menghasilkan aluminium murni (99,99%) dan produk segregasi (produk Ziger), yang mengandung logam berat dan silikon dan dilepaskan dalam bentuk larutan alkali dan residu kristal. Larutan basa adalah produk limbah, dan residu padat digunakan untuk deoksidasi.
Aluminium olahan biasanya memiliki komposisi sebagai berikut,%: Fe 0,0005-0,002; Si 0,002-0,005; Cu 0,0005-0,002; Zn 0,0005-0,002; jejak mg; Semua sisanya.
Aluminium olahan diolah menjadi produk setengah jadi dengan komposisi tertentu atau dicampur dengan magnesium (lihat Tabel 1.2.).
TABEL 1.2. Komposisi kimia aluminium kemurnian tinggi dan aluminium primer menurut DIN 1712, lembar 1.
| Merek | Nomor | Pengotor yang diijinkan*, % | |||||||
| Total | termasuk | ||||||||
| Ya | Fe | Ti | Cu | Zn | lainnya | ||||
| A199.99R | 3.0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 | |
| A199.9H | 3.0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 | |
| A199.8H | 3.0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199.7H | 3.0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199.5H** | 3.0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 | |
| A199H | 3.0200 | 1,0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 | |
* Sebisa mungkin ditentukan dengan menggunakan metode penelitian konvensional. ** Aluminium murni untuk teknik kelistrikan (aluminium konduktor) disuplai dalam bentuk aluminium primer 99,5 yang mengandung tidak lebih dari 0,03% (Ti + Cr + V + Mn); dalam hal ini ditunjuk E-A1, nomor material 3.0256. Kalau tidak, itu sesuai dengan standar VDE-0202. |
|||||||||
Pemurnian dengan kompleks organoaluminium dan peleburan zona
Aluminium dengan tingkat kemurnian lebih tinggi dari kadar A1 99,99 R dapat diperoleh dengan pemurnian elektrolisis aluminium murni atau murni komersial menggunakan senyawa organoaluminum kompleks aluminium sebagai elektrolit. Elektrolisis terjadi pada suhu sekitar 1000°C antara elektroda aluminium padat dan pada prinsipnya mirip dengan pemurnian elektrolisis tembaga. Sifat elektrolit menentukan kebutuhan untuk bekerja tanpa akses udara dan pada kepadatan arus yang rendah.
Elektrolisis pemurnian jenis ini, awalnya hanya digunakan pada skala laboratorium, sudah dilakukan pada skala industri kecil - beberapa ton logam diproduksi per tahun. Derajat pemurnian nominal logam yang dihasilkan adalah 99,999-99,9999%. Aplikasi potensial untuk logam dengan kemurnian ini termasuk teknik kelistrikan kriogenik dan elektronik.
Dimungkinkan untuk menggunakan metode pemurnian yang dipertimbangkan dalam pelapisan listrik.
Kemurnian yang lebih tinggi lagi - secara nominal hingga A1 99,99999 - dapat diperoleh dengan peleburan zona logam berikutnya. Saat mengolah aluminium dengan kemurnian tinggi menjadi produk setengah jadi, lembaran atau kabel, hal ini perlu diperhitungkan suhu rendah rekristalisasi logam, lakukan tindakan pencegahan khusus. Sifat penting dari logam olahan adalah konduktivitas listriknya yang tinggi dalam kisaran suhu kriogenik.
Produksi aluminium sekunder
Daur ulang bahan mentah sekunder dan limbah produksi menguntungkan secara ekonomi. Paduan sekunder yang dihasilkan memenuhi sekitar 25% dari total permintaan aluminium.
 Area penerapan paduan sekunder yang paling penting adalah produksi coran berbentuk aluminium. Dalam DIN 1725, lembar 2, bersama dengan nilai paduan standar, banyak nilai paduan yang diproduksi oleh pengecoran logam terdaftar. Daftar paduan yang diproduksi oleh pabrik ini, selain paduan standar, juga mengandung beberapa paduan non-standar.
Area penerapan paduan sekunder yang paling penting adalah produksi coran berbentuk aluminium. Dalam DIN 1725, lembar 2, bersama dengan nilai paduan standar, banyak nilai paduan yang diproduksi oleh pengecoran logam terdaftar. Daftar paduan yang diproduksi oleh pabrik ini, selain paduan standar, juga mengandung beberapa paduan non-standar.
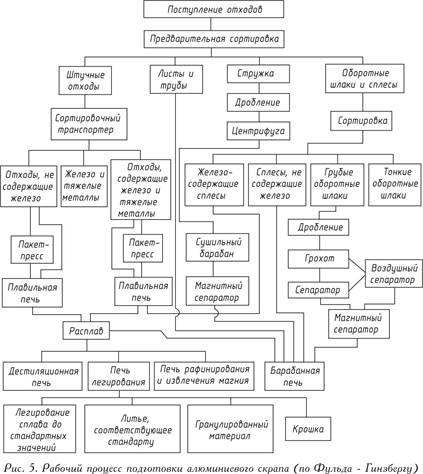
Persiapan skrap aluminium yang sempurna dalam berbagai proporsi hanya dapat dilakukan di pabrik peleburan yang dilengkapi peralatan khusus. Gagasan tentang proses kerja yang kompleks di pabrik tersebut diberikan pada Gambar. 5.
Sampah dicairkan setelah pemilahan awal yang kasar. Besi, nikel atau tembaga yang terkandung dalam limbah ini, yang titik lelehnya lebih tinggi dari titik leleh aluminium, bila dicairkan dalam tungku ambang batas, akan tetap berada di dalamnya, dan aluminium tersebut dilebur. Untuk menghilangkan inklusi non-logam seperti oksida, nitrida, karbida atau gas dari limbah, logam cair diolah dengan garam atau (lebih rasional) ditiup dengan gas - klorin atau nitrogen.
Berbagai metode diketahui untuk menghilangkan pengotor logam dari lelehan, misalnya penambahan magnesium dan penyedotan debu - metode Becksche; penambahan seng atau merkuri diikuti dengan evakuasi - metode subhalogen. Penghapusan magnesium dibatasi oleh masuknya klorin ke dalam logam cair. Dengan memasukkan aditif yang ditentukan secara tepat oleh komposisi lelehan, diperoleh paduan tuang tertentu.
Produksi aluminium kemurnian teknis
Metode elektrolitik adalah satu-satunya metode yang digunakan di seluruh dunia untuk produksi logam aluminium dengan kemurnian teknis. Semua metode lain (zincothermic, karbidotermal, subklorida, nitrida, dll.) yang dengannya aluminium dapat diekstraksi dari bijih aluminium telah dikembangkan pada skala laboratorium dan industri percontohan, tetapi belum menemukan penerapan praktisnya.
Untuk memproduksi paduan aluminium-silikon, metode elektrotermal, yang pertama kali dikembangkan dan diterapkan pada skala industri di Uni Soviet, berhasil digunakan. Ini terdiri dari dua tahap: pada tahap pertama, paduan aluminium-silikon primer yang mengandung 60-63% Al diperoleh dengan reduksi langsung bijih aluminium-silikon dalam tungku listrik bijih-termal; pada tahap kedua, paduan primer diencerkan dengan aluminium teknis, menghasilkan silumin dan paduan aluminium-silikon cor dan tempa lainnya. Penelitian sedang dilakukan untuk mengekstraksi aluminium dengan kemurnian teknis dari paduan primer.
Secara umum produksi aluminium dengan metode elektrolitik meliputi produksi alumina (aluminium oksida) dari bijih aluminium, produksi garam fluorida (kriolit, aluminium fluorida dan natrium fluorida), produksi massa anoda karbon, pembakaran anoda karbon dan blok katoda dan bahan pelapis lainnya, serta produksi aluminium elektrolitik yang sebenarnya, yang merupakan tahap akhir dari metalurgi aluminium modern.
Karakteristik untuk produksi alumina, garam fluorida dan produk karbon adalah persyaratan untuk tingkat kemurnian maksimum bahan-bahan ini, karena lelehan kriolit-alumina yang mengalami elektrolisis tidak boleh mengandung pengotor unsur yang lebih elektropositif daripada aluminium, yang dilepaskan di katoda dalam pertama, akan mencemari logam.
Pada alumina kadar G-00, G-0 dan G-1, yang terutama digunakan dalam elektrolisis, kandungan SiO 2 adalah 0,02-0,05%, aFe 2 O 3 - 0,03-0,05%. Kriolit rata-rata mengandung 0,36-0,38% SiO 2 dan 0,05-0,06% Fe 2 O 3, aluminium fluorida mengandung 0,30-0,35% (SiO 2 + Fe 2 O 3). Massa anoda mengandung tidak lebih dari 0,25% SiO 2 dan 0,20% Fe 2 O 3.
Bijih aluminium terpenting yang menghasilkan alumina adalah bauksit. Dalam bauksit, aluminium hadir dalam bentuk aluminium hidroksida. Di Uni Soviet, selain bauksit, batuan nepheline digunakan untuk memproduksi alumina - natrium dan kalium aluminosilikat, serta batuan alunit, di mana aluminium ditemukan dalam bentuk sulfatnya. Bahan mentah untuk produksi massa anoda dan blok anoda yang dipanggang adalah bahan karbon murni - minyak bumi atau pitch coke dan tar batubara sebagai pengikat, dan untuk produksi kriolit dan garam fluorida lainnya - kalsium fluorida (fluorspar).
Selama produksi elektrolitik aluminium, alumina Al 2 O 3, yang dilarutkan dalam kriolit cair Na 3 AlF 6, terurai secara elektrokimia dengan pelepasan kation aluminium di katoda (aluminium cair), dan ion yang mengandung oksigen (ion oksigen) di karbon. anoda.
Oleh ide-ide modern, kriolit dalam keadaan cair berdisosiasi menjadi ion dan: , dan alumina - menjadi ion kompleks dan: ![]() , yang berada dalam kesetimbangan dengan ion sederhana:
, yang berada dalam kesetimbangan dengan ion sederhana: ![]() ,
, ![]() .
.
Proses utama yang terjadi di katoda adalah reduksi ion aluminium trivalen: Al 3+ + 3 e→ Al (Saya).
Seiring dengan proses utama, pelepasan ion aluminium trivalen yang tidak lengkap dimungkinkan dengan pembentukan ion monovalen: Al 3+ + 2 e→ Al + (II) dan terakhir pelepasan ion monovalen dengan pelepasan logam: Al + + e→ Al(III).
Dalam kondisi tertentu (konsentrasi ion Na+ yang relatif tinggi, panas dll.) pelepasan ion natrium dapat terjadi dengan pelepasan logam: Na++ e→ Na(IV). Reaksi (II) dan (IV) menyebabkan penurunan arus keluaran aluminium.
Ion oksigen dilepaskan di anoda karbon: 2O 2– – 4 e→ HAI 2 . Namun, oksigen tidak dilepaskan dalam bentuk bebas, karena oksigen mengoksidasi karbon anoda untuk membentuk campuran CO 2 dan CO.
Reaksi keseluruhan yang terjadi pada elektroliser dapat direpresentasikan dengan persamaan Al 2 O 3 + X C ↔ 2Al + (2 X–3)CO + (3– X)CO 2 .
Komposisi elektrolit elektroliser aluminium industri, selain komponen utama - kriolit, aluminium fluorida dan alumina, termasuk sejumlah kecil (total hingga 8-9%) beberapa garam lainnya - CaF 2, MgF 2, NaCl dan LiF (aditif), yang meningkatkan beberapa sifat fisik dan kimia elektrolit dan dengan demikian meningkatkan efisiensi elektroliser. Kandungan alumina maksimum dalam elektrolit biasanya 6-8%, menurun selama proses elektrolisis. Ketika elektrolit kehabisan alumina, sebagian alumina lainnya dimasukkan ke dalamnya. Untuk pengoperasian normal elektroliser aluminium, rasio NaF:AlF 3 dalam elektrolit dipertahankan dalam kisaran 2,7-2,8 dengan menambahkan porsi kriolit dan aluminium fluorida.
Dalam produksi aluminium, elektroliser dengan anoda karbon yang dipanggang sendiri dan suplai arus samping atau atas digunakan, serta elektroliser dengan anoda karbon yang dipanggang sebelumnya. Desain elektroliser yang paling menjanjikan dengan anoda panggang, yang memungkinkan untuk meningkatkan daya unit, mengurangi konsumsi spesifik listrik arus searah untuk elektrolisis, memperoleh logam yang lebih murni, meningkatkan kondisi kerja sanitasi dan higienis, serta mengurangi emisi zat berbahaya. ke atmosfer.
Parameter teknis utama dan indikator kinerja elektroliser aluminium dari berbagai jenis diberikan dalam tabel. 1.3.
TABEL 1.3
PARAMETER TEKNIS UTAMA DAN INDIKATOR KINERJA ELEKTROLISER ALUMINIUM
| Parameter dan indikator | Dengan anoda yang dapat menyala sendiri | Dengan anoda panggang | |
samping pasokan saat ini |
pasokan arus atas | ||
| Kekuatan saat ini, kA | 60-120 | 60-155 | 160-255 |
| Produktivitas harian elektroliser, t | 0,42-0,85 | 0,40-1,10 | 1,10-1,74 |
| Kerapatan arus anodik, A/cm 2 | 0,80-0,90 | 0,65-0,70 | 0,70-0,89 |
| Tegangan rata-rata pada elektroliser, V | 4,45-4,65 | 4,50-4,70 | 4,30-4,50 |
| Keluaran saat ini, % | 85-88 | 84-86 | 85-89 |
| Koefisien konsumsi per 1 ton aluminium: | |||
| Listrik DC, kWh | 15100-16200 | 15500-17300 | 14500-15500 |
| alumina, kg | 1920-1940 | 1920-1940 | 1920-1940 |
| massa anoda, kg | 520-560 | 560-620 | - |
| anoda panggang, kg | - | - | 540-600 |
| Garam fluorida dalam satuan fluor, kg | 20-30 | 25-35 | 15-25 |
Aluminium primer yang diekstraksi dari elektroliser (aluminium mentah) mengandung sejumlah pengotor, yang dapat dibagi menjadi tiga kelompok: non-logam (garam fluorida, α- dan γ-alumina, aluminium karbida dan nitrida, partikel karbon yang terperangkap secara mekanis ketika logam dituangkan dari elektroliser); logam (besi, silikon), yang berasal dari bahan mentah, bahan batubara dan elemen struktur elektroliser; berbentuk gas - terutama hidrogen, yang terbentuk dalam logam sebagai hasil dekomposisi elektrolitik air yang memasuki elektrolit dengan bahan mentah.
Dari pengotor logam, selain besi dan silikon, kandungan galium, seng, titanium, mangan, natrium, vanadium, kromium, dan tembaga paling banyak. Kandungan ini dan beberapa pengotor mikro logam lainnya di dalamnya aluminium elektrolitik diberikan di bawah ini, %:
Sumber utama pengotor mikro logam dalam aluminium adalah alumina, yang tergantung pada jenis bahan bakunya, mungkin mengandung galium, seng, kalium, fosfor, belerang, vanadium, titanium, dan kromium. Bahan berkarbon (massa anoda, anoda panggang, produk katoda) berfungsi sebagai sumber pengotor mikro seperti vanadium, titanium, mangan, seng.
Dengan elektrolisis lelehan kriolit-alumina, asalkan bahan awal murni digunakan (terutama bahan alumina dan karbon), dimungkinkan untuk memperoleh aluminium mentah dengan kadar A85 dan A8 (99,85 dan 99,80%). Bagian terbesar logam dari kadar ini (60-70% dari total output) diproduksi dalam elektroliser dengan anoda panggang, serta dalam elektroliser dengan suplai arus lateral (hingga 70% dari total produksi). Dalam elektroliser dengan anoda yang dapat dipanggang sendiri dan suplai arus atas, keluaran aluminium mentah kelas A8 rendah (1-3%), dan logam kelas A85 tidak dapat diperoleh karena pengotor besi yang signifikan memasuki aluminium dari sumber bahan non-mentah. (pin anoda, bagian pengumpul gas besi cor, alat teknologi, unit katoda).
Aluminium primer cair, diekstraksi dari elektroliser menggunakan sendok vakum, memasuki departemen pengecoran untuk pemurnian guna menghilangkan kotoran non-logam dan gas dan diproses lebih lanjut menjadi produk komersial (babi, batangan berbentuk silinder dan datar, batang kawat, dll.). Sebelum pengecoran, aluminium mentah disimpan dalam keadaan cair di tungku tahan listrik (mixer) atau di tungku gema gas. Dalam tungku ini, mereka tidak hanya secara rasional mencampurkan sebagian aluminium cair dari berbagai komposisi, tetapi juga membersihkan sebagian dari inklusi non-logam, lapisan oksida, dan natrium.
Aluminium dicetak dari mixer menjadi ingot menggunakan mesin pengecoran tipe konveyor; ingot silinder dan datar diproduksi dengan pengecoran semi kontinyu, dan unit khusus dari gabungan pengecoran dan penggulungan digunakan untuk memproduksi batang kawat.
Di pabrik peleburan aluminium dalam negeri, saat menuang ingot, aluminium yang berasal dari mixer ke dalam kristalisasi mesin pengecoran mengalami jenis pemurnian yang paling sederhana - menyaring lelehan melalui jaring fiberglass dengan ukuran sel mulai dari 0,6 × 0,6 hingga 1,7 × 1,7 mm. Metode ini memungkinkan Anda membersihkan aluminium hanya dari inklusi oksida yang sangat kasar; metode yang lebih maju adalah dengan menyaring lelehan melalui jaring fiberglass dalam aliran ke atas. Dengan metode penyaringan ini, partikel inklusi oksida, yang bertabrakan dengan jaring, tidak ditangkap oleh aliran lelehan, tetapi disimpan di bagian bawah parit pengecoran.
Untuk memurnikan aluminium secara bersamaan dari pengotor non-logam dan hidrogen, metode filtrasi melalui filter fluks yang dikombinasikan dengan pembersihan nitrogen berhasil digunakan. Elektrolit asam dari elektroliser aluminium dapat digunakan sebagai fluks. Sebagai hasil pemurnian tersebut, kandungan hidrogen dalam aluminium berkurang dari 0,22 menjadi 0,16 cm 3 per 100 g logam.
Dalam aluminium primer yang digunakan untuk produksi paduan sistem Al-Mg, kandungan natrium tidak boleh melebihi 0,001%. Hal ini disebabkan adanya natrium pada paduan tersebut memperburuk sifat mekanik dan sifat kinerja lainnya dari produk yang digunakan di sejumlah sektor perekonomian nasional.
Paling metode yang efektif pemurnian aluminium secara simultan dari natrium, hidrogen, dan pengotor non-logam adalah meniup logam cair dengan campuran gas nitrogen dengan 2-10% klorin, dimasukkan ke dalam lelehan dalam bentuk gelembung kecil menggunakan perangkat khusus. Metode pemurnian ini memungkinkan penurunan kandungan natrium dalam aluminium menjadi 0,0003-0,001% pada konsumsi campuran gas 0,8 hingga 1,5 m 3 /t logam.
Konsumsi listrik untuk produksi 1 ton aluminium komersial dari logam mentah dengan menggunakan tungku listrik adalah 150-200 kWh; kerugian logam yang tidak dapat diperbaiki pada tahap pengecoran adalah 1,5-5%, tergantung pada jenis produk komersial.
Memproduksi aluminium dengan kemurnian tinggi
Untuk mendapatkan aluminium dengan kemurnian tinggi (nilai A995-A95), aluminium primer dengan kemurnian teknis dimurnikan secara elektrolitik. Hal ini memungkinkan untuk mengurangi kandungan pengotor logam dan gas dalam aluminium dan dengan demikian secara signifikan meningkatkan konduktivitas listrik, keuletan, reflektifitas, dan ketahanan terhadap korosi.
Pemurnian aluminium secara elektrolitik dilakukan dengan elektrolisis garam cair menggunakan metode tiga lapis. Inti dari metode ini adalah sebagai berikut. Ada tiga lapisan cair dalam elektroliser pemurnian. Yang lebih rendah, yang terberat, terletak di bagian bawah konduktif dan berfungsi sebagai anoda; itu disebut paduan anoda dan merupakan paduan aluminium halus dengan tembaga, yang ditambahkan untuk membuat lapisan lebih berat. Lapisan tengah adalah cairan elektrolit; kerapatannya lebih kecil dari kerapatan paduan anoda dan lebih tinggi dari kerapatan aluminium murni (katoda) yang terletak di atas elektrolit (lapisan cair ketiga atas).
Selama pelarutan anodik, semua pengotor yang lebih elektropositif daripada aluminium (Fe, Si, Ti, Cu, dll.) tetap berada dalam paduan anodik tanpa masuk ke dalam elektrolit. Hanya aluminium yang akan larut secara anodik, yang berupa ion Al 3+ masuk ke dalam elektrolit: Al– 3 e→ Al 3+ .
Selama elektrolisis, ion aluminium ditransfer ke katoda, di mana mereka dilepaskan: Al 3+ + 3 e→ Al. Akibatnya, lapisan aluminium halus yang meleleh terakumulasi di katoda.
Jika paduan anoda mengandung pengotor yang lebih elektronegatif daripada aluminium (misalnya Ba, Na, Mg, Ca), maka pengotor tersebut dapat larut secara elektrokimia di anoda bersama dengan aluminium dan masuk ke elektrolit dalam bentuk ion. Karena kandungan pengotor elektronegatif dalam aluminium mentah rendah, pengotor tersebut tidak terakumulasi dalam jumlah yang signifikan di dalam elektrolit. Praktis tidak ada pelepasan ion-ion ini di katoda, karena potensial elektrodanya lebih elektronegatif daripada aluminium.
Elektrolit yang digunakan dalam pemurnian elektrolitik aluminium di Uni Soviet dan di sebagian besar negara adalah elektrolit fluorida-klorida, yang komposisinya adalah 55-60% BaCl 2, 35-40% AlF 4 + NaF dan 0-4% NaCl . Rasio molar NaF: AlF 3 dipertahankan pada 1,5-2,0; titik leleh elektrolit 720-730°C; suhu proses elektrolisis sekitar 800°C; kerapatan elektrolit 2,7 g/cm3.
Paduan anoda dibuat dari aluminium primer dan tembaga murni (99,90-99,95% Cu), yang dimasukkan ke dalam logam dalam jumlah 30-40%. Massa jenis paduan anoda cair komposisi ini adalah 3-3,5 g/cm 3 ; massa jenis aluminium katoda cair murni adalah 2,3 g/cm 3 . Dengan rasio kepadatan ini, kondisi yang diperlukan untuk pemisahan yang baik dari tiga lapisan cair tercipta.
Dalam sistem kuaterner Al-Cu-Fe-Si, yang mencakup paduan anoda, terbentuk eutektik dengan titik leleh 520°C. Dengan mendinginkan paduan anodik yang mengandung pengotor besi dan silikon dalam jumlah di atas konsentrasi eutektik, besi dan silikon dapat dilepaskan ke dalam fase padat dalam bentuk senyawa intermetalik FeSiAl 5 dan Cu 2 FeAl 7 . Karena suhu paduan anoda di kantong elektroliser adalah 30-40°C lebih rendah dari suhu paduan anoda di ruang kerja bak, endapan intermetalik padat akan dilepaskan di dalamnya (karena besi dan silikon terakumulasi di dalamnya). paduan anoda). Dengan menghilangkan endapan ini secara berkala, paduan anoda dibersihkan (tanpa memperbaruinya) dari kotoran besi dan silikon. Karena galium terkonsentrasi pada paduan anoda, sedimen yang diekstraksi dari elektroliser (30-40 kg per 1 ton aluminium) dapat berfungsi sebagai sumber logam ini.
Untuk pemurnian elektrolitik, digunakan elektroliser, yang dalam desainnya menyerupai elektroliser dengan anoda panggang untuk produksi elektrolitik aluminium primer, tetapi memiliki sambungan kutub yang berbeda: perapian berfungsi sebagai anoda, dan baris atas elektroda berfungsi sebagai katoda. Elektroliser modern untuk pemurnian aluminium secara elektrolitik dirancang untuk kekuatan arus hingga 75 kA.
Di bawah ini adalah indikator teknis dan ekonomi utama elektroliser pada tahun 1979, yang dicapai oleh perusahaan dalam negeri (1, 2, 3).
Efisiensi arus elektrokimia yang dihitung dari logam yang dituangkan dari elektroliser adalah 97-98%. Efisiensi arus aktual, dihitung berdasarkan jumlah logam komersial, adalah 92-96%.
| Kekuatan saat ini, kA | 23,5 | 62,9 | 69,8* |
| Tegangan rata-rata, V | 5,43 | 5,68 | 5,69 |
| Keluaran saat ini, % | 95,7 | 93,0 | 92,7 |
| Konsumsi daya DC, kW ּ h/t | 17 370 | 18 700 | 19 830 |
| Total listrik AC, kW ּ h/t | 18 670 | 19 590 | 20 780 |
| Tingkat, cm | |||
| katoda aluminium | 16,6 | 12,9 | 14,6 |
| elektrolit | 13,3 | 11,6 | 14,2 |
| paduan anoda | 40,1 | 29,5 | 30,0 |
| Koefisien konsumsi, kg/t: | |||
| barium klorida | 40,5 | 41,5 | 27,0 |
| kriolit | 27,7 | 21,0 | 16,5 |
| aluminium fluorida | 6,7 | 13,1 | 3,8 |
| natrium klorida | 1,0 | 4,8 | - |
| aluminium mentah | 1020 | 1028 | 1032 |
| grafit | 11,9 | 11,5 | 16,6 |
| tembaga | 9,8 | 15,5 | 16,4 |
| Produksi aluminium dengan kemurnian tinggi, % nilai: | |||
| A995 | 47,8** | 3,5 | 2,1 |
| A99 | 30,4 | 67,1 | 54,2 |
| A97 | 8,3 | 21,5 | 43,7 |
| A95 | 10,4 | 7,9 | - |
| di bawah A95 | 3,1 | - | - |
* Indikator produksi aluminium dengan kemurnian tinggi. ** Nilai menurut elektroliser tanpa dekomposisi. |
|||
Faktor utama yang mengurangi efisiensi arus, selain rugi-rugi arus searah akibat pelepasan ion yang lebih elektronegatif, rugi-rugi logam akibat oksidasi dan rugi-rugi mekanis aluminium, adalah pengoperasian elektroliser dengan pelepasan logam bermutu rendah, yang dikembalikan ke paduan anoda untuk pemurnian selanjutnya. Periode pengoperasian elektroliser ini terjadi selama pengaktifan elektroliser dan pelanggaran rezim teknologi.
Pemurnian aluminium secara elektrolitik adalah proses yang sangat intensif energi. Konsumsi listrik pada arus bolak-balik, termasuk energi yang dikeluarkan untuk pembuatan elektrolit dan paduan anoda, pengoperasian alat ventilasi dan kendaraan, serta rugi-rugi untuk mengubah arus bolak-balik menjadi arus searah, adalah 18,5-21,0 ribu kWh per 1 ton listrik. aluminium. Efisiensi energi elektroliser pemurnian tidak melebihi 5-7%, yaitu 93-95% energi dikonsumsi dalam bentuk kehilangan panas, yang dilepaskan terutama di lapisan elektrolit (sekitar 80-85% dari total masukan panas). Oleh karena itu, cara utama untuk lebih mengurangi konsumsi energi spesifik untuk pemurnian aluminium secara elektrolitik adalah dengan meningkatkan isolasi termal elektroliser (terutama bagian atas struktur) dan mengurangi lapisan elektrolit (mengurangi jarak antarelektroda).
Kemurnian aluminium yang dimurnikan dengan metode tiga lapis adalah 99,995%; itu ditentukan oleh perbedaannya dengan lima pengotor utama - besi, silikon, tembaga, seng dan titanium. Jumlah logam dengan kadar ini yang diperoleh bisa mencapai 45-48% dari total output (tanpa terurai dengan kadar yang lebih rendah).
Namun perlu dicatat bahwa aluminium yang dimurnikan secara elektrolitik mengandung pengotor logam lain dalam jumlah yang lebih kecil, sehingga mengurangi kemurnian absolut aluminium tersebut. Analisis radioaktivasi memungkinkan untuk mendeteksi hingga 30 pengotor dalam aluminium yang dimurnikan secara elektrolitik, yang kandungan totalnya kira-kira 60ּ10–4%. Oleh karena itu, kemurnian aluminium olahan dibandingkan dengan pengotor tersebut adalah 99,994%.
Selain pengotor yang ditentukan oleh GOST (lihat Tabel 1.1), kelas paling umum (A99) dari aluminium yang dimurnikan secara elektrolitik mengandung, %: Cr 0,00016; V 0,0001; Ga 0,0006; Pb 0,002; Sn 0,00005; Ca 0,002-0,003; Tidak 0,001-0,008; Mn 0,001-0,007; Mg 0,001-0,007; Sebagai<0,0001; Sb<0,00002; Bi<0,00001; Cd<0,000001; S 0,0007.
Salah satu sumber pencemaran aluminium katoda adalah timah arus grafit, yang mengandung besi dan silikon oksida dan selalu bersentuhan dengan aluminium olahan. Jika arus disuplai langsung ke katoda aluminium melalui batangan aluminium dan alat yang terbuat dari grafit sangat murni digunakan, logam dengan kemurnian 99,999% dapat diperoleh melalui perbedaan pengotor yang terdeteksi (Fe, Si, Cu, Zn). dan Ti). Logam ini rata-rata mengandung %: Si 0,0002; Fe 0,00032; Cu 0,0002; Zn 0,0002 dan Ti 0,00005. Namun karena kesulitan teknis, metode penyediaan arus ini belum diterapkan secara luas di industri.
Produksi aluminium dengan kemurnian tinggi
Aluminium dengan kemurnian tinggi (grade A999) dapat diproduksi dengan tiga cara: peleburan zona, distilasi melalui subhalida, dan elektrolisis senyawa aluminium-organik. Dari metode yang terdaftar untuk memproduksi aluminium dengan kemurnian tinggi, metode peleburan zona menerima penerapan praktis di Uni Soviet.
Prinsip peleburan zona adalah melewatkan zona cair berulang kali di sepanjang batangan aluminium. Menurut koefisien distribusi K=S televisi /DENGAN w (dimana DENGAN TV - konsentrasi pengotor dalam padatan dan DENGAN g - dalam fase cair), yang sangat menentukan efisiensi pemurnian dari pengotor; pengotor ini dapat dibagi menjadi tiga kelompok. Kelompok pertama mencakup pengotor yang menurunkan titik leleh aluminium; mereka memilikinya KE<1 , selama peleburan zona, terkonsentrasi di zona cair dan dipindahkan ke bagian akhir ingot. Pengotor tersebut antara lain Ga, Sn, Be, Sb, Ca, Th, Fe, Co, Ni, Ce, Te, Ba, Pt, Au, Bi, Pb, Cd, In, Na, Mg, Cu, Si, Ge, Zn . Kelompok kedua meliputi pengotor yang meningkatkan titik leleh aluminium; mereka dicirikan K>1 dan selama peleburan zona, mereka terkonsentrasi di bagian padat (awal) ingot. Pengotor tersebut antara lain Nb, Ta, Cr, Ti, Mo, V. Golongan ketiga meliputi pengotor yang koefisien distribusinya sangat mendekati satu (Mn, Sc). Kotoran ini praktis tidak dihilangkan selama peleburan zona aluminium.
Aluminium yang dimaksudkan untuk peleburan zona harus melalui beberapa persiapan, yang terdiri dari filtrasi, degassing, dan pengawetan. Filtrasi diperlukan untuk menghilangkan lapisan oksida tahan api dan tahan lama dari aluminium yang tersebar di logam. Aluminium oksida yang ada dalam aluminium cair dapat menciptakan pusat kristalisasi selama pemadatannya, yang mengarah pada produksi ingot polikristalin dan terganggunya efek redistribusi pengotor antara logam padat dan zona cair. Aluminium disaring dalam ruang hampa (tekanan sisa 0,1-0,4 Pa) melalui lubang di dasar wadah grafit dengan diameter 1,5-2 mm. Degassing awal aluminium sebelum peleburan zona (juga pemanasan dalam ruang hampa) dilakukan untuk mencegah percikan logam ketika zona dicairkan jika proses dilakukan dalam ruang hampa tinggi. Tahap terakhir dalam mempersiapkan aluminium untuk peleburan zona adalah mengetsa permukaannya dengan campuran asam klorida pekat dan asam nitrat.
Karena aluminium memiliki aktivitas kimia yang signifikan dan terutama grafit murni digunakan sebagai bahan utama wadah (perahu), peleburan zona aluminium dilakukan dalam ruang hampa atau dalam atmosfer gas inert (argon, helium).
Peleburan zona dalam ruang hampa memastikan kemurnian aluminium yang lebih besar karena penguapan beberapa pengotor selama evakuasi (logam magnesium, seng, kadmium, alkali dan alkali tanah), dan juga menghilangkan kontaminasi logam yang dimurnikan dengan pengotor akibat penggunaan aluminium. gas inert pelindung. Peleburan zona aluminium dalam ruang hampa dapat dilakukan dengan pemompaan terus menerus dari tabung kuarsa, di mana perahu grafit dengan ingot aluminium ditempatkan, serta dalam ampul kuarsa tertutup, dari mana udara pertama kali dipompa keluar hingga tekanan sisa. sekitar 1ּ10 –3 Pa.
Untuk membuat zona cair pada ingot aluminium selama peleburan zona, pemanasan dapat diterapkan menggunakan tungku resistansi kecil atau arus frekuensi tinggi. Menghidupkan tungku tahan listrik tidak memerlukan peralatan yang rumit; tungku mudah dioperasikan. Satu-satunya kelemahan dari metode pemanasan ini adalah kecilnya penampang batang aluminium yang sedang dimurnikan.
Pemanasan induksi dengan arus frekuensi tinggi adalah cara ideal untuk membuat zona cair pada ingot selama peleburan zona. Metode pemanasan frekuensi tinggi (selain memungkinkan peleburan zona ingot dengan penampang besar) memiliki keuntungan penting karena logam cair terus tercampur di zona tersebut; ini memfasilitasi difusi atom pengotor dari bagian depan kristalisasi ke kedalaman lelehan.
Untuk pertama kalinya, produksi industri aluminium dengan kemurnian tinggi melalui peleburan zona dikuasai di pabrik peleburan aluminium Volkhov pada tahun 1965 menggunakan instalasi UZPI-3 yang dikembangkan oleh VAMI. Instalasi ini dilengkapi dengan empat retort kuarsa dengan pemanas induksi, sedangkan induktor dapat dipindahkan dan wadah logam tidak bergerak. Produktivitasnya adalah 20 kg logam per siklus pembersihan. Selanjutnya, instalasi semua logam berperforma lebih tinggi UZPI-4 dibuat dan dioperasikan secara komersial pada tahun 1972 di Pabrik Peleburan Aluminium Volkhov.
Efisiensi pemurnian aluminium selama peleburan zona dapat dicirikan oleh data berikut. Jika kandungan total pengotor dalam aluminium yang dimurnikan secara elektrolitik adalah (30±60)ּ10–4%, maka setelah zona peleburan berkurang menjadi (2,8±3,2)ּ10–4%, yaitu 15-20 kali lipat. Hal ini sesuai dengan hambatan listrik sisa aluminium ρ ○ (pada suhu helium cair 4,2 K), masing-masing (20±40)ּ10 –10 dan (1,8±2.1)ּ10 –10 atau kemurnian 99.997-99.994 dan 99.9997% . Di meja 1.4 (lihat di bawah) menunjukkan data analisis radioaktivasi tentang kandungan pengotor tertentu dalam aluminium yang dimurnikan secara zona dan dimurnikan secara elektrolitik. Data ini menunjukkan penurunan yang kuat dalam kandungan sebagian besar pengotor, meskipun pengotor seperti mangan dan skandium praktis tidak dihilangkan selama peleburan zona.
Dalam beberapa tahun terakhir, VAMI telah mengembangkan dan menguji teknologi untuk memproduksi aluminium dengan kemurnian 99,9999% di lingkungan industri menggunakan metode peleburan zona kaskade. Inti dari metode peleburan zona kaskade adalah pemurnian aluminium awal dengan kemurnian A999 dilakukan dengan siklus berulang (kaskade) strip zona secara berurutan. Dalam hal ini, bahan awal untuk setiap kaskade berikutnya adalah bagian tengah ingot paling murni yang diperoleh dari siklus pemurnian sebelumnya.
TABEL 1.4
| Ketidakmurnian | Aluminium mentah (dimurnikan secara elektrolitik 99.993-99.994%) | Aluminium setelah zona leleh | |
| grafit, vakum | alund, udara | ||
| Tembaga | 1,9 | 0,02 | 0,08 |
| Arsenik | 0,15 | 0,0015 | 0,001 |
| Antimon | 1,2 | 0,03 | 0,02 |
| Uranus | 0,002 | - | - |
| Besi | 3 | ≤0,2 | ≤0,3 |
| galium | 0,3 | 0,02 | 0,05 |
| mangan | 0,2-0,3 | 0,1-0,2 | 0,15 |
| Skandium | 0,4-0,5 | 0,4-0,5 | 0,4-0,5 |
| Itrium | 0,02-0,04 | <<0,001 | <<0,001 |
| Lutetium | 0,002-0,004 | <<0,0001 | <<0,0001 |
| Holmium | 0,005-0,01 | <<0,0001 | <<0,0001 |
| Gadolinium | 0,02-0,04 | <<0,01 | <<0,01 |
| Terbium | 0,003-0,006 | <<0,001 | <<0,001 |
| Samarium | 0,05-0,01 | <<0,0001 | <<0,0001 |
| Neodimium | 0,1-0,2 | <<0,01 | <<0,01 |
| Praseodymium | 0,05-0,1 | <<0,001 | <<0,001 |
| Cerium | 0,3-0,6 | <<0,01 | <<0,01 |
| Lantanum | 0,01 | <<0,001 | <<0,001 |
| Nikel | 2,3 | - | <1 |
| Kadmium | 3,5 | <<0,01 | 0,02-0,07 |
| Seng | 20 | <<0,05 | 1 |
| Kobalt | 0,01 | <<0,01 | <<0,01 |
| Sodium | 1-2 | <0,2 | <0,2 |
| Kalium | 0,05 | 0,01 | 0,01 |
| Barium | 6 | - | - |
| Klorin | 0,01 | <0,01 | <0,01 |
| Fosfor | 3 | 0,04 | - |
| Sulfur | 15 | 0,5-1,5 | - |
| Karbon | 1-2 | - | 1-2 |
| Catatan. Jumlah telurium, bismut, perak, molibdenum, kromium, zirkonium, kalsium, strontium, rubidium, serium, indium, selenium dan merkuri dalam aluminium setelah peleburan zona berada di bawah sensitivitas analisis radioaktif. | |||
Di meja 1.5 (lihat di bawah) menunjukkan hasil analisis dan pengukuran spektral massa R 293K / R Aluminium 4,2 K diproduksi melalui peleburan zona kaskade. Dari data yang disajikan, dapat disimpulkan bahwa kemurnian aluminium yang ditentukan oleh selisih sepuluh pengotor utama (Si, Fe, Mg, Mn, Ti, Cu, Cr, Zn, Na, dan V), adalah >99,9999%. . Kesimpulan ini secara tidak langsung dikonfirmasi oleh maknanya R 293K / R 4,2 K, yang pada semua sampel >30ּ10 3 .
Untuk memperoleh logam dengan kemurnian 99,9999%, cukup melakukan dua tahap peleburan zona (lihat Tabel 1.5). Peningkatan lebih lanjut dalam jumlah kaskade tidak meningkatkan kemurnian aluminium, meskipun hal ini meningkatkan hasil keseluruhan logam dengan kemurnian 99,9999%.
Proses lain yang mungkin untuk memperoleh aluminium dengan kemurnian tinggi adalah distilasi melalui subhalida, khususnya melalui aluminium subfluorida.
Tekanan uap jenuh logam aluminium tidak cukup tinggi untuk melakukan distilasi langsung pada tingkat yang dapat diterima. Namun, ketika dipanaskan dalam ruang hampa (pada 1000-1050°C) dengan AlF 3, aluminium membentuk subfluorida AlF yang sangat mudah menguap, yang disuling ke zona dingin (800°C), di mana aluminium kembali terurai (disproporsi) dengan pelepasan dari aluminium murni:
Kemungkinan pemurnian mendalam aluminium dari pengotor terutama disebabkan oleh fakta bahwa kemungkinan pembentukan subsenyawa aluminium jauh lebih besar daripada kemungkinan pembentukan subsenyawa pengotor.
TABEL 1.5
HASIL ANALISIS DAN PENGUKURAN SPEKRAL MASSA R 293K / R Peleburan ZONA CASCADE ALUMINIUM 4,2 K.
| Jumlah tahapan | Konten pengotor, ×10 –4% | ||||||
| Ya | Fe | mg | M N | Ti | jumlah | ||
| Asli | 18,3 | 0,210 | <0,103 | 0,89 | <0,061 | 0,069 | 1,544 |
| A999 | |||||||
| 2 | 36,5 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 38,0 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 39,5 | 0,073 | <0,103 | 0,045 | <0,061 | 0,07 | 0,563 |
| 3 | 32,0 | 0,204 | <0,103 | 0,006 | <0,061 | 0,017 | 0,502 |
| 3 | 30,0 | 0,073 | 0,100 | 0,006 | 0,020 | 0,07 | 0,480 |
| 3 | 32,0 | 0,052 | 0,100 | 0,006 | 0,061 | 0,07 | 0,500 |
| 4 | 40,0 | <0,021 | <0,103 | 0,006 | 0,061 | 0,07 | 0,472 |
| 4 | 30,5 | 0,031 | 0,100 | 0,006 | 0,061 | 0,07 | 0,479 |
| 5 | 34,0 | 0,104 | <0,060 | 0,006 | 0,061 | 0,017 | 0,459 |
| Catatan: 1. Jumlah pengotor diberikan dengan memperhitungkan pengotor lainnya, yang kandungannya dalam semua sampel adalah ×10 –4%:<0,071 Cu; <0,038 Cr; 0,048 Zn; 0,017 Na; 0,037 V. 2. При подсчете суммы примесей принимали их максимальное значение, равное пределу чувствительности анализа, например <0,061 считали как 0,061. | |||||||
Kandungan pengotor pada aluminium yang disuling melalui subfluorida berbanding terbalik dengan massa ingot yang dihasilkan. Dalam ingot seberat 1,5-1,7 kg, kandungan total pengotor (Si, Fe, Cu, Mg) adalah 11ּ10–4%, dan kandungan gas 0,007 cm 3 /100 g Resistansi sisa spesifik (ρ ○) pada helium cair suhu untuk logam tersebut adalah (1.7±2.0)ּ10 –10 Ohmּcm. Distilasi aluminium melalui subfluorida memiliki sejumlah kelemahan (produktivitas yang relatif rendah, pemurnian magnesium yang kurang mendalam, dll.), sehingga metode ini belum dikembangkan secara industri.
Metode juga telah dikembangkan untuk memproduksi aluminium dengan kemurnian tinggi melalui elektrolisis senyawa organoaluminium kompleks, yang berbeda dalam komposisi elektrolitnya. Misalnya, di Jerman mereka menggunakan metode elektrolisis larutan 50% NaFּ2Al (C 2 H 5) 3 dalam toluena. Pemurnian dilakukan pada suhu 100°C, tegangan elektroliser 1,0-1,5 V dan rapat arus 0,3-0,5 A/dm 2 menggunakan elektroda aluminium. Efisiensi arus katoda 99%. Pemurnian elektrokimia dalam elektrolit organoaluminum secara signifikan mengurangi kandungan mangan dan skandium, yang praktis tidak dihilangkan selama pemurnian zona. Kerugian dari metode ini adalah produktivitasnya yang rendah dan bahaya kebakaran yang tinggi.
Untuk pemurnian aluminium lebih dalam dan memperoleh logam dengan kemurnian 99,99999% atau lebih, Anda dapat menggunakan kombinasi metode di atas: elektrolisis senyawa organoaluminium atau sublimasi melalui subfluorida, diikuti dengan peleburan zona aluminium yang dihasilkan. Misalnya, dengan pemurnian zona aluminium berulang kali yang diperoleh melalui elektrolisis senyawa organoaluminum, dimungkinkan untuk memperoleh logam dengan kemurnian tinggi dengan kandungan pengotor ×10–9%: Fe 50; Ya<500; Cu 10; Mg 30; Mn5; Ti <500; Cr 20; Zn <50; Co <1; Ag <5; Sb <1 и Se 3.
Aplikasi
Kombinasi sifat fisik, mekanik dan kimia aluminium menentukan penggunaannya secara luas di hampir semua bidang teknologi, terutama dalam bentuk paduannya dengan logam lain. Dalam bidang teknik kelistrikan, aluminium berhasil menggantikan tembaga, terutama dalam produksi konduktor masif, misalnya pada saluran udara, kabel tegangan tinggi, busbar switchgear, trafo (konduktivitas listrik aluminium mencapai 65,5% dari konduktivitas listrik tembaga, dan itu lebih dari tiga kali lebih ringan dari tembaga; dengan penampang yang memberikan konduktivitas yang sama, massa kabel aluminium adalah setengah dari tembaga). Aluminium ultra murni digunakan dalam produksi kapasitor dan penyearah listrik, yang tindakannya didasarkan pada kemampuan film aluminium oksida untuk mengalirkan arus listrik hanya dalam satu arah. Aluminium ultra-murni, dimurnikan dengan peleburan zona, digunakan untuk sintesis senyawa semikonduktor tipe A III B V, digunakan untuk produksi perangkat semikonduktor. Aluminium murni digunakan dalam produksi berbagai jenis cermin reflektif. Aluminium dengan kemurnian tinggi digunakan untuk melindungi permukaan logam dari korosi atmosferik (pelapis, cat aluminium). Memiliki penampang serapan neutron yang relatif rendah, aluminium digunakan sebagai material struktural pada reaktor nuklir.
Tangki aluminium berkapasitas besar menyimpan dan mengangkut gas cair (metana, oksigen, hidrogen, dll.), asam nitrat dan asetat, air bersih, hidrogen peroksida, dan minyak nabati. Aluminium banyak digunakan pada peralatan dan perlengkapan industri makanan, untuk kemasan makanan (dalam bentuk foil), dan untuk produksi berbagai jenis produk rumah tangga. Konsumsi aluminium untuk finishing bangunan, arsitektur, transportasi dan struktur olahraga meningkat tajam.
Dalam metalurgi, aluminium (selain paduan berdasarkan itu) adalah salah satu bahan tambahan paduan yang paling umum dalam paduan berdasarkan Cu, Mg, Ti, Ni, Zn dan Fe. Aluminium juga digunakan untuk mendeoksidasi baja sebelum dituangkan ke dalam cetakan, serta dalam proses produksi logam tertentu menggunakan aluminotermi. Berbahan dasar aluminium, SAP (sintered aluminium powder) dibuat menggunakan metalurgi serbuk, yang memiliki ketahanan panas tinggi pada suhu di atas 300°C.
Aluminium digunakan dalam produksi bahan peledak (ammonal, alumotol). Berbagai senyawa aluminium banyak digunakan.
Produksi dan konsumsi aluminium terus meningkat, jauh melampaui laju pertumbuhan produksi baja, tembaga, timah, dan seng.
DIN (DeutschIndustrienorm) - standar industri Jerman.
Salah satu legenda yang sangat meragukan menceritakan bahwa suatu hari seorang pria mendatangi kaisar Romawi Tiberius (42 SM - 37 M) dengan membawa mangkuk logam yang tidak bisa pecah. Bahan mangkuk tersebut diduga berasal dari alumina (Al 2 O 3) dan oleh karena itu pastilah aluminium. Khawatir logam yang terbuat dari tanah liat tersebut akan mendevaluasi emas dan perak, Tiberius memerintahkan agar kepala pria itu dipenggal, untuk berjaga-jaga. Tentu saja, cerita ini sulit dipercaya: aluminium asli tidak terdapat di alam, dan pada zaman Kekaisaran Romawi tidak mungkin ada sarana teknis yang memungkinkan untuk mengekstraksi aluminium dari senyawanya.
Dalam hal prevalensinya di alam, aluminium menempati urutan pertama di antara logam; kandungannya di kerak bumi adalah 7,45%. Namun, meskipun tersebar luas di alam, aluminium merupakan salah satu logam langka hingga akhir abad ke-19. Aluminium tidak ditemukan dalam bentuk murni karena aktivitas kimianya yang tinggi. Hal ini terutama ditemukan dalam bentuk senyawa dengan oksigen dan silikon - aluminosilikat.
Hanya batuan yang kaya akan alumina (Al 2 O 3) dan terdapat dalam jumlah besar di permukaan bumi yang dapat dijadikan sebagai bijih aluminium. Batuan tersebut antara lain bauksit, nepheline - (Na, K) 2 OּAl 2 O 3 ּ2SiO 2, alunit - (Na, K) 2 SO 4 ּAl 2 (SO 4) 3 ּ4Al(OH) 3 dan kaolin (tanah liat), field spar (ortoklas) - K 2 OּAl 2 O 3 ּ6SiO 2 .
Bijih utama untuk memproduksi aluminium adalah bauksit. Bauksit mengandung aluminium dalam bentuk hidroksida Al(OH), AlOOH, korundum Al 2 O 3 dan kaolinit Al 2 O 3 ּ2SiO 2 ּ2H 2 O. Komposisi kimia bauksit sangat kompleks: 28-70% alumina; 0,5-20% silika; 2-50% besi oksida; 0,1-10% titanium oksida. Baru-baru ini, nepheline dan alunit telah digunakan sebagai bijih.
Deposit besar bauksit terletak di Ural, di distrik Tikhvin di wilayah Leningrad, di wilayah Altai dan Krasnoyarsk.
Nepheline (KּNa 2 OּAl 2 O 3 ּ2SiO 2) merupakan bagian dari batuan nepheline apatit (di Semenanjung Kola).
Aluminium pertama kali diisolasi dalam bentuk bebasnya pada tahun 1825 oleh fisikawan Denmark Oersted dengan mereaksikan amalgam kalium dengan aluminium klorida. Pada tahun 1827 Ahli kimia Jerman Wöhler menyempurnakan metode Oersted dengan mengganti amalgam kalium dengan kalium logam:
AlCl 3 + 3K→3KCl + Al (Reaksi berlangsung dengan pelepasan panas).
Pada tahun 1854, Saint-Clair Deville di Perancis pertama kali menggunakan metode Wöhler untuk produksi industri aluminium, menggunakan natrium yang lebih murah daripada kalium, dan sebagai pengganti aluminium klorida higroskopis, klorida ganda yang lebih stabil dari aluminium dan natrium. Pada tahun 1865, ahli kimia fisik Rusia N. N. Beketov menunjukkan kemungkinan menggantikan aluminium dengan magnesium dari kriolit cair. Reaksi ini digunakan pada tahun 1888 untuk memproduksi aluminium di pabrik Jerman pertama di Gmelingen. Produksi aluminium dengan apa yang disebut metode “kimia” ini dilakukan dari tahun 1854 hingga 1890. Selama 35 tahun, total sekitar 20 ton aluminium diproduksi dengan menggunakan metode ini.
Pada akhir tahun 80-an abad sebelumnya, metode kimia digantikan oleh metode elektrolitik, yang memungkinkan pengurangan tajam biaya aluminium dan menciptakan prasyarat bagi pesatnya perkembangan industri aluminium. Pendiri metode elektrolitik modern dalam produksi aluminium, Héroux di Prancis dan Hall di AS, secara independen mengajukan permohonan serupa pada tahun 1886 untuk mematenkan metode memproduksi aluminium dengan elektrolisis alumina yang dilarutkan dalam kriolit cair. Sejak munculnya paten Heroux dan Hall, industri aluminium modern dimulai, yang selama lebih dari 115 tahun keberadaannya telah berkembang menjadi salah satu cabang metalurgi terbesar.
Proses teknologi produksi aluminium terdiri dari tiga tahap utama:
1). Memperoleh alumina (Al 2 O 3) dari bijih aluminium;
2). Produksi aluminium dari alumina;
3). Pemurnian aluminium.
Memperoleh alumina dari bijih.
Alumina diproduksi dengan tiga cara: basa, asam dan elektrolitik. Yang paling luas adalah metode alkaline (metode K.I. Bayer, dikembangkan di Rusia pada akhir abad sebelumnya dan digunakan untuk memproses bauksit bermutu tinggi dengan sejumlah kecil (hingga 5-6%) silika). Sejak itu, implementasi teknisnya telah ditingkatkan secara signifikan. Diagram produksi alumina menggunakan metode Bayer ditunjukkan pada Gambar. 1.
Inti dari metode ini adalah larutan aluminium cepat terurai ketika aluminium hidroksida dimasukkan ke dalamnya, dan larutan sisa dekomposisi setelah penguapan dalam kondisi pengadukan intensif pada suhu 169-170 o C dapat kembali melarutkan alumina yang terkandung dalam bauksit. Metode ini terdiri dari operasi dasar berikut:
1). Persiapan bauksit, yang terdiri dari penghancuran dan penggilingan di pabrik; bauksit, alkali kaustik dan sedikit kapur disuplai ke pabrik, yang meningkatkan pelepasan Al 2 O 3; pulp yang dihasilkan diumpankan untuk pencucian;
2). Pencucian bauksit (saat ini, blok autoklaf berbentuk bulat yang masih digunakan telah sebagian digantikan oleh autoklaf berbentuk tabung, dimana pencucian terjadi pada suhu 230-250 ° C (500-520 K), yang terdiri dari dekomposisi kimianya dari interaksi dengan larutan alkali berair; Ketika bereaksi dengan alkali, aluminium oksida hidrat masuk ke dalam larutan dalam bentuk natrium aluminat:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH) 3 + NaOH → NaAlO 2 + 2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H 2 O;
dalam larutan, natrium aluminat dan natrium silikat membentuk natrium aluminosilikat yang tidak larut; oksida titanium dan besi masuk ke dalam residu yang tidak larut, memberikan warna merah pada residu; residu ini disebut lumpur merah. Setelah pelarutan selesai, natrium aluminat yang dihasilkan diencerkan dengan larutan alkali berair sekaligus menurunkan suhu sebesar 100°C;
3). Pemisahan larutan aluminat dari lumpur merah, biasanya dilakukan dengan cara dicuci dengan pengental khusus; Akibatnya lumpur merah mengendap, dan larutan aluminat ditiriskan lalu disaring (diklarifikasi). Dalam jumlah terbatas, lumpur digunakan, misalnya sebagai bahan tambahan semen. Tergantung pada jenis bauksit, 1 ton aluminium oksida yang dihasilkan menghasilkan 0,6-1,0 ton lumpur merah (residu kering);
4). Dekomposisi larutan aluminat. Itu disaring dan dipompa ke dalam wadah besar dengan agitator (pengurai). Aluminium hidroksida Al(OH) 3 diekstraksi dari larutan lewat jenuh setelah pendinginan hingga 60°C (330 K) dan pengadukan konstan. Karena proses ini berlangsung lambat dan tidak merata, dan pembentukan serta pertumbuhan kristal aluminium hidroksida sangat penting selama pemrosesan lebih lanjut, sejumlah besar hidroksida padat - sebutir - ditambahkan ke pengurai:
Na 2 OּAl 2 O 3 +4H 2 O→Al(OH) 3 +2NaOH;
5). Isolasi aluminium hidroksida dan klasifikasinya; hal ini terjadi pada hidrosiklon dan filter vakum, dimana endapan yang mengandung 50-60% partikel Al(OH) dipisahkan dari larutan aluminat. Sebagian besar hidroksida dikembalikan ke proses dekomposisi sebagai bahan benih, yang tetap beredar dalam jumlah yang tidak berubah. Residu setelah dicuci dengan air menuju kalsinasi; filtrat juga dikembalikan ke sirkulasi (setelah konsentrasi dalam evaporator - untuk pencucian bauksit baru);
6). Dehidrasi aluminium hidroksida (kalsinasi); Ini adalah langkah terakhir dalam produksi alumina; ini dilakukan dalam tanur putar berbentuk tabung, dan baru-baru ini juga dalam tanur dengan pergerakan material yang turbulen pada suhu 1150-1300 o C; aluminium hidroksida mentah, melewati tanur putar, dikeringkan dan didehidrasi; Ketika dipanaskan, transformasi struktural berikut terjadi secara berurutan:
| Al(OH) 3 →AlOOH→ γ-Al 2 O 3 → α-Al 2 O 3 |
|||
Akhirnya alumina yang dikalsinasi mengandung 30-50% α-Al 2 O 3 (korundum), sisanya γ-Al 2 O 3.
Metode ini mengekstraksi 85-87% dari total alumina yang dihasilkan. Aluminium oksida yang dihasilkan merupakan senyawa kimia kuat dengan titik leleh 2050 o C.
Pembuatan aluminium dari oksidanya
Elektrolisis aluminium oksida
 Reduksi elektrolitik aluminium oksida yang dilarutkan dalam lelehan berbasis kriolit dilakukan pada suhu 950-970°C dalam elektroliser. Elektroliser terdiri dari bak yang dilapisi dengan blok karbon, di bagian bawahnya disuplai arus listrik. Aluminium cair yang dilepaskan di tungku, yang berfungsi sebagai katoda, lebih berat daripada garam cair elektrolit, oleh karena itu aluminium dikumpulkan di dasar batubara, yang kemudian dipompa keluar secara berkala (Gbr. 2). Anoda karbon direndam dalam elektrolit di atasnya, yang terbakar dalam atmosfer oksigen yang dilepaskan dari aluminium oksida, melepaskan karbon monoksida (CO) atau karbon dioksida (CO2). Dalam prakteknya, dua jenis anoda digunakan:
Reduksi elektrolitik aluminium oksida yang dilarutkan dalam lelehan berbasis kriolit dilakukan pada suhu 950-970°C dalam elektroliser. Elektroliser terdiri dari bak yang dilapisi dengan blok karbon, di bagian bawahnya disuplai arus listrik. Aluminium cair yang dilepaskan di tungku, yang berfungsi sebagai katoda, lebih berat daripada garam cair elektrolit, oleh karena itu aluminium dikumpulkan di dasar batubara, yang kemudian dipompa keluar secara berkala (Gbr. 2). Anoda karbon direndam dalam elektrolit di atasnya, yang terbakar dalam atmosfer oksigen yang dilepaskan dari aluminium oksida, melepaskan karbon monoksida (CO) atau karbon dioksida (CO2). Dalam prakteknya, dua jenis anoda digunakan:
a) anoda Zederberg yang dapat terbakar sendiri, terdiri dari briket, yang disebut “roti” massa Zederberg (batubara abu rendah dengan kadar tar batubara 25-35%), dimasukkan ke dalam cangkang aluminium; di bawah pengaruh suhu tinggi, massa anoda dibakar (disinter);
b) anoda yang dipanggang atau “kontinu” yang terbuat dari balok karbon besar (misalnya, 1900x600x500 mm dengan berat sekitar 1,1 ton).
Kekuatan arus dalam elektroliser adalah 150.000 A. Mereka dihubungkan ke jaringan secara seri, yaitu, suatu sistem (seri) diperoleh - deretan elektroliser yang panjang.
Tegangan pengoperasian pada bak, 4-5 V, secara signifikan lebih tinggi daripada tegangan penguraian aluminium oksida, karena kehilangan tegangan di berbagai bagian sistem tidak dapat dihindari selama pengoperasian. Keseimbangan bahan baku dan energi pada produksi 1 ton aluminium disajikan pada Gambar. 3.
Elektrolisis aluminium klorida (metode Alcoa)
 Dalam bejana reaksi, aluminium oksida diubah terlebih dahulu menjadi aluminium klorida. Kemudian, dalam bak berinsulasi rapat, terjadi elektrolisis AlCl 3 yang dilarutkan dalam garam cair KCl dan NaCl. Klorin yang dilepaskan selama proses ini disedot dan disuplai untuk didaur ulang; aluminium diendapkan pada katoda.
Dalam bejana reaksi, aluminium oksida diubah terlebih dahulu menjadi aluminium klorida. Kemudian, dalam bak berinsulasi rapat, terjadi elektrolisis AlCl 3 yang dilarutkan dalam garam cair KCl dan NaCl. Klorin yang dilepaskan selama proses ini disedot dan disuplai untuk didaur ulang; aluminium diendapkan pada katoda.
Keuntungan metode ini dibandingkan elektrolisis lelehan kriolit-alumina cair (Al 2 O 3 yang dilarutkan dalam kriolit Na 3 AlF 6) adalah: menghemat energi hingga 30%; kemungkinan penggunaan aluminium oksida, yang tidak cocok untuk elektrolisis tradisional (misalnya, Al 2 O 3 dengan kandungan silikon tinggi); mengganti kriolit yang mahal dengan garam yang lebih murah; hilangnya bahaya pelepasan fluorida.
Reduksi aluminium klorida dengan mangan (metode Toth)
 Ketika direduksi dengan mangan, aluminium dilepaskan dari aluminium klorida. Melalui kondensasi terkendali, kontaminan terkait klorin dilepaskan dari aliran mangan klorida. Ketika klorin dilepaskan, mangan klorida dioksidasi menjadi oksida mangan, yang kemudian direduksi menjadi mangan, cocok untuk penggunaan sekunder. Informasi dalam publikasi yang ada sangat tidak akurat, sehingga dalam hal ini evaluasi metode tersebut perlu ditinggalkan.
Ketika direduksi dengan mangan, aluminium dilepaskan dari aluminium klorida. Melalui kondensasi terkendali, kontaminan terkait klorin dilepaskan dari aliran mangan klorida. Ketika klorin dilepaskan, mangan klorida dioksidasi menjadi oksida mangan, yang kemudian direduksi menjadi mangan, cocok untuk penggunaan sekunder. Informasi dalam publikasi yang ada sangat tidak akurat, sehingga dalam hal ini evaluasi metode tersebut perlu ditinggalkan.
Memperoleh aluminium olahan
Untuk aluminium, pemurnian elektrolisis dengan dekomposisi larutan garam berair tidak mungkin dilakukan. Karena untuk beberapa tujuan tingkat pemurnian aluminium industri (Al 99,5 - Al 99,8), yang diperoleh dengan elektrolisis lelehan kriolit-alumina, tidak mencukupi, bahkan aluminium yang lebih murni (Al 99, 99 R) diperoleh dari aluminium industri atau limbah logam dengan pengilangan. Metode pemurnian yang paling terkenal adalah elektrolisis tiga lapis.
Pemurnian dengan elektrolisis tiga lapis
Dilapisi dengan lembaran baja, beroperasi dengan arus searah (ditunjukkan pada Gambar 4 - lihat di atas), bak pemurnian terdiri dari perapian batubara dengan kabel arus dan lapisan magnesit insulasi panas. Berbeda dengan elektrolisis lelehan kriolit-alumina, anoda di sini biasanya adalah logam cair yang dimurnikan (lapisan anoda bawah). Elektrolitnya terdiri dari fluorida murni atau campuran barium klorida dan aluminium dan natrium fluorida (lapisan tengah). Aluminium, yang larut dari lapisan anoda ke dalam elektrolit, dilepaskan di atas elektrolit (lapisan katoda atas). Logam murni berfungsi sebagai katoda. Arus disuplai ke lapisan katoda oleh elektroda grafit.
Bak mandi beroperasi pada suhu 750-800°C, konsumsi listrik 20 kWh per 1 kg aluminium murni, yaitu sedikit lebih tinggi dibandingkan dengan elektrolisis aluminium konvensional.
Logam anoda mengandung 25-35% Cu; 7-12% Zn; 6-9% Si; Fe sampai 5% dan sedikit mangan, nikel, timbal dan timah, sisanya (40-55%) adalah aluminium. Semua logam berat dan silikon tetap berada di lapisan anoda selama pemurnian. Kehadiran magnesium dalam elektrolit menyebabkan perubahan komposisi elektrolit yang tidak diinginkan atau slagging yang parah. Untuk menghilangkan magnesium, terak yang mengandung magnesium diolah dengan fluks atau gas klor.
Hasil pemurnian menghasilkan aluminium murni (99,99%) dan produk segregasi (produk Ziger), yang mengandung logam berat dan silikon dan dilepaskan dalam bentuk larutan alkali dan residu kristal. Larutan basa adalah produk limbah, dan residu padat digunakan untuk deoksidasi.
Aluminium olahan biasanya memiliki komposisi sebagai berikut,%: Fe 0,0005-0,002; Si 0,002-0,005; Cu 0,0005-0,002; Zn 0,0005-0,002; jejak mg; Semua sisanya.
Aluminium olahan diolah menjadi produk setengah jadi dengan komposisi tertentu atau dicampur dengan magnesium (lihat Tabel 1.2.).
TABEL 1.2. Komposisi kimia aluminium kemurnian tinggi dan aluminium primer menurut DIN 17122, lembar 1.
| Pengotor yang diijinkan*, % | |||||||||
| termasuk |
|||||||||
| A199.99R | 3.0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 | |
| A199.9H | 3.0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 | |
| A199.8H | 3.0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199.7H | 3.0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199.5H** | 3.0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 | |
| A199H | 3.0200 | 1,0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 | |
| * Sebisa mungkin ditentukan dengan menggunakan metode penelitian konvensional. ** Aluminium murni untuk teknik kelistrikan (aluminium konduktor) disuplai dalam bentuk aluminium primer 99,5 yang mengandung tidak lebih dari 0,03% (Ti + Cr + V + Mn); dalam hal ini ditunjuk E-A1, nomor material 3.0256. Kalau tidak, itu sesuai dengan standar VDE-0202. |
|||||||||
Pemurnian dengan kompleks organoaluminium dan peleburan zona
Aluminium dengan tingkat kemurnian lebih tinggi dari kadar A1 99,99 R dapat diperoleh dengan pemurnian elektrolisis aluminium murni atau murni komersial menggunakan senyawa organoaluminum kompleks aluminium sebagai elektrolit. Elektrolisis terjadi pada suhu sekitar 1000°C antara elektroda aluminium padat dan pada prinsipnya mirip dengan pemurnian elektrolisis tembaga. Sifat elektrolit menentukan kebutuhan untuk bekerja tanpa akses udara dan pada kepadatan arus yang rendah.
Elektrolisis pemurnian jenis ini, awalnya hanya digunakan pada skala laboratorium, sudah dilakukan pada skala industri kecil - beberapa ton logam diproduksi per tahun. Derajat pemurnian nominal logam yang dihasilkan adalah 99,999-99,9999%. Aplikasi potensial untuk logam dengan kemurnian ini termasuk teknik kelistrikan kriogenik dan elektronik.
Dimungkinkan untuk menggunakan metode pemurnian yang dipertimbangkan dalam pelapisan listrik.
Kemurnian yang lebih tinggi lagi - secara nominal hingga A1 99,99999 - dapat diperoleh dengan peleburan zona logam berikutnya. Saat memproses aluminium dengan kemurnian tinggi menjadi produk setengah jadi, lembaran atau kawat, mengingat suhu rekristalisasi logam yang rendah, perlu dilakukan tindakan pencegahan khusus. Sifat penting dari logam olahan adalah konduktivitas listriknya yang tinggi dalam kisaran suhu kriogenik.
Produksi aluminium sekunder
Daur ulang bahan mentah sekunder dan limbah produksi menguntungkan secara ekonomi. Paduan sekunder yang dihasilkan memenuhi sekitar 25% dari total permintaan aluminium.
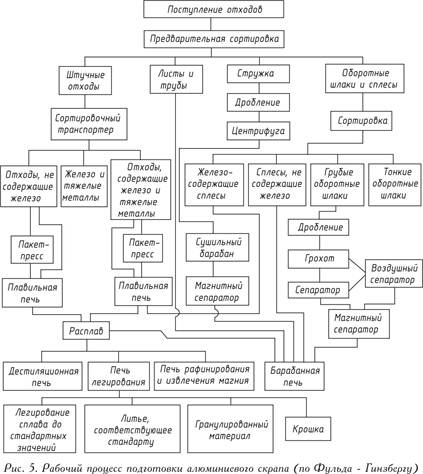 Area penerapan paduan sekunder yang paling penting adalah produksi coran berbentuk aluminium. Dalam DIN 1725, lembar 2, bersama dengan nilai paduan standar, banyak nilai paduan yang diproduksi oleh pengecoran logam terdaftar. Daftar paduan yang diproduksi oleh pabrik ini, selain paduan standar, juga mengandung beberapa paduan non-standar.
Area penerapan paduan sekunder yang paling penting adalah produksi coran berbentuk aluminium. Dalam DIN 1725, lembar 2, bersama dengan nilai paduan standar, banyak nilai paduan yang diproduksi oleh pengecoran logam terdaftar. Daftar paduan yang diproduksi oleh pabrik ini, selain paduan standar, juga mengandung beberapa paduan non-standar.
Persiapan skrap aluminium yang sempurna dalam berbagai proporsi hanya dapat dilakukan di pabrik peleburan yang dilengkapi peralatan khusus. Gagasan tentang proses kerja yang kompleks di pabrik tersebut diberikan pada Gambar. 5.
Sampah dicairkan setelah pemilahan awal yang kasar. Besi, nikel atau tembaga yang terkandung dalam limbah ini, yang titik lelehnya lebih tinggi dari titik leleh aluminium, bila dicairkan dalam tungku ambang batas, akan tetap berada di dalamnya, dan aluminium tersebut dilebur. Untuk menghilangkan inklusi non-logam seperti oksida, nitrida, karbida atau gas dari limbah, logam cair diolah dengan garam atau (lebih rasional) ditiup dengan gas - klorin atau nitrogen.
Berbagai metode diketahui untuk menghilangkan pengotor logam dari lelehan, misalnya penambahan magnesium dan penyedotan debu - metode Becksche; penambahan seng atau merkuri diikuti dengan evakuasi - metode subhalogen. Penghapusan magnesium dibatasi oleh masuknya klorin ke dalam logam cair. Dengan memasukkan aditif yang ditentukan secara tepat oleh komposisi lelehan, diperoleh paduan tuang tertentu.
Produksi aluminium kemurnian teknis
Metode elektrolitik adalah satu-satunya metode yang digunakan di seluruh dunia untuk produksi logam aluminium dengan kemurnian teknis. Semua metode lain (zincothermic, karbidotermal, subklorida, nitrida, dll.) yang dengannya aluminium dapat diekstraksi dari bijih aluminium telah dikembangkan pada skala laboratorium dan industri percontohan, tetapi belum menemukan penerapan praktisnya.
Untuk memproduksi paduan aluminium-silikon, metode elektrotermal, yang pertama kali dikembangkan dan diterapkan pada skala industri di Uni Soviet, berhasil digunakan. Ini terdiri dari dua tahap: pada tahap pertama, paduan aluminium-silikon primer yang mengandung 60-63% Al diperoleh dengan reduksi langsung bijih aluminium-silikon dalam tungku listrik bijih-termal; pada tahap kedua, paduan primer diencerkan dengan aluminium teknis, menghasilkan silumin dan paduan aluminium-silikon cor dan tempa lainnya. Penelitian sedang dilakukan untuk mengekstraksi aluminium dengan kemurnian teknis dari paduan primer.
Secara umum produksi aluminium dengan metode elektrolitik meliputi produksi alumina (aluminium oksida) dari bijih aluminium, produksi garam fluorida (kriolit, aluminium fluorida dan natrium fluorida), produksi massa anoda karbon, pembakaran anoda karbon dan blok katoda dan bahan pelapis lainnya, serta produksi aluminium elektrolitik yang sebenarnya, yang merupakan tahap akhir dari metalurgi aluminium modern.
Karakteristik untuk produksi alumina, garam fluorida dan produk karbon adalah persyaratan untuk tingkat kemurnian maksimum bahan-bahan ini, karena lelehan kriolit-alumina yang mengalami elektrolisis tidak boleh mengandung pengotor unsur yang lebih elektropositif daripada aluminium, yang dilepaskan di katoda dalam pertama, akan mencemari logam.
Pada alumina kadar G-00, G-0 dan G-1, yang terutama digunakan dalam elektrolisis, kandungan SiO 2 adalah 0,02-0,05%, dan Fe 2 O 3 - 0,03-0,05%. Kriolit rata-rata mengandung 0,36-0,38% SiO 2 dan 0,05-0,06% Fe 2 O 3, aluminium fluorida mengandung 0,30-0,35% (SiO 2 + Fe 2 O 3). Massa anoda mengandung tidak lebih dari 0,25% SiO 2 dan 0,20% Fe 2 O 3.
Bijih aluminium terpenting yang menghasilkan alumina adalah bauksit. Dalam bauksit, aluminium hadir dalam bentuk aluminium hidroksida. Di Uni Soviet, selain bauksit, batuan nepheline digunakan untuk memproduksi alumina - natrium dan kalium aluminosilikat, serta batuan alunit, di mana aluminium ditemukan dalam bentuk sulfatnya. Bahan mentah untuk produksi massa anoda dan blok anoda yang dipanggang adalah bahan karbon murni - minyak bumi atau pitch coke dan tar batubara sebagai pengikat, dan untuk produksi kriolit dan garam fluorida lainnya - kalsium fluorida (fluorspar).
Selama produksi elektrolitik aluminium, alumina Al 2 O 3, yang dilarutkan dalam kriolit cair Na 3 AlF 6, terurai secara elektrokimia dengan pelepasan kation aluminium di katoda (aluminium cair), dan ion yang mengandung oksigen (ion oksigen) di karbon. anoda.
Menurut konsep modern, kriolit dalam keadaan cair terdisosiasi menjadi ion dan: , dan alumina terdisosiasi menjadi ion kompleks dan: ![]() , yang berada dalam kesetimbangan dengan ion sederhana:
, yang berada dalam kesetimbangan dengan ion sederhana: ![]() ,
, ![]() .
.
Proses utama yang terjadi di katoda adalah reduksi ion aluminium trivalen: Al 3+ + 3e → Al (I).
Seiring dengan proses utama, pelepasan ion aluminium trivalen yang tidak lengkap dimungkinkan dengan pembentukan ion monovalen: Al 3+ + 2e → Al + (II) dan, terakhir, pelepasan ion monovalen dengan pelepasan logam: Al + + e → Al (III).
Dalam kondisi tertentu (konsentrasi ion Na+ yang relatif tinggi, suhu tinggi, dll), pelepasan ion natrium dapat terjadi dengan pelepasan logam: Na++e → Na(IV). Reaksi (II) dan (IV) menyebabkan penurunan arus keluaran aluminium.
Pelepasan ion oksigen terjadi pada anoda karbon: 2O 2– – 4e → O 2. Namun, oksigen tidak dilepaskan dalam bentuk bebas, karena oksigen mengoksidasi karbon anoda untuk membentuk campuran CO 2 dan CO.
Reaksi keseluruhan yang terjadi dalam elektroliser dapat direpresentasikan dengan persamaan Al 2 O 3 + xC ↔ 2Al + (2x–3)CO + (3–x)CO 2 .
Komposisi elektrolit elektroliser aluminium industri, selain komponen utama - kriolit, aluminium fluorida dan alumina, termasuk sejumlah kecil (total hingga 8-9%) beberapa garam lainnya - CaF 2, MgF 2, NaCl dan LiF (aditif), yang meningkatkan beberapa sifat fisik dan kimia elektrolit dan dengan demikian meningkatkan efisiensi elektroliser. Kandungan alumina maksimum dalam elektrolit biasanya 6-8%, menurun selama proses elektrolisis. Ketika elektrolit kehabisan alumina, sebagian alumina lainnya dimasukkan ke dalamnya. Untuk pengoperasian normal elektroliser aluminium, rasio NaF:AlF 3 dalam elektrolit dipertahankan dalam kisaran 2,7-2,8 dengan menambahkan porsi kriolit dan aluminium fluorida.
Dalam produksi aluminium, elektroliser dengan anoda karbon yang dipanggang sendiri dan suplai arus samping atau atas digunakan, serta elektroliser dengan anoda karbon yang dipanggang sebelumnya. Desain elektroliser yang paling menjanjikan dengan anoda panggang, yang memungkinkan untuk meningkatkan daya unit, mengurangi konsumsi spesifik listrik arus searah untuk elektrolisis, memperoleh logam yang lebih murni, meningkatkan kondisi kerja sanitasi dan higienis, serta mengurangi emisi zat berbahaya. ke atmosfer.
Parameter teknis utama dan indikator kinerja elektroliser aluminium dari berbagai jenis diberikan dalam tabel. 1.3.
TABEL 1.3
PARAMETER TEKNIS UTAMA DAN INDIKATOR KINERJA ELEKTROLISER ALUMINIUM
| Parameter dan indikator | Dengan anoda yang dapat menyala sendiri | Dengan anoda panggang |
|
| pasokan saat ini | pasokan arus atas |
||
| Kekuatan saat ini, kA | 60-120 | 60-155 | 160-255 |
| Produktivitas harian elektroliser, t | 0,42-0,85 | 0,40-1,10 | 1,10-1,74 |
| Kerapatan arus anodik, A/cm 2 | 0,80-0,90 | 0,65-0,70 | 0,70-0,89 |
| Tegangan rata-rata pada elektroliser, V | 4,45-4,65 | 4,50-4,70 | 4,30-4,50 |
| Keluaran saat ini, % | 85-88 | 84-86 | 85-89 |
| Koefisien konsumsi per 1 ton aluminium: | |||
| Listrik DC, kWh | 15100-16200 | 15500-17300 | 14500-15500 |
| alumina, kg | 1920-1940 | 1920-1940 | 1920-1940 |
| massa anoda, kg | 520-560 | 560-620 | - |
| anoda panggang, kg | - | - | 540-600 |
| Garam fluorida dalam satuan fluor, kg | 20-30 | 25-35 | 15-25 |
Aluminium primer yang diekstraksi dari elektroliser (aluminium mentah) mengandung sejumlah pengotor, yang dapat dibagi menjadi tiga kelompok: non-logam (garam fluorida, α- dan γ-alumina, aluminium karbida dan nitrida, partikel karbon yang terperangkap secara mekanis saat menuangkan logam dari elektroliser); logam (besi, silikon), yang berasal dari bahan mentah, bahan batubara dan elemen struktur elektroliser; berbentuk gas - terutama hidrogen, yang terbentuk dalam logam sebagai hasil dekomposisi elektrolitik air yang memasuki elektrolit dengan bahan mentah.
Dari pengotor logam, selain besi dan silikon, kandungan galium, seng, titanium, mangan, natrium, vanadium, kromium, dan tembaga paling banyak. Kandungan pengotor mikro logam ini dan beberapa pengotor mikro lainnya dalam aluminium elektrolitik diberikan di bawah ini, %:
| Konten rata-rata | 0,0025 | 0,003 | 0,0025 | 0,004 | 0,002 | 0,007 |
| Batasan perubahan | 0,001-0,008 | 0,001-0,006 | 0,001-0,008 | 0,002-0,008 | 0,001-0,008 | 0,002-0,014 |
| Konten rata-rata | <0,002 | 0,0002 | 0,001 | 0,0005 | 0,008 | 0,004 |
| Batasan perubahan | <0,001-0,004 | 0,0001-0,0003 | 0,001-0,0024 | 0,0001-0,0009 | 0,004-0,012 | 0,002-0,008 |
Sumber utama pengotor mikro logam dalam aluminium adalah alumina, yang tergantung pada jenis bahan bakunya, mungkin mengandung galium, seng, kalium, fosfor, belerang, vanadium, titanium, dan kromium. Bahan berkarbon (massa anoda, anoda panggang, produk katoda) berfungsi sebagai sumber pengotor mikro seperti vanadium, titanium, mangan, seng.
Dengan elektrolisis lelehan kriolit-alumina, asalkan bahan awal murni digunakan (terutama bahan alumina dan karbon), dimungkinkan untuk memperoleh aluminium mentah dengan kadar A85 dan A8 (99,85 dan 99,80%). Bagian terbesar logam dari kadar ini (60-70% dari total output) diproduksi dalam elektroliser dengan anoda panggang, serta dalam elektroliser dengan suplai arus lateral (hingga 70% dari total produksi). Dalam elektroliser dengan anoda yang dapat dipanggang sendiri dan suplai arus atas, keluaran aluminium mentah kelas A8 rendah (1-3%), dan logam kelas A85 tidak dapat diperoleh karena pengotor besi yang signifikan memasuki aluminium dari sumber bahan non-mentah. (pin anoda, bagian pengumpul gas besi cor, alat teknologi, unit katoda).
Aluminium primer cair, diekstraksi dari elektroliser menggunakan sendok vakum, memasuki departemen pengecoran untuk pemurnian guna menghilangkan kotoran non-logam dan gas dan diproses lebih lanjut menjadi produk komersial (babi, batangan berbentuk silinder dan datar, batang kawat, dll.). Sebelum pengecoran, aluminium mentah disimpan dalam keadaan cair di tungku tahan listrik (mixer) atau di tungku gema gas. Dalam tungku ini, mereka tidak hanya secara rasional mencampurkan sebagian aluminium cair dari berbagai komposisi, tetapi juga membersihkan sebagian dari inklusi non-logam, lapisan oksida, dan natrium.
Aluminium dicetak dari mixer menjadi ingot menggunakan mesin pengecoran tipe konveyor; ingot silinder dan datar diproduksi dengan pengecoran semi kontinyu, dan unit khusus dari gabungan pengecoran dan penggulungan digunakan untuk memproduksi batang kawat.
Di pabrik peleburan aluminium dalam negeri, saat menuang ingot, aluminium yang berasal dari mixer ke dalam kristalisasi mesin pengecoran mengalami jenis pemurnian yang paling sederhana - menyaring lelehan melalui jaring fiberglass dengan ukuran sel mulai dari 0,6 × 0,6 hingga 1,7 × 1,7 mm. Metode ini memungkinkan Anda membersihkan aluminium hanya dari inklusi oksida yang sangat kasar; metode yang lebih maju adalah dengan menyaring lelehan melalui jaring fiberglass dalam aliran ke atas. Dengan metode penyaringan ini, partikel inklusi oksida, yang bertabrakan dengan jaring, tidak ditangkap oleh aliran lelehan, tetapi disimpan di bagian bawah parit pengecoran.
Untuk memurnikan aluminium secara bersamaan dari pengotor non-logam dan hidrogen, metode filtrasi melalui filter fluks yang dikombinasikan dengan pembersihan nitrogen berhasil digunakan. Elektrolit asam dari elektroliser aluminium dapat digunakan sebagai fluks. Sebagai hasil pemurnian tersebut, kandungan hidrogen dalam aluminium berkurang dari 0,22 menjadi 0,16 cm 3 per 100 g logam.
Dalam aluminium primer yang digunakan untuk produksi paduan sistem Al-Mg, kandungan natrium tidak boleh melebihi 0,001%. Hal ini disebabkan adanya natrium pada paduan tersebut memperburuk sifat mekanik dan sifat kinerja lainnya dari produk yang digunakan di sejumlah sektor perekonomian nasional.
Metode paling efektif untuk memurnikan aluminium secara bersamaan dari natrium, hidrogen, dan pengotor non-logam adalah dengan meniup logam cair dengan campuran gas nitrogen dan 2-10% klorin, dimasukkan ke dalam lelehan dalam bentuk gelembung kecil menggunakan perangkat khusus. . Metode pemurnian ini memungkinkan penurunan kandungan natrium dalam aluminium menjadi 0,0003-0,001% pada konsumsi campuran gas 0,8 hingga 1,5 m 3 /t logam.
Konsumsi listrik untuk produksi 1 ton aluminium komersial dari logam mentah dengan menggunakan tungku listrik adalah 150-200 kWh; kerugian logam yang tidak dapat diperbaiki pada tahap pengecoran adalah 1,5-5%, tergantung pada jenis produk komersial.
Memproduksi aluminium dengan kemurnian tinggi
Untuk mendapatkan aluminium dengan kemurnian tinggi (nilai A995-A95), aluminium primer dengan kemurnian teknis dimurnikan secara elektrolitik. Hal ini memungkinkan untuk mengurangi kandungan pengotor logam dan gas dalam aluminium dan dengan demikian secara signifikan meningkatkan konduktivitas listrik, keuletan, reflektifitas, dan ketahanan terhadap korosi.
Pemurnian aluminium secara elektrolitik dilakukan dengan elektrolisis garam cair menggunakan metode tiga lapis. Inti dari metode ini adalah sebagai berikut. Ada tiga lapisan cair dalam elektroliser pemurnian. Yang lebih rendah, yang terberat, terletak di bagian bawah konduktif dan berfungsi sebagai anoda; itu disebut paduan anoda dan merupakan paduan aluminium halus dengan tembaga, yang ditambahkan untuk membuat lapisan lebih berat. Lapisan tengah adalah cairan elektrolit; kerapatannya lebih kecil dari kerapatan paduan anoda dan lebih tinggi dari kerapatan aluminium murni (katoda) yang terletak di atas elektrolit (lapisan cair ketiga atas).
Selama pelarutan anodik, semua pengotor yang lebih elektropositif daripada aluminium (Fe, Si, Ti, Cu, dll.) tetap berada dalam paduan anodik tanpa masuk ke dalam elektrolit. Hanya aluminium yang larut secara anodik, yang berupa ion Al 3+ masuk ke dalam elektrolit: Al– 3e → Al 3+.
Selama elektrolisis, ion aluminium ditransfer ke katoda, di mana ion tersebut dilepaskan: Al 3+ + 3e → Al. Akibatnya, lapisan aluminium halus yang meleleh terakumulasi di katoda.
Jika paduan anoda mengandung pengotor yang lebih elektronegatif daripada aluminium (misalnya Ba, Na, Mg, Ca), maka pengotor tersebut dapat larut secara elektrokimia di anoda bersama dengan aluminium dan masuk ke elektrolit dalam bentuk ion. Karena kandungan pengotor elektronegatif dalam aluminium mentah rendah, pengotor tersebut tidak terakumulasi dalam jumlah yang signifikan di dalam elektrolit. Praktis tidak ada pelepasan ion-ion ini di katoda, karena potensial elektrodanya lebih elektronegatif daripada aluminium.
Elektrolit yang digunakan dalam pemurnian elektrolitik aluminium di Uni Soviet dan di sebagian besar negara adalah elektrolit fluorida-klorida, yang komposisinya adalah 55-60% BaCl 2, 35-40% AlF 4 + NaF dan 0-4% NaCl . Rasio molar NaF: AlF 3 dipertahankan pada 1,5-2,0; titik leleh elektrolit 720-730°C; suhu proses elektrolisis sekitar 800°C; kerapatan elektrolit 2,7 g/cm3.
Paduan anoda dibuat dari aluminium primer dan tembaga murni (99,90-99,95% Cu), yang dimasukkan ke dalam logam dalam jumlah 30-40%. Massa jenis paduan anoda cair komposisi ini adalah 3-3,5 g/cm 3 ; massa jenis aluminium katoda cair murni adalah 2,3 g/cm 3 . Dengan rasio kepadatan ini, kondisi yang diperlukan untuk pemisahan yang baik dari tiga lapisan cair tercipta.
Dalam sistem kuaterner Al-Cu-Fe-Si, yang mencakup paduan anoda, terbentuk eutektik dengan titik leleh 520°C. Dengan mendinginkan paduan anodik yang mengandung pengotor besi dan silikon dalam jumlah di atas konsentrasi eutektik, besi dan silikon dapat dilepaskan ke dalam fase padat dalam bentuk senyawa intermetalik FeSiAl 5 dan Cu 2 FeAl 7 . Karena suhu paduan anoda di kantong elektroliser adalah 30-40°C lebih rendah dari suhu paduan anoda di ruang kerja bak, endapan intermetalik padat akan dilepaskan di dalamnya (karena besi dan silikon terakumulasi di dalamnya). paduan anoda). Dengan menghilangkan endapan ini secara berkala, paduan anoda dibersihkan (tanpa memperbaruinya) dari kotoran besi dan silikon. Karena galium terkonsentrasi pada paduan anoda, sedimen yang diekstraksi dari elektroliser (30-40 kg per 1 ton aluminium) dapat berfungsi sebagai sumber logam ini.
Untuk pemurnian elektrolitik, digunakan elektroliser, yang dalam desainnya menyerupai elektroliser dengan anoda panggang untuk produksi elektrolitik aluminium primer, tetapi memiliki sambungan kutub yang berbeda: perapian berfungsi sebagai anoda, dan baris atas elektroda berfungsi sebagai katoda. Elektroliser modern untuk pemurnian aluminium secara elektrolitik dirancang untuk kekuatan arus hingga 75 kA.
Di bawah ini adalah indikator teknis dan ekonomi utama elektroliser pada tahun 1979, yang dicapai oleh perusahaan dalam negeri (1, 2, 3).
Efisiensi arus elektrokimia yang dihitung dari logam yang dituangkan dari elektroliser adalah 97-98%. Efisiensi arus aktual, dihitung berdasarkan jumlah logam komersial, adalah 92-96%.
| Kekuatan saat ini, kA | 23,5 | 62,9 | 69,8* |
| Tegangan rata-rata, V | 5,43 | 5,68 | 5,69 |
| Keluaran saat ini, % | 95,7 | 93,0 | 92,7 |
| Konsumsi listrik DC, kWh/t | 17 370 | 18 700 | 19 830 |
| Total listrik AC, kWh/t | 18 670 | 19 590 | 20 780 |
| Tingkat, cm | |||
| katoda aluminium | 16,6 | 12,9 | 14,6 |
| elektrolit | 13,3 | 11,6 | 14,2 |
| paduan anoda | 40,1 | 29,5 | 30,0 |
| Koefisien konsumsi, kg/t: |
|||
| barium klorida | 40,5 | 41,5 | 27,0 |
| 27,7 | 21,0 | 16,5 | |
| aluminium fluorida | 6,7 | 13,1 | 3,8 |
| natrium klorida | 1,0 | 4,8 | - |
| aluminium mentah | 1020 | 1028 | 1032 |
| 11,9 | 11,5 | 16,6 | |
| 9,8 | 15,5 | 16,4 | |
| Produksi aluminium dengan kemurnian tinggi, % nilai: |
|||
| 47,8** | 3,5 | 2,1 | |
| 30,4 | 67,1 | 54,2 | |
| 8,3 | 21,5 | 43,7 | |
| 10,4 | 7,9 | - | |
| 3,1 | - | - | |
| * Indikator produksi aluminium dengan kemurnian tinggi. ** Nilai menurut elektroliser tanpa dekomposisi. |
|||
Faktor utama yang mengurangi efisiensi arus, selain rugi-rugi arus searah akibat pelepasan ion yang lebih elektronegatif, rugi-rugi logam akibat oksidasi dan rugi-rugi mekanis aluminium, adalah pengoperasian elektroliser dengan pelepasan logam bermutu rendah, yang dikembalikan ke paduan anoda untuk pemurnian selanjutnya. Periode pengoperasian elektroliser ini terjadi selama pengaktifan elektroliser dan pelanggaran rezim teknologi.
Pemurnian aluminium secara elektrolitik adalah proses yang sangat intensif energi. Konsumsi listrik pada arus bolak-balik, termasuk energi yang dikeluarkan untuk pembuatan elektrolit dan paduan anoda, pengoperasian alat ventilasi dan kendaraan, serta rugi-rugi untuk mengubah arus bolak-balik menjadi arus searah, adalah 18,5-21,0 ribu kWh per 1 ton listrik. aluminium. Efisiensi energi elektroliser pemurnian tidak melebihi 5-7%, yaitu 93-95% energi dikonsumsi dalam bentuk kehilangan panas, yang dilepaskan terutama di lapisan elektrolit (sekitar 80-85% dari total masukan panas). Oleh karena itu, cara utama untuk lebih mengurangi konsumsi energi spesifik untuk pemurnian aluminium secara elektrolitik adalah dengan meningkatkan isolasi termal elektroliser (terutama bagian atas struktur) dan mengurangi lapisan elektrolit (mengurangi jarak antarelektroda).
Kemurnian aluminium yang dimurnikan dengan metode tiga lapis adalah 99,995%; itu ditentukan oleh perbedaannya dengan lima pengotor utama - besi, silikon, tembaga, seng dan titanium. Jumlah logam dengan kadar ini yang diperoleh bisa mencapai 45-48% dari total output (tanpa terurai dengan kadar yang lebih rendah).
Namun perlu dicatat bahwa aluminium yang dimurnikan secara elektrolitik mengandung pengotor logam lain dalam jumlah yang lebih kecil, sehingga mengurangi kemurnian absolut aluminium tersebut. Analisis radioaktivasi memungkinkan untuk mendeteksi hingga 30 pengotor dalam aluminium yang dimurnikan secara elektrolitik, yang kandungan totalnya kira-kira 60ּ10–4%. Oleh karena itu, kemurnian aluminium olahan dibandingkan dengan pengotor tersebut adalah 99,994%.
Selain pengotor yang ditentukan oleh GOST (lihat Tabel 1.1), kelas paling umum (A99) dari aluminium yang dimurnikan secara elektrolitik mengandung, %: Cr 0,00016; V 0,0001; Ga 0,0006; Pb 0,002; Sn 0,00005; Ca 0,002-0,003; Tidak 0,001-0,008; Mn 0,001-0,007; Mg 0,001-0,007; Sebagai<0,0001; Sb<0,00002; Bi<0,00001; Cd<0,000001; S 0,0007.
Salah satu sumber pencemaran aluminium katoda adalah timah arus grafit, yang mengandung besi dan silikon oksida dan selalu bersentuhan dengan aluminium olahan. Jika arus disuplai langsung ke katoda aluminium melalui batangan aluminium dan alat yang terbuat dari grafit sangat murni digunakan, logam dengan kemurnian 99,999% dapat diperoleh melalui perbedaan pengotor yang terdeteksi (Fe, Si, Cu, Zn). dan Ti). Logam ini rata-rata mengandung %: Si 0,0002; Fe 0,00032; Cu 0,0002; Zn 0,0002 dan Ti 0,00005. Namun karena kesulitan teknis, metode penyediaan arus ini belum diterapkan secara luas di industri.
Produksi aluminium dengan kemurnian tinggi
Aluminium dengan kemurnian tinggi (grade A999) dapat diproduksi dengan tiga cara: peleburan zona, distilasi melalui subhalida, dan elektrolisis senyawa aluminium-organik. Dari metode yang terdaftar untuk memproduksi aluminium dengan kemurnian tinggi, metode peleburan zona menerima penerapan praktis di Uni Soviet.
Prinsip peleburan zona adalah melewatkan zona cair berulang kali di sepanjang batangan aluminium. Berdasarkan koefisien distribusi K = C padat / C cair (di mana C padat adalah konsentrasi pengotor dalam padatan dan C cair - dalam fase cair), yang sangat menentukan efisiensi pemurnian dari pengotor, pengotor ini dapat dibagi menjadi tiga kelompok. Kelompok pertama meliputi pengotor yang menurunkan titik leleh aluminium; mereka punya K<1, при зонной плавке концентрируются в расплавленной зоне и переносятся ею к конечной части слитка. К числу этих примесей принадлежат Ga, Sn, Be, Sb, Ca, Th, Fe, Co, Ni, Ce, Te, Ba, Pt, Au, Bi, Pb, Cd, In, Na, Mg, Cu, Si, Ge, Zn. Ко второй группе принадлежат примеси, повышающие температуру плавления алюминия; они характеризуются К>1 dan selama peleburan zona, mereka terkonsentrasi di bagian padat (awal) ingot. Pengotor tersebut antara lain Nb, Ta, Cr, Ti, Mo, V. Golongan ketiga meliputi pengotor yang koefisien distribusinya sangat mendekati satu (Mn, Sc). Kotoran ini praktis tidak dihilangkan selama peleburan zona aluminium.
Aluminium yang dimaksudkan untuk peleburan zona harus melalui beberapa persiapan, yang terdiri dari filtrasi, degassing, dan pengawetan. Filtrasi diperlukan untuk menghilangkan lapisan oksida tahan api dan tahan lama dari aluminium yang tersebar di logam. Aluminium oksida yang ada dalam aluminium cair dapat menciptakan pusat kristalisasi selama pemadatannya, yang mengarah pada produksi ingot polikristalin dan terganggunya efek redistribusi pengotor antara logam padat dan zona cair. Aluminium disaring dalam ruang hampa (tekanan sisa 0,1-0,4 Pa) melalui lubang di dasar wadah grafit dengan diameter 1,5-2 mm. Degassing awal aluminium sebelum peleburan zona (juga pemanasan dalam ruang hampa) dilakukan untuk mencegah percikan logam ketika zona dicairkan jika proses dilakukan dalam ruang hampa tinggi. Tahap terakhir dalam mempersiapkan aluminium untuk peleburan zona adalah mengetsa permukaannya dengan campuran asam klorida pekat dan asam nitrat.
Karena aluminium memiliki aktivitas kimia yang signifikan dan terutama grafit murni digunakan sebagai bahan utama wadah (perahu), peleburan zona aluminium dilakukan dalam ruang hampa atau dalam atmosfer gas inert (argon, helium).
Peleburan zona dalam ruang hampa memastikan kemurnian aluminium yang lebih besar karena penguapan beberapa pengotor selama evakuasi (logam magnesium, seng, kadmium, alkali dan alkali tanah), dan juga menghilangkan kontaminasi logam yang dimurnikan dengan pengotor akibat penggunaan aluminium. gas inert pelindung. Peleburan zona aluminium dalam ruang hampa dapat dilakukan dengan pemompaan terus menerus dari tabung kuarsa, di mana perahu grafit dengan ingot aluminium ditempatkan, serta dalam ampul kuarsa tertutup, dari mana udara pertama kali dipompa keluar hingga tekanan sisa. sekitar 1ּ10 –3 Pa.
Untuk membuat zona cair pada ingot aluminium selama peleburan zona, pemanasan dapat diterapkan menggunakan tungku resistansi kecil atau arus frekuensi tinggi. Menghidupkan tungku tahan listrik tidak memerlukan peralatan yang rumit; tungku mudah dioperasikan. Satu-satunya kelemahan dari metode pemanasan ini adalah kecilnya penampang batang aluminium yang sedang dimurnikan.
Pemanasan induksi dengan arus frekuensi tinggi adalah cara ideal untuk membuat zona cair pada ingot selama peleburan zona. Metode pemanasan frekuensi tinggi (selain memungkinkan peleburan zona ingot dengan penampang besar) memiliki keuntungan penting karena logam cair terus tercampur di zona tersebut; ini memfasilitasi difusi atom pengotor dari bagian depan kristalisasi ke kedalaman lelehan.
Untuk pertama kalinya, produksi industri aluminium dengan kemurnian tinggi melalui peleburan zona dikuasai di pabrik peleburan aluminium Volkhov pada tahun 1965 menggunakan instalasi UZPI-3 yang dikembangkan oleh VAMI. Instalasi ini dilengkapi dengan empat retort kuarsa dengan pemanas induksi, sedangkan induktor dapat dipindahkan dan wadah logam tidak bergerak. Produktivitasnya adalah 20 kg logam per siklus pembersihan. Selanjutnya, instalasi semua logam berperforma lebih tinggi UZPI-4 dibuat dan dioperasikan secara komersial pada tahun 1972 di Pabrik Peleburan Aluminium Volkhov.
Efisiensi pemurnian aluminium selama peleburan zona dapat dicirikan oleh data berikut. Jika kandungan total pengotor dalam aluminium yang dimurnikan secara elektrolitik adalah (30±60)ּ10–4%, maka setelah zona peleburan berkurang menjadi (2,8±3,2)ּ10–4%, yaitu 15-20 kali lipat. Hal ini sesuai dengan hambatan listrik sisa aluminium ρ ○ (pada suhu helium cair 4,2 K), masing-masing (20±40)ּ10 –10 dan (1,8±2.1)ּ10 –10 atau kemurnian 99.997-99.994 dan 99.9997% . Di meja 1.4 (lihat di bawah) menunjukkan data analisis radioaktivasi tentang kandungan pengotor tertentu dalam aluminium yang dimurnikan secara zona dan dimurnikan secara elektrolitik. Data ini menunjukkan penurunan yang kuat dalam kandungan sebagian besar pengotor, meskipun pengotor seperti mangan dan skandium praktis tidak dihilangkan selama peleburan zona.
Dalam beberapa tahun terakhir, VAMI telah mengembangkan dan menguji teknologi untuk memproduksi aluminium dengan kemurnian 99,9999% di lingkungan industri menggunakan metode peleburan zona kaskade. Inti dari metode peleburan zona kaskade adalah pemurnian aluminium awal dengan kemurnian A999 dilakukan dengan siklus berulang (kaskade) strip zona secara berurutan. Dalam hal ini, bahan awal untuk setiap kaskade berikutnya adalah bagian tengah ingot paling murni yang diperoleh dari siklus pemurnian sebelumnya.
TABEL 1.4
| Aluminium mentah (dimurnikan secara elektrolitik 99.993-99.994%) | Aluminium setelah zona leleh |
||
| grafit, vakum | alund, udara |
||
| Tembaga | 1,9 | 0,02 | 0,08 |
| Arsenik | 0,15 | 0,0015 | 0,001 |
| Antimon | 1,2 | 0,03 | 0,02 |
| Uranus | 0,002 | - | - |
| Besi | 3 | ≤0,2 | ≤0,3 |
| galium | 0,3 | 0,02 | 0,05 |
| mangan | 0,2-0,3 | 0,1-0,2 | 0,15 |
| Skandium | 0,4-0,5 | 0,4-0,5 | 0,4-0,5 |
| Itrium | 0,02-0,04 | <<0,001 | <<0,001 |
| Lutetium | 0,002-0,004 | <<0,0001 | <<0,0001 |
| Holmium | 0,005-0,01 | <<0,0001 | <<0,0001 |
| Gadolinium | 0,02-0,04 | <<0,01 | <<0,01 |
| Terbium | 0,003-0,006 | <<0,001 | <<0,001 |
| Samarium | 0,05-0,01 | <<0,0001 | <<0,0001 |
| Neodimium | 0,1-0,2 | <<0,01 | <<0,01 |
| Praseodymium | 0,05-0,1 | <<0,001 | <<0,001 |
| Cerium | 0,3-0,6 | <<0,01 | <<0,01 |
| Lantanum | 0,01 | <<0,001 | <<0,001 |
| Nikel | 2,3 | - | <1 |
| Kadmium | 3,5 | <<0,01 | 0,02-0,07 |
| Seng | 20 | <<0,05 | 1 |
| Kobalt | 0,01 | <<0,01 | <<0,01 |
| Sodium | 1-2 | <0,2 | <0,2 |
| Kalium | 0,05 | 0,01 | 0,01 |
| Barium | 6 | - | - |
| Klorin | 0,01 | <0,01 | <0,01 |
| Fosfor | 3 | 0,04 | - |
| Sulfur | 15 | 0,5-1,5 | - |
| Karbon | 1-2 | - | 1-2 |
| Catatan. Jumlah telurium, bismut, perak, molibdenum, kromium, zirkonium, kalsium, strontium, rubidium, serium, indium, selenium dan merkuri dalam aluminium setelah peleburan zona berada di bawah sensitivitas analisis radioaktif. | |||
Di meja Gambar 1.5 (lihat di bawah) menunjukkan hasil analisis spektral massa dan pengukuran aluminium R 293 K / R 4,2 K yang diperoleh melalui peleburan zona kaskade. Dari data yang disajikan, dapat disimpulkan bahwa kemurnian aluminium yang ditentukan oleh selisih sepuluh pengotor utama (Si, Fe, Mg, Mn, Ti, Cu, Cr, Zn, Na, dan V), adalah >99,9999%. . Kesimpulan tersebut secara tidak langsung diperkuat dengan nilai R 293 K /R 4,2 K yang pada seluruh sampel >30ּ10 3.
Untuk memperoleh logam dengan kemurnian 99,9999%, cukup melakukan dua tahap peleburan zona (lihat Tabel 1.5). Peningkatan lebih lanjut dalam jumlah kaskade tidak meningkatkan kemurnian aluminium, meskipun hal ini meningkatkan hasil keseluruhan logam dengan kemurnian 99,9999%.
Proses lain yang mungkin untuk memperoleh aluminium dengan kemurnian tinggi adalah distilasi melalui subhalida, khususnya melalui aluminium subfluorida.
Tekanan uap jenuh logam aluminium tidak cukup tinggi untuk melakukan distilasi langsung pada tingkat yang dapat diterima. Namun, ketika dipanaskan dalam ruang hampa (pada 1000-1050°C) dengan AlF 3, aluminium membentuk subfluorida AlF yang sangat mudah menguap, yang disuling ke zona dingin (800°C), di mana aluminium kembali terurai (disproporsi) dengan pelepasan dari aluminium murni:
Kemungkinan pemurnian mendalam aluminium dari pengotor terutama disebabkan oleh fakta bahwa kemungkinan pembentukan subsenyawa aluminium jauh lebih besar daripada kemungkinan pembentukan subsenyawa pengotor.
TABEL 1.5
HASIL ANALISIS SPEKRAL MASSA DAN PENGUKURAN R 293 K/R 4,2 K LELTING ZONA CASCADE ALUMINIUM.
| Jumlah tahapan | |||||||
| Asli | 18,3 | 0,210 | <0,103 | 0,89 | <0,061 | 0,069 | 1,544 |
| A999 | |||||||
| 2 | 36,5 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 38,0 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 39,5 | 0,073 | <0,103 | 0,045 | <0,061 | 0,07 | 0,563 |
| 3 | 32,0 | 0,204 | <0,103 | 0,006 | <0,061 | 0,017 | 0,502 |
| 3 | 30,0 | 0,073 | 0,100 | 0,006 | 0,020 | 0,07 | 0,480 |
| 3 | 32,0 | 0,052 | 0,100 | 0,006 | 0,061 | 0,07 | 0,500 |
| 4 | 40,0 | <0,021 | <0,103 | 0,006 | 0,061 | 0,07 | 0,472 |
| 4 | 30,5 | 0,031 | 0,100 | 0,006 | 0,061 | 0,07 | 0,479 |
| 5 | 34,0 | 0,104 | <0,060 | 0,006 | 0,061 | 0,017 | 0,459 |
| Catatan: 1. Jumlah pengotor diberikan dengan memperhitungkan pengotor lainnya, yang kandungannya dalam semua sampel adalah ×10 –4%:<0,071 Cu; <0,038 Cr; 0,048 Zn; 0,017 Na; 0,037 V. 2. При подсчете суммы примесей принимали их максимальное значение, равное пределу чувствительности анализа, например <0,061 считали как 0,061. |
|||||||
Kandungan pengotor pada aluminium yang disuling melalui subfluorida berbanding terbalik dengan massa ingot yang dihasilkan. Dalam ingot seberat 1,5-1,7 kg, kandungan total pengotor (Si, Fe, Cu, Mg) adalah 11ּ10–4%, dan kandungan gas 0,007 cm 3 /100 g Resistansi sisa spesifik (ρ ○) pada helium cair suhu untuk logam tersebut adalah (1.7±2.0)ּ10 –10 Ohmּcm. Distilasi aluminium melalui subfluorida memiliki sejumlah kelemahan (produktivitas yang relatif rendah, pemurnian magnesium yang kurang mendalam, dll.), sehingga metode ini belum dikembangkan secara industri.
Metode juga telah dikembangkan untuk memproduksi aluminium dengan kemurnian tinggi melalui elektrolisis senyawa organoaluminium kompleks, yang berbeda dalam komposisi elektrolitnya. Misalnya, di Jerman mereka menggunakan metode elektrolisis larutan 50% NaFּ2Al (C 2 H 5) 3 dalam toluena. Pemurnian dilakukan pada suhu 100°C, tegangan elektroliser 1,0-1,5 V dan rapat arus 0,3-0,5 A/dm 2 menggunakan elektroda aluminium. Efisiensi arus katoda 99%. Pemurnian elektrokimia dalam elektrolit organoaluminum secara signifikan mengurangi kandungan mangan dan skandium, yang praktis tidak dihilangkan selama pemurnian zona. Kerugian dari metode ini adalah produktivitasnya yang rendah dan bahaya kebakaran yang tinggi.
Untuk pemurnian aluminium lebih dalam dan memperoleh logam dengan kemurnian 99,99999% atau lebih, Anda dapat menggunakan kombinasi metode di atas: elektrolisis senyawa organoaluminium atau sublimasi melalui subfluorida, diikuti dengan peleburan zona aluminium yang dihasilkan. Misalnya, dengan pemurnian zona aluminium berulang kali yang diperoleh melalui elektrolisis senyawa organoaluminum, dimungkinkan untuk memperoleh logam dengan kemurnian tinggi dengan kandungan pengotor ×10–9%: Fe 50; Ya<500; Cu 10; Mg 30; Mn 5; Ti <500; Cr 20; Zn <50; Co <1; Ag <5; Sb <1 и Se 3.
Aplikasi
Kombinasi sifat fisik, mekanik dan kimia aluminium menentukan penggunaannya secara luas di hampir semua bidang teknologi, terutama dalam bentuk paduannya dengan logam lain. Dalam bidang teknik kelistrikan, aluminium berhasil menggantikan tembaga, terutama dalam produksi konduktor masif, misalnya pada saluran udara, kabel tegangan tinggi, busbar switchgear, trafo (konduktivitas listrik aluminium mencapai 65,5% dari konduktivitas listrik tembaga, dan itu lebih dari tiga kali lebih ringan dari tembaga; dengan penampang yang memberikan konduktivitas yang sama, massa kabel aluminium adalah setengah dari tembaga). Aluminium ultra murni digunakan dalam produksi kapasitor dan penyearah listrik, yang tindakannya didasarkan pada kemampuan film aluminium oksida untuk mengalirkan arus listrik hanya dalam satu arah. Aluminium ultra-murni, dimurnikan dengan peleburan zona, digunakan untuk sintesis senyawa semikonduktor tipe A III B V, digunakan untuk produksi perangkat semikonduktor. Aluminium murni digunakan dalam produksi berbagai jenis cermin reflektif. Aluminium dengan kemurnian tinggi digunakan untuk melindungi permukaan logam dari korosi atmosferik (pelapis, cat aluminium). Memiliki penampang serapan neutron yang relatif rendah, aluminium digunakan sebagai material struktural pada reaktor nuklir.
Tangki aluminium berkapasitas besar menyimpan dan mengangkut gas cair (metana, oksigen, hidrogen, dll.), asam nitrat dan asetat, air bersih, hidrogen peroksida, dan minyak nabati. Aluminium banyak digunakan pada peralatan dan perlengkapan industri makanan, untuk kemasan makanan (dalam bentuk foil), dan untuk produksi berbagai jenis produk rumah tangga. Konsumsi aluminium untuk finishing bangunan, arsitektur, transportasi dan struktur olahraga meningkat tajam.
Dalam metalurgi, aluminium (selain paduan berdasarkan itu) adalah salah satu bahan tambahan paduan yang paling umum dalam paduan berdasarkan Cu, Mg, Ti, Ni, Zn dan Fe. Aluminium juga digunakan untuk mendeoksidasi baja sebelum dituangkan ke dalam cetakan, serta dalam proses produksi logam tertentu menggunakan aluminotermi. Berbahan dasar aluminium, SAP (sintered aluminium powder) dibuat menggunakan metalurgi serbuk, yang memiliki ketahanan panas tinggi pada suhu di atas 300°C.
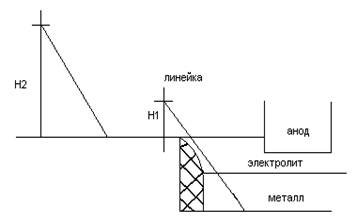
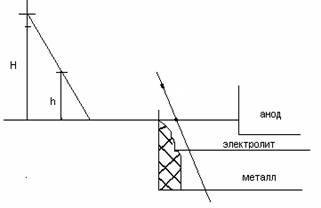
Pengayaan gas anoda dengan karbon monoksida dan munculnya partikel karbon yang sangat kecil dalam elektrolit. Komplikasi lain dari proses katodik adalah pelepasan kation Na+, yang selalu terkandung dalam aluminium selama produksinya. Jumlah natrium yang dilepaskan tergantung pada rasio kriolit (CR) elektrolit. Ketika CO berkurang dari 3 menjadi 2,5, kandungan natrium berkurang 2,5 kali lipat. Pada suhu...
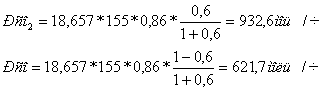
Dalam hal menggunakan anoda pembakaran sendiri, sebagian massa anoda meninggalkan proses dalam bentuk komponen kokas yang mudah menguap. Dalam perhitungan material, produktivitas elektroliser dan konsumsi bahan baku untuk produksi aluminium ditentukan. produktivitas elektroliser (P), dengan kuat arus J = 155A dan keluaran arus yang diterima = 86%, adalah: dimana 0,3354 adalah ekuivalen elektrokimia untuk; - ...
Rasio pengotor besi dan silikon yang termasuk dalam komposisi juga berbeda. Huruf E pada grade AE berarti aluminium grade ini ditujukan untuk produksi kabel listrik. Persyaratan tambahan untuk sifat-sifat aluminium adalah hambatan listrik yang rendah, yang untuk kawat yang dibuat darinya tidak boleh lebih dari 0,0280 ohm mm m pada 20 C. Aluminium digunakan untuk produksi produk darinya...
1.1 Memperoleh alumina dari bijih
Alumina diproduksi dengan tiga cara: basa, asam dan elektrolitik. Yang paling luas adalah metode alkaline (metode K.I. Bayer, dikembangkan di Rusia pada akhir abad sebelumnya dan digunakan untuk memproses bauksit bermutu tinggi dengan sejumlah kecil (hingga 5-6%) silika). Sejak itu, implementasi teknisnya telah ditingkatkan secara signifikan. Diagram produksi alumina menggunakan metode Bayer ditunjukkan pada Gambar. 1.
Inti dari metode ini adalah larutan aluminium cepat terurai ketika aluminium hidroksida dimasukkan ke dalamnya, dan larutan sisa dekomposisi setelah penguapan dalam kondisi pengadukan intensif pada suhu 169-170 o C dapat kembali melarutkan alumina yang terkandung dalam bauksit. Metode ini terdiri dari operasi dasar berikut:
Persiapan bauksit, yang terdiri dari penghancuran dan penggilingan di pabrik; bauksit, alkali kaustik dan sedikit kapur disuplai ke pabrik, yang meningkatkan pelepasan Al 2 O 3; pulp yang dihasilkan diumpankan untuk pencucian;
Pencucian bauksit (saat ini, blok autoklaf berbentuk bulat yang masih digunakan telah sebagian digantikan oleh autoklaf berbentuk tabung, dimana pencucian terjadi pada suhu 230-250 ° C (500-520 K), yang terdiri dari dekomposisi kimianya dari interaksi dengan larutan alkali berair; Ketika bereaksi dengan alkali, aluminium oksida hidrat masuk ke dalam larutan dalam bentuk natrium aluminat:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH) 3 + NaOH → NaAlO 2 + 2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H 2 O;
dalam larutan, natrium aluminat dan natrium silikat membentuk natrium aluminosilikat yang tidak larut; oksida titanium dan besi masuk ke dalam residu yang tidak larut, memberikan warna merah pada residu; residu ini disebut lumpur merah. Setelah pelarutan selesai, natrium aluminat yang dihasilkan diencerkan dengan larutan alkali berair sekaligus menurunkan suhu sebesar 100°C;
Pemisahan larutan aluminat dari lumpur merah, biasanya dilakukan dengan cara dicuci dengan pengental khusus; Akibatnya lumpur merah mengendap, dan larutan aluminat ditiriskan lalu disaring (diklarifikasi). Dalam jumlah terbatas, lumpur digunakan, misalnya sebagai bahan tambahan semen. Tergantung pada jenis bauksit, 1 ton aluminium oksida yang dihasilkan menghasilkan 0,6-1,0 ton lumpur merah (residu kering);
Dekomposisi larutan aluminat. Itu disaring dan dipompa ke dalam wadah besar dengan agitator (pengurai). Aluminium hidroksida Al(OH) 3 diekstraksi dari larutan lewat jenuh setelah pendinginan hingga 60°C (330 K) dan pengadukan konstan. Karena proses ini berlangsung lambat dan tidak merata, dan pembentukan serta pertumbuhan kristal aluminium hidroksida sangat penting selama pemrosesan lebih lanjut, sejumlah besar hidroksida padat - sebutir - ditambahkan ke pengurai:
Na 2 OּAl 2 O 3 +4H 2 O→Al(OH) 3 +2NaOH;
Isolasi aluminium hidroksida dan klasifikasinya; hal ini terjadi pada hidrosiklon dan filter vakum, dimana endapan yang mengandung 50-60% partikel Al(OH) dipisahkan dari larutan aluminat. Sebagian besar hidroksida dikembalikan ke proses dekomposisi sebagai bahan benih, yang tetap beredar dalam jumlah yang tidak berubah. Residu setelah dicuci dengan air menuju kalsinasi; filtrat juga dikembalikan ke sirkulasi (setelah konsentrasi dalam evaporator - untuk pencucian bauksit baru);
Dehidrasi aluminium hidroksida (kalsinasi); Ini adalah langkah terakhir dalam produksi alumina; ini dilakukan dalam tanur putar berbentuk tabung, dan baru-baru ini juga dalam tanur dengan pergerakan material yang turbulen pada suhu 1150-1300 o C; aluminium hidroksida mentah, melewati tanur putar, dikeringkan dan didehidrasi; Ketika dipanaskan, transformasi struktural berikut terjadi secara berurutan:
| Al(OH) 3 →AlOOH→ γ-Al 2 O 3 → α-Al 2 O 3 |
Akhirnya alumina yang dikalsinasi mengandung 30-50% α-Al 2 O 3 (korundum), sisanya γ-Al 2 O 3.
Metode ini mengekstraksi 85-87% dari total alumina yang dihasilkan. Aluminium oksida yang dihasilkan merupakan senyawa kimia kuat dengan titik leleh 2050 o C.
1.2 Pembuatan aluminium dari oksidanya
Reduksi elektrolitik aluminium oksida yang dilarutkan dalam lelehan berbasis kriolit dilakukan pada suhu 950-970°C dalam elektroliser. Elektroliser terdiri dari bak yang dilapisi dengan blok karbon, di bagian bawahnya disuplai arus listrik. Aluminium cair yang dilepaskan di tungku, yang berfungsi sebagai katoda, lebih berat daripada garam cair elektrolit, oleh karena itu, ia dikumpulkan di atas dasar batubara, dari mana ia dipompa keluar secara berkala (Gbr. 2). Anoda karbon direndam dalam elektrolit di atasnya, yang terbakar dalam atmosfer oksigen yang dilepaskan dari aluminium oksida, melepaskan karbon monoksida (CO) atau karbon dioksida (CO2). Dalam prakteknya, dua jenis anoda digunakan:
a) anoda Zederberg yang dapat terbakar sendiri, terdiri dari briket, yang disebut “roti” massa Zederberg (batubara abu rendah dengan kadar tar batubara 25-35%), dimasukkan ke dalam cangkang aluminium; di bawah pengaruh suhu tinggi, massa anoda dibakar (disinter);
b) anoda yang dipanggang atau “kontinu” yang terbuat dari balok karbon besar (misalnya, 1900x600x500 mm dengan berat sekitar 1,1 ton).
Kekuatan arus dalam elektroliser adalah 150.000 A. Mereka dihubungkan ke jaringan secara seri, yaitu, suatu sistem (seri) diperoleh - deretan elektroliser yang panjang.
Tegangan pengoperasian pada bak, 4-5 V, secara signifikan lebih tinggi daripada tegangan penguraian aluminium oksida, karena kehilangan tegangan di berbagai bagian sistem tidak dapat dihindari selama pengoperasian. Keseimbangan bahan baku dan energi pada produksi 1 ton aluminium disajikan pada Gambar. 3.
Elektrolisis aluminium klorida (metode Alcoa)
Dalam bejana reaksi, aluminium oksida diubah terlebih dahulu menjadi aluminium klorida. Kemudian, dalam bak berinsulasi rapat, terjadi elektrolisis AlCl 3 yang dilarutkan dalam garam cair KCl dan NaCl. Klorin yang dilepaskan selama proses ini disedot dan disuplai untuk didaur ulang; aluminium diendapkan pada katoda.
Keuntungan metode ini dibandingkan elektrolisis lelehan kriolit-alumina cair (Al 2 O 3 yang dilarutkan dalam kriolit Na 3 AlF 6) adalah: menghemat energi hingga 30%; kemungkinan penggunaan aluminium oksida, yang tidak cocok untuk elektrolisis tradisional (misalnya, Al 2 O 3 dengan kandungan silikon tinggi); mengganti kriolit yang mahal dengan garam yang lebih murah; hilangnya bahaya pelepasan fluorida.
Reduksi aluminium klorida dengan mangan (metode Toth)
Ketika direduksi dengan mangan, aluminium dilepaskan dari aluminium klorida. Melalui kondensasi terkendali, kontaminan terkait klorin dilepaskan dari aliran mangan klorida. Ketika klorin dilepaskan, mangan klorida dioksidasi menjadi oksida mangan, yang kemudian direduksi menjadi mangan, cocok untuk penggunaan sekunder. Informasi dalam publikasi yang ada sangat tidak akurat, sehingga dalam hal ini evaluasi metode tersebut perlu ditinggalkan.


